トップページ > 広報活動 > プレスリリース > 大腸がん幹細胞を抑制する新規化合物を創出
大腸がん幹細胞を抑制する新規化合物を創出
2016年8月26日
国立研究開発法人国立がん研究センター
国立研究開発法人 理化学研究所
カルナバイオサイエンス株式会社
国立研究開発法人 日本医療研究開発機構
本研究成果のポイント
- 大腸がんの90%以上でおこる遺伝子異常を標的とした新規化合物を産学の共同研究で創出いたしました。
- この化合物は大腸がんの根元の細胞(がん幹細胞)の働きを抑制し、腫瘍を作れなくすることが分かりました。
国立研究開発法人国立がん研究センター、国立研究開発法人理化学研究所、カルナバイオサイエンス株式会社の研究グループは、大腸がんの発生に必須なシグナル伝達経路を阻害することができる新規化合物を創出しました。大腸がんの90%以上の方で、このシグナル伝達経路に遺伝子異常がおこることは以前より分かっていましたが、治療薬として実用化されたものはありません。
従来の抗がん剤は腫瘍を縮小することができましたが、薬剤が効かない「がん幹細胞(がんの根元の細胞)」が残ってしまい、がんが再発する原因になっていました。この新規化合物はがん幹細胞が腫瘍を再度作る働きを抑えることが動物実験で明らかになりました。国立がん研究センターでは、現在、大腸がんに対する新規治療薬として実用化を目指しています。
本研究成果は、国立研究開発法人日本医療研究開発機構(AMED)などの支援を受け行ったもので、研究成果は国際学術誌「Nature Communications」に発表されました(8月26日付けオンライン掲載)。
研究背景
わが国では年間約5万人が大腸がんで死亡し、その治療は大きな問題になっています。転移のない大腸がんの多くは外科切除のみで治癒しますが、遠隔転移や術後再発を来たした方の治療は未だに困難です。近年、多剤併用の化学療法や分子標的治療の進歩により進行例であっても2年を超える生存が可能になってきましたが、治療を続けるとしだいに化学療法に抵抗性となり、遠隔転移のあった大腸がん患者さんの5年生存率は約15%にとどまります。
がんの治療抵抗性の原因に、「がん幹細胞」の関与が考えられています。がん幹細胞はポンプのようなタンパク質により薬剤を細胞の外に排出し、活性酸素除去機構を持ち、冬眠したような状態で長期間潜み続けるため、従来の抗がん剤では根絶することができません。いわばがんの「根元」のような細胞です。下の図で赤く染色されているのは、ヒトの大腸がんにみられたがん幹細胞マーカーを発現する細胞です。
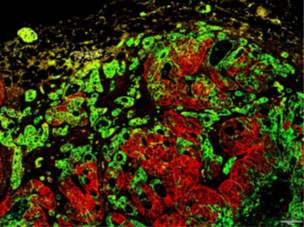
がん幹細胞は自己複製能(自分と同じ細胞を作る能力)と高い造腫瘍性(腫瘍を作る能力)を持ち、治療後に少数でも残存すると、腫瘍を再構築できるため、再発の原因となります。そのため、がん幹細胞を標的とする新規治療薬の開発が期待されています(下図)。
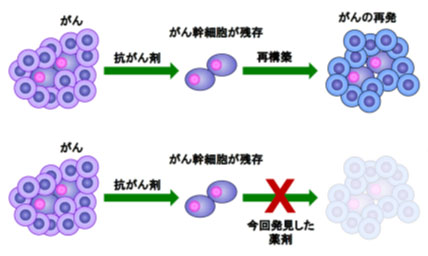
大腸がんの90%以上の症例では、APC、β-catenin (CTNNB1)、TCF4(TCF7L2)などのWntシグナル遺伝子に変異が認められます。これらの変異はWntシグナル伝達経路(注1)を恒常的に活性化し、大腸がんの元となるがん幹細胞を発生させると考えられています。そのため、Wntシグナル伝達経路を遮断することで大腸がんが治療できると考えられ、多くの研究者や企業がWntシグナルを標的とした創薬を試みていますが、医薬品として実用化されたものはありません。
研究手法と成果
TNIK酵素の働きを阻害すことでWntシグナルを遮断できることを発見
研究グループはTNIK(注2)というリン酸化酵素(参考論文1)が、Wntシグナル経路の活性化に必要なことを発見しました。TNIKは大腸がん細胞の増殖維持に必須であり(参考論文2)、その活性を阻害できる化合物が同定できれば、治療薬になると考えられました(参考論文3)。
TNIKの活性を阻害する薬剤の発見
国立研究開発法人国立がん研究センターとカルナバイオサイエンス株式会社との産学共同で化合物ライブラリーをスクリーニングし、徹底的な誘導体合成から最終的にTNIKの酵素活性を低濃度(IC50値21 nM)で阻害する新規化合物NCB-0846を同定しました。理化学研究所はNCB-0846とTNIKの複合体のX線結晶構造解析を行い、この化合物がTNIKの酵素活性を抑制するメカニズムを明らかにいたしました。
大腸がん幹細胞の機能を抑制
大腸がん幹細胞は高い造腫瘍性があり、細胞一個からでも腫瘍を再構築することができますが、NCB-0846はその働きを強く抑制することが分かりました(下図、上段)。さらに、NCB-0846は経口投与可能であり、ヒト大腸がん細胞を移植したマウスに投与すると、がんの増殖及びがん幹細胞マーカーCD44の発現が顕著に抑制されることが分かりました(下図、下段)。がん幹細胞の働きを、これほど強く抑える薬剤は今まで発見されておりませんでした。
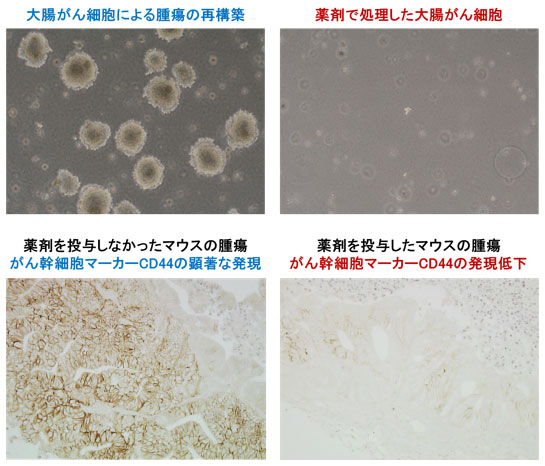
今後の展望
今回研究グループが発見した化合物は、このがん幹細胞が腫瘍を形成する働きを抑え、「がんを根絶やし」にすることが期待できるものです。この化合物が治療薬として実用化されると、従来の抗がん剤が効かなくなった患者さんでも、新しい治療の機会が得られる可能性があります。研究グループでは臨床試験の前段階となる非臨床試験を実施中で、今後、大腸がんに対する新規薬剤として実用化を目指していきます。
共同研究者
- 国立研究開発法人国立がん研究センター
代表者:研究所 創薬臨床研究分野長 山田哲司 - 国立研究開発法人理化学研究所
代表者:ライフサイエンス技術基盤研究センター 構造・合成生物学部門
部門長 白水美香子(副センター長) - カルナバイオサイエンス株式会社
代表者:研究開発本部 本部長 澤匡明
発表論文
- 雑誌名:Nature Communications, 2016, on line publication.
- タイトル:TNIK Inhibition Abrogates Colorectal Cancer Stemness.
- 著者:Mari Masuda, Yuko Uno, Naomi Ohbayashi, Hirokazu Ohata, Ayako Mimata, Mutsuko Kukimoto-Niino, Hideki Moriyama, Shigeki Kashimoto, Tomoko Inoue, Naoko Goto, Koji Okamoto, Mikako Shirouzu, Masaaki Sawa, Tesshi Yamada.(責任著者)
- Doi:10.1038/ncomms12586
- URL:http://www.nature.com/naturecommunications(外部サイトにリンクします)
本研究への支援
本研究は、下記機関より資金的支援を受けて実施されました。
国立がん研究センター研究開発費
日本医療研究開発機構 創薬支援推進事業(創薬総合支援事業)
医薬基盤研究所 先駆的医薬品・医療機器研究発掘支援事業
参考論文
- Shitashige et al., Gastroenterology. 2008 Jun;134(7):1961-71.
- Shitashige et al., Cancer Res. 2010 Jun 15;70(12):5024-33.
- Sawa et al., Expert Opin Ther Targets. 2015 Oct 6時1分-11.
用語解説
- 注1 Wntシグナル経路
Wntと呼ばれる分泌タンパク質が細胞に作用することにより活性化される細胞内シグナル伝達機構で、様々な生物の初期発生において形態形成や細胞極性の決定などの重要な生命現象に関係している。例えば、アフリカツメガエルの初期胚でWntシグナルの働きを抑えると体軸の形成が失われてしまう。ヒトではWntシグナルは正常の腸上皮の幹細胞の維持に必須で、APC遺伝子などの変異によりシグナルが活性化すると、大腸がんの元になる腺腫細胞が発生する(下図)。さらにTP53、KRAS、SMAD4などの他の遺伝子異常が蓄積することでがん細胞になる。
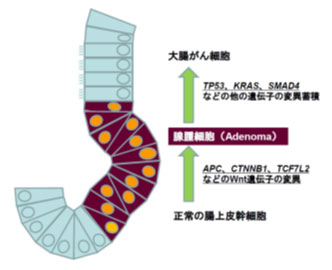
- 注2 TNIK (TRAF2 and NCK-interacting protein kinase)
Wntシグナルは良い治療標的になると期待されているが、医薬品として実用化されたものはない。これは大腸がんの80%以上でAPC遺伝子に機能喪失変異があり、その下流でWntシグナルを遮断する必要があるからである。そこで、国立がん研究センターでは、Wntシグナル伝達経路の最下流で実行分子として働く転写因子TCF4に注目し、これと相互作用する分子を免疫沈降法と質量分析で徹底的にプロテオーム解析し、リン酸化酵素のTNIKを同定した。TNIKはWntシグナルの活性化に必須で、その酵素活性を阻害することで、大腸がんの治療薬になることが期待されていた。
プレスリリース
- 大腸がん幹細胞を抑制する新規化合物を創出
関連ファイルをご覧ください。
報道関係からのお問い合わせ先
- 国立研究開発法人国立がん研究センター
企画戦略局 広報企画室
郵便番号:104-0045 東京都中央区築地5-1-1
電話番号:03-3542-2511(代表)
ファクス番号:03-3542-2545
Eメール: ncc-admin●ncc.go.jp(●を@に置き換えください) - カルナバイオサイエンス株式会社
経営企画部
郵便番号:650-0047 神戸市中央区港島南町1丁目5番5号 BMA3F
電話番号:078-302-7075
ファクス番号:078-302-6665
Eメール: ir-team●carnabio.com(●を@に置き換えください) - 国立研究開発法人 理化学研究所
広報室 報道担当
電話番号:048-467-9272
ファクス番号:048-462-4715
Eメール:ex-press●riken.jp(●を@に置き換えください)
支援機関窓口
- 国立研究開発法人日本医療研究開発機構(AMED)
創薬支援戦略部 西日本統括部
郵便番号:530-0011 大阪府大阪市北区大深町3-1 グランフロント大阪 タワーB11F
電話番号:06-6372-1771 ファクス:06-6372-1772
Eメール:id3desk●amed.go.jp(●を@に置き換えください)
がん対策全般に関するお問い合わせ先
- 厚生労働省 健康局 がん・疾病対策課
郵便番号:100-8916 東京都千代田区霞が関1丁目2番2号
電話番号:03-5253-111
