トップページ > 広報活動 > プレスリリース > 肝臓を再構築する肝前駆細胞へのリプログラミングにラット、マウスで成功再生医療やがん治療への応用に期待
肝臓を再構築する肝前駆細胞へのリプログラミングにラット、マウスで成功再生医療やがん治療への応用に期待
2016年11月11日
国立研究開発法人 国立がん研究センター
国立研究開発法人 日本医療研究開発機構
本研究成果のポイント
- 成熟肝細胞から、肝臓を再構築する肝前駆細胞へのリプログラミングおよび安定培養に成功。
- 培養に成功した肝前駆細胞を、肝障害をもつ動物の肝臓に移植すると高い再生能力を示し、75%から90%という極めて高い効率でホスト肝臓を再構築した。
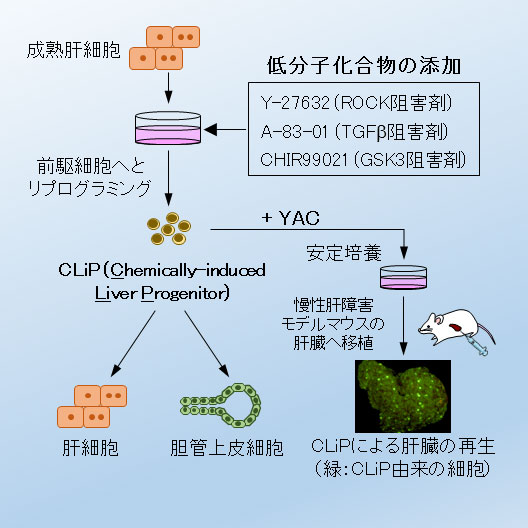
国立がん研究センター(理事長:中釜 斉、東京都中央区)研究所分子細胞治療研究分野落谷孝広分野長、勝田毅研究員の研究チームは、低分子化合物を用いることで遺伝子組み換えを行うことなく、ラットおよびマウスの成熟肝細胞から、生体外で増殖可能で、かつ生体内で高い再生能を示し肝臓を再構築する肝前駆細胞(Chemically-induced Liver Progenitors:CLiPと命名)へのリプログラミングに成功しました。
これまで、重篤肝疾患に対する治療は肝移植しかありませんでしたが、再生能を有する移植可能な成熟肝細胞を生体外で安定かつ安全に供給する方法はこれまで開発されていません。今後、ヒトの肝細胞を利用したCLiPを開発することにより、患者自身の検体をソースとした新たな細胞治療や、肝がんの発生機序の解明への応用が期待されます。
本研究は、国立研究開発法人日本医療研究開発機構(AMED)B型肝炎創薬実用化等研究事業「HBVの感染初期過程を評価する系の開発とそれを用いた感染阻害低分子化合物およびレセプター探索」の支援を受け行いました。
研究成果は、国際科学雑誌「Cell Stem Cell」(11月10日付け:日本時間11月11日2時)に掲載されました。
背景
肝臓には臓器の中で唯一再生能力があるため病気があっても、修復、再生し機能が維持されます。しかし、慢性肝炎などでは再生能力が低下し、線維化や肝硬変へと進行し、最終的には肝がんが引き起こされることもあります。このような重篤な肝疾患に対する治療法は、現在、肝移植しかありません。しかし、絶対的にドナーが不足しており、これを代替するため肝細胞移植が提案されてきましたが、肝移植治療同様にドナー不足問題を抱えることに加え、凍結保存に伴う肝細胞の機能低下や再生能低下の問題もあり、現実的な手段とは見なされていません。
そのため近年、多能性幹細胞をソースとして、再生能を有する移植可能な肝前駆細胞や成熟肝細胞を生体外で安定かつ安全に供給する試みが行われています。しかし、多能性幹細胞からの肝前駆細胞や成熟肝細胞の誘導は極めて難しく、実際に肝障害動物への移植後の生着率・再生能は依然極めて低い状況です。また、多能性幹細胞の場合は、移植後のがん化などの懸念もあり、実現化には多くの課題を抱えています。
また、肝臓内には成熟肝細胞よりも高い増殖能をもつ肝前駆細胞が存在することも知られており、この細胞を利用した細胞治療の可能性も検討されていますが、採取が困難であり、培養方法が十分に確立されていないことなどの問題が残っています。こうした背景から、肝細胞を生体外で安定かつ安全に増殖させる技術が強く求められています。
慢性肝障害では成熟肝細胞の増殖能が低下して再生が不十分となり、症状の進行とともに、肝前駆細胞が増殖し始めます。これらの肝前駆細胞は正常時にはほとんどその存在を認めることができないことから、正常肝臓内ではその数が極めて少なくかつ休眠状態にあり、慢性肝炎に陥った際に初めて活性化されて再生に寄与する、いわば切り札の細胞であると考えられていました。ところが最近の研究から、肝前駆細胞だと考えられていたこれらの細胞が、実際には休眠状態から活性化された細胞ではなく、成熟した肝細胞から変化した細胞であるという意外な事実が明らかとなりました。つまり、慢性肝障害時に受ける何らかの刺激によって、成熟肝細胞が肝前駆細胞へとリプログラミングされるということが明らかとなったのです。この事実は肝臓の基礎研究に大きなインパクトを与えるとともに、肝臓の再生医療にも重要な示唆をもたらしました。すなわち、成熟肝細胞から増殖能の高い肝前駆細胞を作り出せる可能性が示されたのです。
研究手法と成果
研究チームでは、シグナル伝達阻害剤である低分子化合物に着目し、様々な組織由来の幹細胞を生体外で安定に培養できることを報告してきました(Kawamata & Ochiya. 2010, PNAS; Kawamata & Ochiya. 2012 Sci. Rep.)。この経験と知識を背景に、本研究ではこれらの低分子化合物を用い、生体外で成熟肝細胞を肝前駆細胞へとリプログラミングできることを明らかにしました。この発見は、生体内で観察されている成熟肝細胞のリプログラミング現象をさらに確かなものとするための貴重な証拠となるとともに、肝臓の再生医療における新たなアプローチを提案する重要な成果となります。
成熟肝細胞から高い分化能をもった肝前駆細胞(CLiP)へのリプログラミングに成功
当研究室で幹細胞維持に有用であることを確認していた4つの低分子化合物の全ての組み合わせを添加してラットの肝臓細胞を培養し、細胞が増殖するかどうかを検討しました。その結果、3つの化合物の組み合わせ(Y-27632、A-83-01、CHIR99021)を加えたときに、肝前駆細胞だけでなく、驚いたことに成熟肝細胞までもが増殖能を獲得し、形態的に幹前駆様の細胞へと変化することが明らかとなりました。実際に遺伝子・タンパクの発現解析結果からも、複数の肝前駆細胞マーカーの発現が低分子化合物存在下で上昇していることが確認できました。さらに、肝分化誘導または胆管分化誘導への刺激を加えると、これらの肝前駆様細胞が実際に肝細胞または胆管上皮細胞へと分化することが確認でき、表現型としても確かな肝前駆細胞であることが明らかとなりました。
この細胞を、Chemically-induced Liver Progenitors: CLiPと命名しました。また、CLiPについて以下の特長も確認しました。
肝前駆細胞(CLiP)の特長
- 低分子化合物存在下で増殖能を失うことなく安定に培養可能
- 長期培養後も肝分化誘導刺激を加えれば容易に肝細胞へと再分化させることが可能
- 一方で、低分子化合物を除去すると即座に増殖能を失う。このことから、CLiPががん細胞特有の自律的な(増殖刺激に依存しない)増殖能を獲得した細胞ではないことが確認できた
- ラットだけでなくマウスの肝細胞を用いても、CLiPを誘導できることが確認できた
正常なラット肝細胞が慢性肝炎マウスの肝臓の75%から90%を置換
長期培養に成功したラット由来のCLiPを、慢性肝炎モデルの免疫不全マウス(cDNA-uPA/SCIDマウス)の肝臓に移植し再生能力を評価しました。その結果、全てのマウス肝臓の75%から90%が、ラット細胞に置換されていることが判明しました。実際に、マウス血中のラットアルブミン濃度も移植後増加しており、CLiP由来の肝細胞が肝機能を示すことが確かめられました。一方で、マウス血中のラットアルブミン濃度は生理的に十分な量(約15ミリグラム/ミリリットル)にまで達すると、その後は増加することなく一定量に落ち着き、移植されたCLiPの増殖が無秩序なものでないことが確かめられました。
置換率が75%から90%に達した移植後8週間で摘出したマウス肝臓は、大きさも正常で、かつ病理学的にも正常な構造であり、安全性の面でも問題ないことが示されました。
これまで様々な研究で多能性幹細胞由来の肝(前駆)細胞や成体肝臓から採取した肝前駆細胞を用いた移植実験が行われてきましたが、これらの細胞によって置換される肝細胞の割合は15%以下であり、十分な肝再生の実現には至っていませんでした。
今後の期待
今回の報告では、これまで精力的に取り組まれてきた、多能性幹細胞から肝(前駆)細胞へと分化誘導するアプローチとは反対の、成熟細胞から前駆細胞へと部分的にリプログラミングするという新たなアプローチを提案できました。このような部分的リプログラミングというアプローチは、肝臓だけでなく様々な臓器を対象として展開できる可能性が十分にあり、再生医療分野における新たな方向性を示すことになります。研究チームは、このアプローチをベースに、凍結保存されているヒト肝細胞、あるいは生検サンプルから採取したヒト肝細胞をソースに、移植治療に使えるヒトCLiPの誘導を目指して研究を続けています。
また、本研究をがん研究へも応用することが可能だと考えています。肝がん細胞は慢性肝障害時に出現する肝前駆細胞に由来すると考えられています。CLiP技術を用いて、CLiP細胞にある変異が加わることで自律的な増殖能を獲得し、がん細胞へと形質転換されるかどうかを調べることでこの仮説に対して新たな知見が得られる可能性があります。これまで患者検体を用いたゲノム解析などの研究から、数多くの肝がん関連遺伝子が同定されていますが、発がん過程におけるそれぞれの遺伝子の役割についての理解は進んでいません。ヒトCLiPを開発できれば、肝細胞への遺伝子操作が容易になるため、ヒト正常肝臓から発がんに至るまでの過程を直接追跡することが可能となり、発がんメカニズムの解明につながることが期待されます。

論文情報
- 雑誌名:Cell Stem Cell
- タイトル:Conversion of terminally committed hepatocytes to culturable bipotent progenitor cells with regenerative capacity
- 著者:Takeshi Katsuda, Masaki Kawamata, Keitaro Hagiwara, Ryou-u Takahashi, Yusuke Yamamoto, Fernando D. Camargo and Takahiro Ochiya
研究費
国立研究開発法人日本医療研究開発機構(AMED)B型肝炎創薬実用化等研究事業
「HBVの感染初期過程を評価する系の開発とそれを用いた感染阻害低分子化合物およびレセプター探索」
プレスリリース
- 肝臓を再構築する肝前駆細胞へのリプログラミングにラット、マウスで成功 再生医療やがん治療への応用に期待
関連ファイルをご覧ください。
報道関係からのお問い合せ先
- 国立研究開発法人国立がん研究センター 企画戦略局 広報企画室
電話番号:03-3542-2511(代表)
ファクス番号:03-3542-2545
Eメール:ncc-admin●ncc.go.jp(●を@に置き換えください) - 国立研究開発法人日本医療研究開発機構(AMED) 戦略推進部感染症研究課
郵便番号:100-0004 東京都千代田区大手町1-7-1
電話番号:03-6870-2225
Eメール:hepatitis●amed.go.jp(●を@に置き換えください)
