科学的根拠に基づくわが国の大腸がん検診を提言「有効性評価に基づく大腸がん検診ガイドライン」2024年度版公開
2024年11月27日
国立研究開発法人国立がん研究センター
発表ポイント
- 「有効性評価に基づく大腸がん検診ガイドライン」2005年版公開後の新たな研究の科学的根拠を検証し、わが国で推奨する大腸がん検診ガイドラインとして提言をまとめました。
- 便潜血検査免疫法の推奨グレードはA、全大腸内視鏡検査の推奨グレードはCです。
- 便潜血検査免疫法を用いた検診の対象年齢と検診間隔、採便回数を新たに明示しました。
- 複数の研究結果を集約し、便潜血検査免疫法の統合感度と統合特異度を算出しました。現在国内外で使用されている便潜血検査免疫法の感度が以前より大幅に向上したことが明らかになりました。便潜血検査を定期的に受診し、陽性になった場合には必ず精密検査を受けることで、大腸がんによる死亡がさらに減少すると考えられます。
- 全大腸内視鏡検査は死亡率減少効果を示す科学的根拠はありますが、証拠の信頼性が低いことから、現状では対策型検診で実施しないことを推奨します。現在、国内外で全大腸内視鏡検査の有効性を評価するための無作為化比較対照試験が複数進行中のため、これらの研究結果が公表された段階で再評価を行います。
概要
国立研究開発法人国立がん研究センター(東京都中央区、理事長:中釜 斉)がん対策研究所検診研究部(部長:中山 富雄)の研究グループは、科学的根拠に基づくがん検診を推進するために、がん検診に関する国内外の研究を検証し、検診の利益と不利益を勘案した「有効性評価に基づく検診ガイドライン」として提言をまとめています。
これまで、大腸がん(2005年)、胃がん(2005年度、2014年度)、肺がん(2006年度)、前立腺がん(2008年度)、子宮頸がん(2009年度、2019年度)、乳がん(2013年度)の検診ガイドラインをまとめました。これらは厚生労働省における「がん検診のあり方検討会」において、対策型がん検診のあり方を検討するための資料として用いられています。
「有効性評価に基づく大腸がん検診ガイドライン」は、2005年版を公開後19年が経過しており、その間に報告された大腸がん検診に関する新たな研究の科学的根拠を明確にまとめることが求められていました。
国立がん研究センターがん対策研究所検診研究部は、2005年版公開後に報告された研究を検証し、わが国で実施すべき大腸がん検診方法を「有効性評価に基づく大腸がん検診ガイドライン」2024年度版としてまとめ11月27日に公開します。
背景
大腸がんについて
大腸がんは大腸(結腸・直腸)に発生するがんで、日本では1年間に約15万人から16万人が診断されています。大腸がんと診断される人は40歳代から増加しはじめ、年齢が高くなるほど大腸がんの罹患率が高くなります。死亡率も同じ傾向です。
日本では1992年より便潜血検査免疫法による大腸がん検診が公的に実施されています。しかし、検診受診率と精密検査受診率が低いため、大腸がん死亡率の減少は十分ではありません。
近年、全大腸内視鏡を検診において活用したいという要望が高まっており、大腸内視鏡検査の有効性を含めた科学的根拠を吟味し、課題を整理する必要性に迫られていました。また、現在検診で使用されている便潜血検査免疫法の実施方法に関する課題についても検討する必要があります。
研究成果「有効性評価に基づく大腸がん検診ガイドライン」2024年度版について
検討対象
1. 便潜血検査免疫法
便潜血検査は便中の血液を調べる検査です。便の表面を専用の器具で擦りとり、便中に含まれるヒトヘモグロビンを測定します。検査前の食事制限や薬剤制限は不要です。大腸がん検診として国際的に広く用いられています。
2. 全大腸内視鏡検査
全大腸内視鏡検査は肛門から内視鏡を挿入し、直腸から回盲部までを観察します。わが国では便潜血検査陽性者の精密検査として用いられており、検診としては人間ドックなどのオプション検査として導入されています。全大腸内視鏡検査は腸管内を直接観察でき、治療も実施できます。しかし、排便を促すための前処置として腸管洗浄剤や下剤を服用する必要があります。
更新版における大腸がん検診の推奨グレード注1
2024年度版では、便潜血検査免疫法(以下、免疫法)と全大腸内視鏡検査(以下、全大腸内視鏡)の利益(大腸がん死亡率減少効果)と不利益(偽陽性、過剰診断、全大腸内視鏡検査の偶発症、精神的負担)を比較して、有効性の検討を行いました。
1. 便潜血検査免疫法(推奨グレードA)
がん検診の利益となる死亡率減少効果について、免疫法は無作為化比較対照試験(RCT)で死亡率減少効果が証明されている便潜血検査化学法(免疫法の前に実施されていた検査法、免疫法よりも感度が低い)と同等以上の死亡率減少効果が期待できます。
また、1万人を対象に大腸がん検診を行ったと仮定した場合の大腸がん検出数は、免疫法は24名、化学法は14名でした(図1)。
がん検診の不利益はNumber Needed to Scope(以下、NNS)という偽陽性の指標を用いて検討しました。NNSは、免疫法による陽性者数を精密検査(全大腸内視鏡)で実際に大腸がんが発見された発見数で割った値です。大腸がん1例を発見するために必要な精密検査数であり、NNSが大きいほど不必要な精密検査数が多いことを意味します。その結果、免疫法でのNNSは13、化学法は11で大差はありませんでした(図1)。NNSの他にも免疫法の不利益はありますが、それらを総合しても利益が不利益を上回ると判断されるため、対策型検診・任意型検診注2としての実施を勧めます。
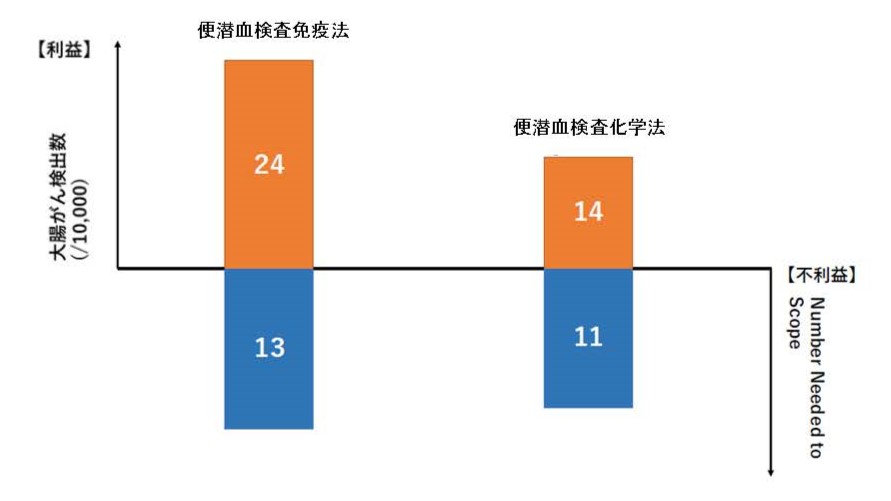
Number Needed to Scope : 大腸がん1例を発見するために必要な全大腸内視鏡検査数(精密検査数)
図1. 便潜血検査免疫法の利益と不利益の対比 出典:大腸がん検診エビデンスレポート2023年度版 p.366
2. 全大腸内視鏡検査(推奨グレードC)
がん検診の利益となる死亡率減少効果について、全大腸内視鏡の観察研究では大腸がん死亡率減少効果が示されていますが、検査目的が診療(有症状者などハイリスク者)なのか検診(平均リスク者)なのか明確に区別されていないという特徴があります。そのため証拠の信頼性は低いと判断されます。追加で実施した代替指標評価注3でも、参照基準としたS状結腸鏡検査(以下、S状結腸鏡)の検出率を上回ることができませんでした。代替指標評価では、研究参加者全員(検査の受診・非受診に関わらず)で解析を行いますが、大腸内視鏡検査の受診率が他の検査よりも低いことが効果を検出しにくい理由と考えられます。
また、1万人を対象に大腸がん検診行ったと仮定した場合の大腸がん検出数は、免疫法は14名、S状結腸鏡は16名、全大腸内視鏡は11名でした(図2)。
がん検診の不利益として各検査法のNNSは、免疫法20、S状結腸鏡17、全大腸内視鏡200でした(図2)。総合すると、全大腸内視鏡は死亡率減少効果を示すものの、証拠の信頼性は低く対策型検診では推奨されません。任意型検診においては利益と不利益に関する適切な情報を医療者と検診対象者が共有し、医療者は検診対象者の判断を支援する必要があります。
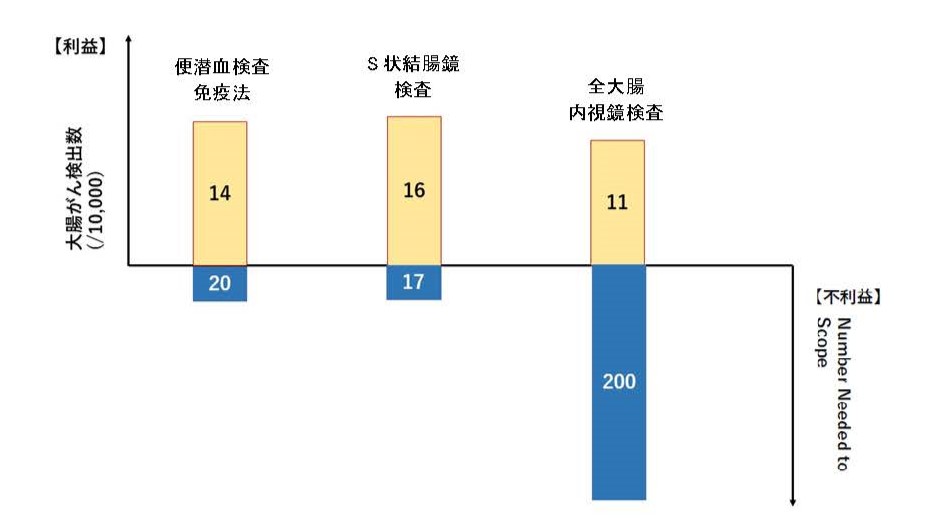
Number Needed to Scope : 大腸がん1例を発見するために必要な全大腸内視鏡検査数
図2. 全大腸内視鏡検査の利益と不利益の対比 出典:大腸がん検診エビデンスレポート2023年度版 p.368
2005年版からの主な変更点
1. 便潜血検査免疫法の感度と特異度
複数の研究結果をとりまとめ、免疫法の感度と特異度を計算しました。大腸がんを検出する感度(大腸がん患者が免疫法を受けて陽性となる確率)は84%、特異度(大腸がんでない人が免疫法を受けて陰性となる確率)は92%でした。2005年版当時の免疫法の感度55.6から92.9%(国内)、30から87%(国外)に比べて、現在国内外で使用されている免疫法の感度が大幅に向上したことが明らかになりました。
2. 便潜血検査免疫法による大腸がん検診の対象年齢、検診間隔、採便回数の明示
2005年版では明示していなかった検診対象年齢、検診間隔、採便回数を明示しました。
検診対象は40歳から74歳を推奨しますが、45歳または50歳開始も許容されます。40歳以上を対象に大腸がん検診が実施されているにもかかわらず、40代と50代の大腸がん罹患率は国際的に高いレベルにあることを重視して決定しました。ただし、若年者ほど検診の不利益であるNNSが大きく、他国の検診開始年齢は50歳が多いことから、45歳または50歳開始も許容されました。他方、終了年齢に関しては、対策型検診では様々なレベルの身体機能を持つ高齢者が受診するため、精密検査や治療に伴う偶発症や合併症を考慮して74歳で検診を終了することが妥当であると判断されました。
検診間隔を1年から2年にすることも可能です。
採便回数も1回法でも2回法どちらでも可能です。
展望
大腸がんの対策型検診として免疫法を引き続き推奨します。ただし、免疫法のカットオフ値(検査陽性と判定する便中ヒトヘモグロビン値)の設定など運用に関する課題や郵送法は今後の検討課題です。
全大腸内視鏡に対する今回の評価はあくまで健常者を対象としたスクリーニング検査としての評価であり、便潜血検査陽性者への精密検査や内視鏡治療における重要性に関しては、決して揺るがないものです。全大腸内視鏡による検診の死亡率減少効果を調べる無作為化比較対照試験が国内外で進行中です。それらの結果が公表された後に再評価を行います。
研究費
国立がん研究センター研究開発費
研究課題名:検診ガイドライン作成と検診の効率的運用方法の体制に関する研究
研究期間:2020年度から2022年度
研究代表者名:中山 富雄
研究課題名:科学的根拠が不十分ながん検診手法の低減を目指したガイドライン作成とわかりやすい情報提供に関する研究
研究期間:2023年度から2025年度
研究代表者名:中山 富雄
用語説明
注1:推奨グレードについて
推奨グレードは、対策型検診と任意型検診における実施の可否を示しています。推奨グレードは、各種がん検診の利益と不利益のバランスを考慮して決定します。がん検診の主たる利益は死亡率減少効果です。一方、不利益とは、偽陰性率、偽陽性率、過剰診断、偶発症、放射線被曝、感染、受診者の心理的・身体的負担などがあります。推奨グレードの決定においては、証拠の信頼性や不利益の程度も重要です。
また、推奨グレードは、「子宮頸がん検診ガイドライン」2019年度版から2点の大きな変更があります。1)推奨Cが「条件付き推奨」から対策型検診では「実施を推奨しない」、任意型検診では「利益と不利益に関する適切な情報を提供し個人の判断に委ねる」へ変更、2)推奨グレードの判断に、医療資源(費用を含む)や受診者の価値観や選好性を含めないことにしました。
注2:対策型検診と任意型検診
対策型検診とは、集団全体の死亡率減少を目的として実施するものを指し、公共的な予防対策として行われます。そのため、有効性が確立したがん検診を選択し、利益は不利益を上回ることが基本条件になります。わが国では、対策型検診として市区町村が行う住民検診が該当します。
一方、任意型検診とは、対策型検診以外の検診が該当しますが、その方法・提供体制は様々です。典型的な例は、医療機関や検診機関が行う人間ドックが該当しますが、保険者による予防給付や個人による受診選択など受診形態も様々です。検診方法の選択、精度管理などの問題がありますが、個々の受診者への対応が可能になるという利点もあります。
注3:代替指標評価
これまで実施されてきた標準的ながん検診の有効性評価では、死亡率減少効果を直接評価した研究を根拠に推奨グレードを決定します。無作為化比較対照試験の最終データが使用できない場合は次善の方法として観察研究や代替指標による評価を行います。
本ガイドラインでは観察研究による有効性評価を行いましたが、様々なバイアスの影響で確定的な結論が出せませんでした。そこで、世界内視鏡学会(WEO)の提唱する代替指標評価が実施されました。死亡率減少効果があると証明された検診手法と類似した検診手法に対して、テスト精度・プログラム評価に基づく証拠を積み重ね、その検診手法の有効性を検討する評価方法です。
無作為化比較対照試験は新しい検査手法による死亡率減少効果を直接確認できる信頼性の最も高い研究デザインです。一方、代替指標評価は死亡率減少効果を推測する方法のため、無作為化比較対照試験による証拠の信頼性を上回ることはありません。
お問い合わせ先
研究に関するお問い合わせ
国立研究開発法人国立がん研究センター
がん対策研究所 検診研究部 検診評価研究室
室長 細野 覚代
電話番号:03-3542-2511(代表)
E-mail:shosono●ncc.go.jp
広報窓口
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室
電話番号:03-3542-2511(代表)
E-mail:ncc-admin●ncc.go.jp
