消化器がんのがんゲノム医療のさらなる発展
リキッドバイオプシーによるゲノム解析の有用性を証明へ
2020年10月6日
国立研究開発法人国立がん研究センター
国立研究開発法人日本医療研究開発機構
in English
発表のポイント
- 消化器がんにおいて、患者さんの血液を用いてがんのゲノム異常を検出する検査(リキッドバイオプシー)を治験のスクリーニングに取り入れた結果、従来の腫瘍組織検査に比べてより迅速に検査結果が返却され、より多くの患者さんが治験に登録されたことを世界で初めて示しました。
- 治験のスクリーニング検査*1として、腫瘍組織検査とリキッドバイオプシーの有用性を大規模に比較した研究はこれまでありませんでした。
- リキッドバイオプシーがスクリーニング検査としてより多くの治験に活用されることで、より多くの患者さんに最善の医療を提供できることが期待されます。
概要
国立研究開発法人国立がん研究センター(理事長:中釜 斉、東京都中央区)東病院(病院長:大津 敦、千葉県柏市)は、消化器がんにおいて、患者さんの血液を用いてがんのゲノム異常を検出する検査(リキッドバイオプシー)を治験のスクリーニングに取り入れた結果、従来の腫瘍組織検査に比べてより迅速に検査結果が返却され、より多くの患者さんが治験に登録されたことを世界で初めて示しました。
リキッドバイオプシーでは、がん組織を採取せずに、採血で繰り返し測定することが可能です。従来の腫瘍組織の採取は患者さんへの侵襲が大きく、治療決定の遅れにも繋がることがありましたが、今回、リキッドバイオプシーの有用性が証明されたことにより、身体に負担の少ない方法で、より多くの患者さんが最適な治療薬にたどり着くことに繋がることが期待されます。
本研究では、進行消化器がんの患者さんを対象にした腫瘍組織を用いたがんゲノムスクリーニングプロジェクト「GI-SCREEN-Japan(腫瘍組織検査)」と、リキッドバイオプシー研究「GOZILA Study(リキッドバイオプシー)」のゲノム解析結果において結果判明までの期間や適合する治験への登録割合及びその効果を比較しました。その結果、リキッドバイオプシーが腫瘍組織検査と比べ、約22日早く解析結果が判明し、さらにゲノム解析結果に基づき、対応する治療薬の治験に登録した患者さんの割合が高まることが明らかになりました。
なお、本研究は国立がん研究センター東病院 消化管内科長の吉野孝之、同院 トランスレーショナルリサーチ支援室・消化管内科医員の中村能章らがGI-SCREEN-JapanおよびGOZILA Studyを通じて行ったもので、本研究成果は米国科学雑誌「Nature Medicine」オンライン版(2020年10月5日付:日本時間10月6日)に掲載されます。
背景
がんゲノム医療*2の実現のため、がんのゲノム異常に基づいて治療薬の効果を検証する治験が世界中で行われています。これらの治験では、患者さんのがんゲノム異常を同定するため、腫瘍組織の解析が従来用いられてきました。しかし、必ずしも腫瘍組織が採取できない患者さんがいることや、腫瘍組織の解析に時間を要することなどが、これらの治験促進の大きな障壁となっていました。
一方、近年、リキッドバイオプシーの技術が目覚ましい進歩を遂げています。リキッドバイオプシーは腫瘍組織を採取できない患者さんでも、ゲノム異常を解析することができ、検査結果の返却も早いことから、従来の腫瘍組織検査がもつ課題を克服する可能性が示唆されてきました。しかし、消化器がんにおいて治験のスクリーニング検査として、腫瘍組織検査とリキッドバイオプシーの有用性を大規模に比較した研究はこれまでありませんでした。
そこで今回国立がん研究センター東病院では、産学連携全国がんゲノムスクリーニング事業「SCRUM-Japan(スクラム・ジャパン)」*3の基盤を活用し、世界に類を見ない大規模な比較研究を実施しました。
研究方法と成果
国立がん研究センターでは、産学連携全国がんゲノムスクリーニング事業「SCRUM-Japan(スクラム・ジャパン)」を立ち上げ、2014年2月より「GI-SCREEN-Japan(現:MONSTAR-SCREEN)」に取り組んできました。GI-SCREEN-Japanは、国内の主要ながん専門病院や大学病院と協働して、進行消化器がんの患者さんの腫瘍組織を遺伝子パネル検査(Oncomine Comprehensive Assay)で解析し、治療薬を届ける全国がんゲノムスクリーニングプロジェクトです。さらに2018年1月より、GI-SCREEN-Japanの基盤を活用し、進行消化器がんの患者さんの血液をリキッドバイオプシー(Guardant360®、Guardant AMEA Inc.)で解析するスクリーニングプロジェクト「GOZILA Study」を、米国Guardant Health社との共同研究として開始しました。
本研究では、2015年2月から2019年4月まで(4年2ヶ月)にGI-SCREEN-Japan(腫瘍組織検査)に登録された5743例と、2018年1月から2019年8月まで(1年7ヶ月)にGOZILA Study(リキッドバイオプシー)に登録された1787例を比較しました(図1)。
図1 研究の概要
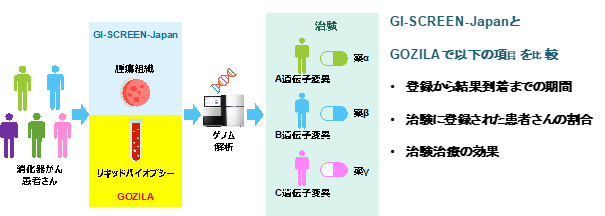
◆比較結果(GI-SCREEN-Japan vs. GOZILA Study)(図2)
- プロジェクト登録後~検体到着までの期間(中央値:14日 vs. 4日、P<0.0001)
- 検体到着後から解析結果が患者さんに返却されるまでの期間(中央値:19日 vs. 7日、P<0.0001)
- 治療標的となるゲノム異常が同定された患者さんの割合(54% vs. 57%)
- ゲノム異常に適合した薬剤の治験に登録された患者さんの割合(4.1% vs. 9.5%、P<0.0001)
- 治験治療で腫瘍が縮小した患者さんの割合(16.7% vs. 20.0%、P=0.69)
- 治験治療で病気が悪くなるまでの期間(中央値:2.8か月 vs. 2.4か月、P=0.70)
図2 GI-SCREEN-Japan(腫瘍組織検査)とGOZILA Study(リキッドバイオプシー)との比較結果
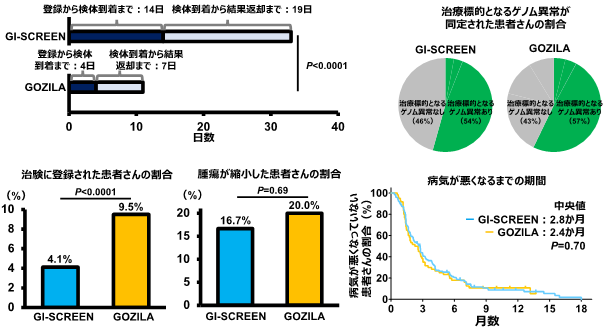
さらに、GOZILA Studyのリキッドバイオプシーで同定されたゲノム異常のプロファイリング*4の結果、有用なバイオマーカーや治療標的として将来的な臨床開発に繋がる可能性のある新たなドライバー遺伝子*5異常(食道扁平上皮がんのNFE2L2変異や膵がんのGNAS変異、胆道癌のCTNNB1変異など)が複数見出されました(図3)。
図3 GOZILA Studyにおけるがんゲノム異常のプロファイリング
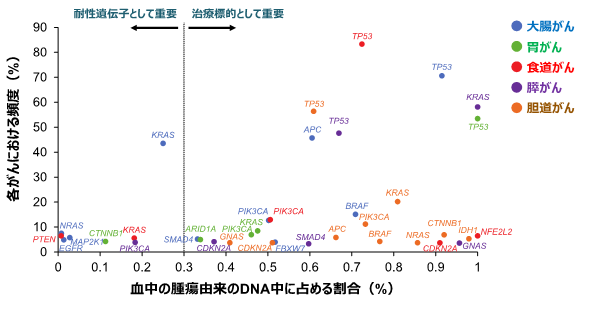
展望
本研究の成果により、リキッドバイオプシーがスクリーニング検査としてより多くの治験に活用されることで、より多くの患者さんに最善の医療を提供できることが期待されます。また、新たなドライバー遺伝子異常の発見により、これまで着手されていなかったドライバー遺伝子異常に対する治療開発が活発化する可能性があります。なおGOZILA Studyでは、既にリキッドバイオプシーの結果に基づく医師主導治験が複数実施されています。今後も国立がん研究センター東病院は、一人でも多くの患者さんが最善の治療を受けられるよう、リキッドバイオプシーによるがんゲノム医療の実現を目指してまいります。
発表論文
雑誌名
Nature Medicine
タイトル
Clinical Utility of Circulating Tumor DNA Sequencing in Advanced Gastrointestinal Cancer: SCRUM-Japan GI-SCREEN and GOZILA Studies
著者
Yoshiaki Nakamura1,2,33, Hiroya Taniguchi1,2,33, Masafumi Ikeda3, Hideaki Bando4, Ken Kato5,6, Chigusa Morizane7, Taito Esaki8, Yoshito Komatsu9, Yasuyuki Kawamoto9, Naoki Takahashi10, Makoto Ueno11, Yoshinori Kagawa12, Tomohiro Nishina13, Takeshi Kato14, Yoshiyuki Yamamoto15, Junji Furuse16, Tadamichi Denda17, Hisato Kawakami18, Eiji Oki19, Takako Nakajima20, Naohiro Nishida21, Kensei Yamaguchi22, Hisateru Yasui23, Masahiro Goto24, Nobuhisa Matsuhashi25, Koushiro Ohtsubo26, Kentaro Yamazaki27, Akihito Tsuji28, Wataru Okamoto2,29, Katsuya Tsuchihara2,30, Takeharu Yamanaka31, Izumi Miki2, Yasutoshi Sakamoto2, Hiroko Ichiki2, Masayuki Hata2, Riu Yamashita30, Atsushi Ohtsu1, Justin I. Odegaard32, Takayuki Yoshino1*
所属
- Department of Gastroenterology and Gastrointestinal Oncology, National Cancer Center Hospital East, Kashiwa, Japan
- Translational Research Support Section, National Cancer Center Hospital East, Kashiwa, Japan
- Department of Hepatobiliary and Pancreatic Oncology, National Cancer Center Hospital East, Kashiwa, Japan
- Department of Clinical Oncology, Aichi Cancer Center Hospital, Nagoya, Japan
- Department of Gastrointestinal Oncology, National Cancer Center Hospital, Tokyo, Japan
- Biobank Translational Research Support Section, National Cancer Center Hospital, Tokyo, Japan
- Department of Hepatobiliary and Pancreatic Oncology, National Cancer Center Hospital, Tokyo, Japan
- Department of Gastrointestinal and Medical Oncology, National Hospital Organization Kyushu Cancer Center, Fukuoka, Japan
- Department of Cancer Center, Hokkaido University Hospital, Sapporo, Japan
- Department of Gastroenterology, Saitama Cancer Center, Kitaadachi-gun, Japan
- Department of Gastroenterology, Hepatobiliary and Pancreatic Medical Oncology Division, Kanagawa Cancer Center, Yokohama, Japan
- Department of Colorectal Surgery, Kansai Rosai Hospital, Amagasaki, Japan
- Department of Gastrointestinal Medical Oncology, National Hospital Organization Shikoku Cancer Center, Matsuyama, Japan
- Department of Surgery, National Hospital Organization Osaka National Hospital, Osaka, Japan
- Department of Gastroenterology and Hepatology, University of Tsukuba Hospital, Tsukuba, Japan
- Department of Medical Oncology, Kyorin University Hospital, Mitaka, Japan
- Division of Gastroenterology, Chiba Cancer Center, Chiba, Japan
- Department of Medical Oncology, Kindai University Hospital, Osakasayama, Japan
- Department of Surgery and Science, Graduate School of Medical Sciences, Kyushu University, Fukuoka, Japan
- Department of Medical Oncology, St. Marianna University School of Medicine, Kawasaki, Japan
- Department of Frontier Science for Cancer and Chemotherapy, Graduate School of Medicine, Osaka University, Suita, Japan
- Department of Gastroenterological Chemotherapy, Cancer Institute Hospital of Japanese Foundation for Cancer Research, Tokyo, Japan
- Department of Medical Oncology, Kobe City Medical Center General Hospital, Kobe, Japan
- Cancer Chemotherapy Center, Osaka Medical College Hospital, Takatsuki, Japan
- Department of Surgical Oncology, Graduate School of Medicine, Gifu University, Gifu, Japan
- Division of Medical Oncology, Cancer Research Institute, Kanazawa University, Kanazawa, Japan
- Division of Gastrointestinal Oncology, Shizuoka Cancer Center, Shunto-gun, Japan
- Department of Clinical Oncology, Kagawa University Hospital, Kita-gun, Japan
- Cancer Treatment Center, Hiroshima University Hospital, Hiroshima, Japan
- Division of Translational Informatics, Exploratory Oncology Research and Clinical Trial Center, National Cancer Center, Kashiwa, Japan
- Division of Biostatistics, National Cancer Center Hospital East, Kashiwa, Japan
- Guardant Health, Redwood City, CA
- These authors contributed equally: Yoshiaki Nakamura and Hiroya Taniguchi
DOI
10.1038/s41591-020-1063-5
掲載日
2020年10月5日付(米国時間)
研究費
本研究は下記事業の支援を受けて行われました。
- SCRUM-Japan参加企業による資金
- 国立研究開発法人日本医療研究開発機構(AMED) 革新的がん医療実用化研究事業
「血液循環腫瘍DNA解析を活用した切除不能・進行再発大腸がんにおけるがんゲノム異常のClonal Evolutionに関する網羅的カタログの作成」(研究代表者:中村 能章) - 国立がん研究センター研究開発費「新たな解析技術を組み入れた国際的遺伝子スクリーニング基盤の構築と臨床開発に関する研究(31-A-5)」(研究代表者:大津 敦)
用語解説
*1 スクリーニング検査
治験におけるスクリーニング検査では、患者さんの状態が治験に参加できる条件を満たしているか確認する検査や聞き取り調査を行う。主に、身長、体重、体温、血圧、採血、呼吸器検査、心電図、CTスキャン、問診など。
*2 がんゲノム医療
多数の遺伝子を同時に調べ、がんのゲノム異常を明らかにすることにより、一人一人の体質や病状に合わせて治療などを行う医療。
*3 SCRUM-Japan(Cancer Genome Screening Project for Individualized Medicine in Japan)
2013年に開始した肺がん患者さんを対象としたLC-SCRUM-Japan(現:LC-SCRUM-Asia)と、2014年に開始した消化器がん患者さんを対象としたGI-SCREEN-Japan(現:MONSTAR-SCREEN)が統合した、産学連携がんゲノムスクリーニングプロジェクト。固形がん患者さんを対象に、がんの遺伝子異常を調べるプロジェクトであり、2015年2月の設立以降、約1万例を超える進行固形がん患者さんが研究に参加。本プロジェクトの成果として、すでに8つの新薬と9つの体外診断薬の薬事承認を取得している。全国から200を超える医療機関と17社の製薬企業や検査会社が参画し、アカデミアと臨床現場、産業界が一体となって、日本のがん患者さんの遺伝子異常に合った治療薬や診断薬の開発を行っている。
参考:
- SCRUM-Japan
- プレスリリース「産学連携全国がんゲノムスクリーニング「SCRUM-Japan」第三期プロジェクトを開始」
- プレスリリース「SCRUM-Japan GI-SCREEN、73種の遺伝子異常を血液で解析 リキッドバイオプシーを用いた個別化医療の実現を目指す」
*4 プロファイリング
がんの組織を用いて、1回の検査でがんに関連する多数の遺伝子を同時に調べる検査。
*5 ドライバー遺伝子
がん遺伝子・がん抑制遺伝子といった、がんの発生・進展において直接的に重要な役割を果たす遺伝子。
問い合わせ先
取材・報道関係からのお問い合わせ
国立研究開発法人国立がん研究センター 企画戦略局 広報企画室(柏キャンパス)
電話番号:04-7133-1111(代表) FAX:04-7130-0195
Eメール:ncc-admin@ncc.go.jp
AMED事業に関するお問い合わせ
国立研究開発法人日本医療研究開発機構(AMED)
疾患基礎研究事業部 疾患基礎研究課 革新的がん医療実用化研究事業事務局
電話番号:03-6870-2286 Eメール:cancer@amed.go.jp
