がん遺伝子パネル検査の実臨床における有用性を解明―標的治療の実態と効果、患者さんの予後改善が明らかに―
2026年1月8日
国立研究開発法人国立がん研究センター
慶應義塾大学医学部
発表のポイント
- C-CATに登録された50,000例以上の臨床ゲノムデータを用いて、遺伝子異常を標的とした治療(標的治療)の実態や効果、患者予後などを解析することで、がん遺伝子パネル検査の実臨床における有用性を明らかにしました。
- 国内承認済みの薬剤だけでなく、国内未承認でも有効性が示されている薬剤の標的となる遺伝子異常が検出された場合に、患者予後が改善することを示しました。この結果は、治験や患者申出療養制度などを通じた未承認薬・適応外薬の使用が患者予後を改善する可能性を示唆しています。
- がん遺伝子パネル検査に基づいて、標的治療を新たに受けた患者さんの割合は、全体では8.0%にとどまっていましたが、その割合ががん種ごとに大きく異なり、甲状腺がん(34.8%)・非小細胞肺がん(20.3%)・小細胞肺がん(20.1%)では高いという結果でした。また、経時的な解析によって、その割合が増加傾向にあることが分かりました。
- 大規模データを利活用することにより、(1)腫瘍遺伝子変異量が高い症例には一般に免疫チェックポイント阻害薬が有効ですが、その有効性はがん種ごとに異なり、乳房外パジェット病では有効性が低いことや、(2)コンパニオン診断薬が陰性例においても、がん遺伝子パネル検査で陽性の場合には、標的治療が有効な症例が頻繁に存在するといった新たな知見も示されました。
概要
国立研究開発法人国立がん研究センター(理事長:間野 博行、東京都中央区)研究所の斎藤 優樹 研究員(分子腫瘍学分野)、片岡 圭亮 分野長(分子腫瘍学分野/慶應義塾大学医学部内科学教室(血液) 教授)らの研究グループは、慶應義塾大学医学部の平田 賢郎 専任講師(腫瘍センター)・舩越 建 准教授(皮膚科学教室)らと共同で、国立がん研究センターがんゲノム情報管理センター注1(Center for Cancer Genomics and Advanced Therapeutics:C-CAT)に蓄積された、固形がん注2症例を対象に、保険診療の一環としてがん遺伝子パネル検査注3が実施された54,185症例の臨床ゲノムデータを解析しました。その結果、遺伝子異常注4を標的とした治療(標的治療注5)の実施割合や患者予後注6との関連など、がん遺伝子パネル検査の実臨床における有用性を明らかにしました。本研究結果は2026年1月6日に英科学誌「Nature Medicine」に掲載されました。
今回の研究の主な成果は以下の点です。
- がん遺伝子パネル検査において、国内承認薬の標的となる遺伝子異常だけではなく、国内では未承認であっても有効性が示されている薬剤の標的となる遺伝子異常が検出された場合にも、患者予後が改善することを明らかにしました。この結果は、治験注7や患者申出療養制度注8などを通じた未承認薬・適応外薬の使用が患者予後を改善する可能性を示唆しています。
- 治療標的となる遺伝子異常注9は72.7%の患者さんに認められましたが、がん遺伝子パネル検査結果に基づいて実際にこの遺伝子異常を標的とした治療を受けた患者さんは8.0%にとどまりました。がん種別にみると、甲状腺がん(34.8%)・非小細胞肺がん(20.3%)・小細胞肺がん(20.1%)などでは高いものの、膵がん(1.3%)・肝臓がん(1.8%)などでは低く、がん種による差が大きいことが分かりました。また、検査実施時期別では、2019~2020年の5.5%から2023~2024年には10.0%へと上昇しており、実際に標的治療を受けられる患者さんの割合が近年増加していることが明らかになりました。
- 多数例からなる大規模データベースを活用することで、これまで十分な医学的根拠(エビデンス)が得られていなかった課題に新たな示唆を与えました。例えば、腫瘍遺伝子変異量が高い(TMB-high)注10症例に対してペムブロリズマブという免疫チェックポイント阻害薬が有効とされています。しかし、この有効性はがん種ごとに異なり、「乳房外パジェット病注11」という希少がんでは有効性が低いことが示されました。また、標的治療における適応の判断にはコンパニオン診断薬注12が使用されますが、コンパニオン診断薬で陰性であっても、がん遺伝子パネル検査で陽性の場合に、標的治療が有効な場合が頻繁に存在することが明らかになりました。
本成果は、日本で保険診療として実施されたがん遺伝子パネル検査データと臨床データの網羅的解析により、がん遺伝子パネル検査の実臨床における有用性や、がんゲノム医療注13の現状を明らかにしたものです。
背景
近年、がんゲノム研究の進歩に伴い、発がんを促進する遺伝子異常が多数同定されました。また、個別の遺伝子異常を標的とした薬剤(分子標的薬)の開発が進み、遺伝子異常に基づいて患者さんごとに適切な薬剤を投与することが可能になってきました。これらの薬剤は、特定のがん種を対象にしたもの(例:EGFR変異を有する肺がんに対するEGFR阻害薬)が主ですが、近年はがん種横断的に承認された薬剤(例:高い腫瘍遺伝子変異量(TMB-high)に対するペムブロリズマブ)も増加しています。
従来、がんの遺伝子異常は一つ一つの遺伝子を順番に調べる必要がありましたが、近年は100種類以上の遺伝子を同時に調べる「がん遺伝子パネル検査」を行うことが可能になりました。
これまでの様々な研究において、がん遺伝子パネル検査を行うと、様々な治療標的となる遺伝子異常を検出できることが報告されてきました(参考「日本人のがんゲノム異常の全体像を解明」2024年2月29日プレスリリース)。しかし、承認薬の場合はコンパニオン診断薬に基づいて投与される場合も多いこと、未承認薬・適応外薬の場合は患者さんの薬剤へのアクセスが限定されていることから、治療標的となる遺伝子異常が検出されることが、実際に遺伝子異常を標的とした治療(標的治療)の実施に繋がるかは従来明らかではありませんでした。また、個々の標的治療の承認薬を使用することが、対象となる標的遺伝子異常を有する患者さんの予後を改善することは知られているものの、がん遺伝子パネル検査に基づいて未承認薬を使用することが患者予後を改善するかは明らかではありませんでした。
日本では2019年6月より、標準治療が終了となった固形がんの患者さん、または局所進行または転移が認められ標準治療が終了となった固形がんの患者さんを対象に、「がん遺伝子パネル検査」が保険適用されています。がん遺伝子パネル検査によって検出された遺伝子異常(ゲノムデータ)や、その後の標的治療や患者予後などの情報(臨床データ)は、患者さんの同意のもとC-CATに集約・保管されています。本研究では、このデータを利活用し、標的治療の実態や効果、患者予後などを解析することで、がん遺伝子パネル検査の実臨床における有用性を調べました。
研究成果(方法・結果)
1.国内未承認薬の標的となる遺伝子異常が検出された場合にも、患者予後が改善する
研究グループは、C-CATに登録された54,185人のデータを解析しました。対象としたのは、2019年6月から2024年6月の間に日本において固形がんに対して保険診療でがん遺伝子パネル検査(FoundationOne® CDx がんゲノムプロファイル)を実施した患者さんです。
このうち、11.2%の患者さんでは、国内承認薬の標的となる遺伝子異常(治療エビデンスレベル注9A[国内承認薬あり])が検出されました。また、5.4%の患者さんでは、国内では未承認であるものの、米国で承認薬がある、またはガイドラインに記載されている薬剤の標的となる遺伝子異常(治療エビデンスレベルA[国内承認薬なし])が検出されました。さらに、8.1%の患者さんでは、信憑性の高い臨床試験と専門家間の合意によって有効性が示されている薬剤の標的となる遺伝子異常(治療エビデンスレベルB)が検出されました。さらに、治療エビデンスレベルC・Dの遺伝子異常はそれぞれ47.4%、0.6%に認められました(図1左上・右上)。
これらの治療エビデンスレベルごとの患者予後を比較したところ、エビデンスレベルA(国内承認薬あり)の患者さんが最も良好な予後を示し、次いでエビデンスレベルA(国内承認薬なし)、エビデンスレベルBの順でした。エビデンスレベルC~Eの患者さんは予後が最も不良でした(図1下)。この傾向は、全てのがん種をまとめた解析結果(図1下)だけでなく、個々のがん種ごとの解析でも概ね同様でした。
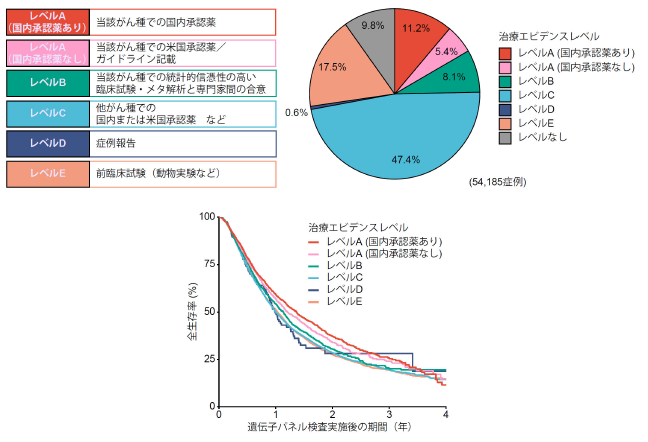
(右上)全体における治療エビデンスレベルの割合
(下)治療エビデンスレベルごとの患者予後を示す生存曲線
このことから、国内承認薬の標的となる遺伝子異常(治療エビデンスレベルA[国内承認薬あり])だけではなく、国内未承認でも有効性が示されている薬剤の標的となる遺伝子異常(治療エビデンスレベルA[国内承認薬なし]と治療エビデンスレベルB)が検出された場合にも、患者予後が改善することを明らかになりました。
2.標的治療が新たに導入される患者さんは全体で8.0%―がん種ごとに差があり、近年は増加傾向
次に、研究グループは、がん遺伝子パネル検査を行った症例のうち、検査で検出された遺伝子異常を標的とする治療が新たに導入された割合を調べました。具体的には、
- 治療エビデンスレベルA(国内承認薬あり)の遺伝子異常が検出され、検査後にはじめてその承認薬が保険診療で使用された患者さん
- 治療エビデンスレベルA(国内承認薬なし)またはB~Dの遺伝子異常が検出され、治験や患者申出療養制度などを通じて対応する未承認薬・適応外薬が使用された患者さん
の割合を算出しました。
その結果、臨床的に治療標的となる遺伝子異常(治療エビデンスレベルA~D)が検出された症例は全体の72.7%にのぼる一方、実際に標的治療を新たに受けた患者さんの割合は8.0%にとどまることが分かりました。
がん種別にみると、甲状腺がん(34.8%)・非小細胞肺がん(20.3%)・小細胞肺がん(20.1%)では割合が高い一方、膵がん(1.3%)・肝臓がん(1.8%)・消化管間質腫瘍(2.7%)では低く、がん種ごとに標的治療導入率に大きな差があることが分かりました(図2)。
さらに、検査実施時期で比較すると、2019~2020年では5.5%、2021~2022年では7.3%、2023~2024年では10.0%と近年増加していました(図3)。これは、この数年間で新規の標的治療薬の開発・承認が進み、がん遺伝子パネル検査に基づいた治療選択肢が増えていることを反映しています。
以上のように、がん遺伝子パネル検査結果に基づく標的治療導入率はがん種ごとに大きく異なり、現時点では限定的であるものの、近年増加していることが明らかになりました。
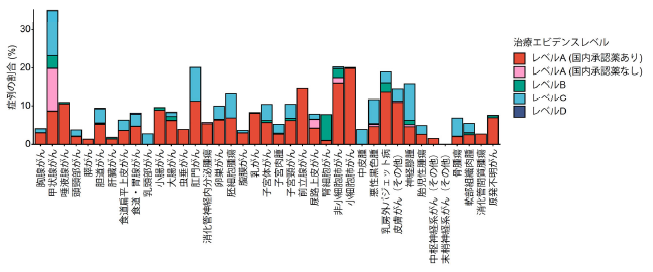
図2:がん遺伝子パネル検査に基づいて標的治療が導入された割合(がん種別)
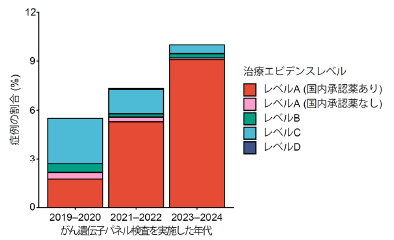
図3:がん遺伝子パネル検査に基づいて標的治療が導入された割合(検査実施時期別;全がん種)
3.医学的根拠が不足していた課題に対する様々な新知見:がんゲノム医療に有益な情報を明らかに
最後に、研究グループは、多数例からなる大規模データベースを活用し、がん遺伝子パネル検査を受けた患者さんの生命予後や標的治療の奏効を詳細に解析することで、これまで十分な医学的根拠(エビデンス)が得られていなかった課題に対する新たな知見を明らかにしました。主な知見は以下の通りです。
- がん遺伝子パネル検査において高い腫瘍遺伝子変異量(TMB-high)が検出されると、免疫チェックポイント阻害薬であるペムブロリズマブが有効であることが知られており、固形がん全般に承認されています。しかし、従来は多数例のデータが不足していたため、がん種ごとの有効性の違いは十分に明らかではありませんでした。そこでがん種ごとの有効性の違いを調べたところ、膵がんや胆道がんなど多くのがん種においてTMB-high症例に対するペムブロリズマブは有効であった一方で、例外的に「乳房外パジェット病」という希少がんでは有効性が低いことが明らかになりました。
- 現在TMB-highは腫瘍遺伝子変異量10 変異/Mb以上という基準が使用されています。本研究において、腫瘍遺伝子変異量20 変異/Mb以上の患者さんではペムブロリズマブの奏効率が高く、生命予後の大幅な改善が認められました。一方で、10~20 変異/Mbでは奏効率が低く、予後改善がほとんど認められませんでした。この傾向は、高頻度マイクロサテライト不安定性(MSI-high)注14の有無に関わらず共通していました。
- NTRK融合遺伝子注15が検出されると、TRK阻害薬(エヌトレクチニブなど)が有効であると知られており、固形がん全般に承認されています。このうち、最も多いタイプの融合遺伝子であるETV6::NTRK3は、他のNTRK融合遺伝子に比べてTRK阻害薬の有効性が高く、生命予後が良い傾向が認められました。
- 既存のコンパニオン診断薬で遺伝子異常が検出されず、がん遺伝子パネル検査ではじめて遺伝子異常が検出された患者さんに対して、標的治療が有効な場合が頻繁に存在することが明らかになりました。例えば、コンパニオン診断薬でEGFR遺伝子変異陰性であった(=検出されなかった)肺がん症例でも、がん遺伝子パネル検査でEGFR遺伝子変異陽性と判明し、EGFR阻害薬(オシメルチニブなど)が奏功した症例などが複数確認されました。
これらの知見は、これまで十分な医学的根拠がなかった領域に対する貴重なデータであり、臨床現場での治療選択において有用な情報と考えられます。
展望
研究グループは、日本で保険診療としてがん遺伝子パネル検査を実施された約50,000例の臨床ゲノムデータを解析することで、がん遺伝子パネル検査の実臨床における有用性を様々な角度から明らかにしました。本研究により、国内で未承認の薬剤であっても有効性が示されている薬剤の標的となる遺伝子異常が検出された場合に、患者予後が改善することが明らかになりました。また、現時点では遺伝子異常を標的とした治療(標的治療)導入率は低いもののその割合は近年増加していることを明らかにし、がん遺伝子パネル検査の有用性やがんゲノム医療の現状を示しました。さらに、多数例を解析することで、症例数の問題からこれまで十分な医学的根拠(エビデンス)が得られていなかった課題に対する新たな知見を明らかにしました。
研究グループは、今後も大規模な臨床ゲノムデータを用いたがんゲノム解析研究を継続し、固形がんだけではなく血液がんにおけるがん遺伝子パネル検査の有用性や、がん組織を用いず採血検体を用いるがん遺伝子パネル検査(リキッド・バイオプシー)の有用性なども明らかにしていく予定です。
謝辞
C-CATへのデータ利活用にご同意いただいた患者さん、データをご登録いただいた医療関係者の皆様、C-CATスタッフに心から感謝申し上げます。
発表論文
雑誌名
Nature Medicine
タイトル
Real-world clinical utility of comprehensive genomic profiling in advanced solid tumors
著者
斎藤優樹、堀江沙良、木暮泰寛、水野洸太、伊藤勇太、水上耀介、金夏倫、田村全、古屋淳史、舩越建、平田賢郎、片岡圭亮
DOI
10.1038/s41591-025-04086-8
掲載日
2026 年1 月6 日
URL
https://www.nature.com/articles/s41591-025-04086-8(外部サイトにリンクします)
研究費
- 日本医療研究開発機構(AMED) 次世代がん医療加速化研究事業
「患者間・腫瘍間・腫瘍内における遺伝学的・免疫学的不均一性の統合的理解」 (JP22ama221510)
「全がんctDNA解析による腫瘍不均一性と治療抵抗性機構の解明」(JP25ama221543) - 日本医療研究開発機構(AMED) 革新的先端研究開発支援事業(CREST)
「時空間マルチサンプリング検体の単一細胞解析によるヒト免疫療法の基盤となる免疫記憶の解明」(JP25gm1810002h0004) - 国立研究開発法人科学技術振興機構(JST) ムーンショット型研究開発事業
「生体内ネットワークの理解による難治性がん克服に向けた挑戦」 (JPMJMS2022) - 上原記念生命科学財団 第11回 特定研究助成金
「マルチオミクスデータ解析による新規発がん機構の解明」 - JSPS 科研費 腫瘍学およびその関連分野
「本邦がんゲノムリアルワールドデータを用いたがんの人種・地域間差の解明」 (JP 22K20808)
「リキッド・バイオプシーと変異体スクリーニングによる抗がん剤抵抗性変異の網羅的同定」(JP25K18889) - 武田科学振興財団 がん領域(基礎)
「がん種横断的マルチコホート解析による遺伝子間相互作用の包括的解明」 - JCA-KFCR 若手研究助成
「本邦大規模がん遺伝子パネル検査データを用いたリキッド・バイオプシーの特徴および薬剤到達率・薬剤耐性変異の解明」
用語解説
注1 がんゲノム情報管理センター(C-CAT)
日本において保険診療下で実施されたがん遺伝子パネル検査から得られたゲノムデータおよび臨床データは、各患者さんの同意のもと、C-CATに集約・保管されている。このC-CATデータは一定の条件下に研究者が利活用することができる。
注2 固形がん
血液のがん(白血病など)以外のがんの総称。
注3 がん遺伝子パネル検査
がんの組織から100種類以上の遺伝子を同時に調べることにより、がん細胞に生じた遺伝子異常(注4参照)を検出する検査のこと。この検査の結果を基に、標的治療(注5参照)を検討できる。
注4 遺伝子異常
がんのゲノムDNAに生じた変化(ゲノム異常)のうち、遺伝子に関連するもののこと。変異(DNAが置換・挿入・欠失される異常)、構造異常(長さが数十塩基対以上の異常や、染色体をまたいだ異常)、コピー数異常(常染色体のゲノムDNAは通常2コピーだが、このDNAのコピー数が増減すること)などがある。
注5 標的治療
特定の遺伝子異常を標的とした治療のこと。例えばBRAF遺伝子変異を有する大腸がんを対象としたBRAF阻害薬など。
注6 患者予後
病気の経過の見込みのこと。本研究では、がん遺伝子パネル検査を受けた患者さんが、その後どの程度の期間生存するか(あるいは生存したか)の期間のことを指す。
注7 治験
厚生労働省からの承認を得るために、未承認の新薬(あるいは新しい医療機器)の安全性と有効性を確認することを目的として、人に対して行う臨床試験。製薬会社が主体となる場合(企業治験)と医師が研究者として主体的に行う場合(医師主導治験)がある。
注8 患者申出療養制度
患者さんが未承認薬等を迅速に保険外併用療養として使用したいと希望する場合に、患者さんからの申出を起点とし、安全性・有効性等を確認しつつ、保険診療と併用して受けられるようにする制度。がん遺伝子パネル検査に基づいた推奨治療があるものの、その推奨治療薬が国内で承認されていない場合に、この制度を用いて治療薬を受けることが可能な場合がある。
注9 治療標的となる遺伝子異常・治療エビデンスレベル
各がん遺伝子異常を標的とした治療(標的治療)の推奨に関する科学的根拠の強さを治療エビデンスレベルと呼ぶ。本研究では、C-CATによって定義された治療エビデンスレベルに原則準拠しており、その基準は下記の通りである。本研究では、治療エビデンスレベルAのうち、国内承認薬がある場合を治療エビデンスレベルA(国内承認薬あり)、国内承認薬がない場合を治療エビデンスレベルA(国内承認薬なし)に分類している。また、治療エビデンスレベルA~Dの遺伝子異常を「治療標的となる遺伝子異常」と呼称している。
|
分類 |
基準 |
|
A(国内承認薬あり) |
当該がん種において国内承認薬がある。 |
|
A(国内承認薬なし) |
当該がん種において米国での承認薬がある/ ガイドラインに記載されている。 |
|
B |
当該がん種において統計的信憑性の高い臨床試験・メタ解析と専門家間の合意がある。 |
|
C |
他がん種において国内または米国における承認薬がある/ 他がん種において統計的信憑性の高い臨床試験・メタ解析と専門家間の合意がある/ がん種に関わらず、規模の小さい臨床試験で有用性が示されている。 |
|
D |
がん種に関わらず、症例報告で有用性が示されている。 |
|
E |
前臨床試験(動物実験など)で有用性が示されている。 |
注10 高い腫瘍遺伝子変異量(TMB-high)
がん細胞の中にどのくらいの遺伝子変異(遺伝子異常の一種)が蓄積しているかの総量を示す指標を腫瘍遺伝子変異量(tumor mutation burden: TMB)と呼ぶ(単位:変異/Mb)。TMBが10 変異/Mb以上のことをTMB-highと呼び、免疫チェックポイント阻害薬であるペムブロリズマブが奏功しやすいことが知られている。
日本でもペムブロリズマブは「がん化学療法後に増悪した高い腫瘍遺伝子変異量(TMB-high)を有する進行・再発の固形癌(標準的な治療が困難な場合に限る)」への適応がある。
注11 乳房外パジェット病
皮膚に分布する汗腺の一つである「アポクリン腺」に由来するといわれる皮膚がん。外陰部や肛門周囲、脇の下などアポクリン腺が多く存在する部位に生じやすい。希少がんの一つ。
注12 コンパニオン診断薬
特定の医薬品の効果があるかを調べるために、その医薬品の使用前に遺伝子異常などをあらかじめ検査する目的で使用される診断薬。がん遺伝子パネル検査自体もコンパニオン診断薬として承認されている場合があるが、ここではがん遺伝子パネル検査以外のコンパニオン診断薬のことを指す。
注13 がんゲノム医療
がん遺伝子パネル検査などによって得られた遺伝子異常の情報に基づいて、一人ひとりのがんに合わせた治療を行う医療のこと。
注14 高頻度マイクロサテライト不安定性(MSI-high)
DNAには、マイクロサテライトと呼ばれる1~数塩基の塩基配列の繰り返しが散在しているが、DNAのミスを修復するしくみが働かないようながんでは、複製ミスによりマイクロサテライトが通常と異なる反復回数を示すことがあり、これをマイクロサテライト不安定性(MSI-high)と呼ぶ。MSI-highがんも、免疫チェックポイント阻害薬が奏功しやすいことが知られている。MSI-highがんは、高い腫瘍遺伝子変異量(TMB-high)(注10参照)を示すことが多い。
注15 融合遺伝子
2つの異なる遺伝子が連結されてできる異常遺伝子のこと。発がんに関与する融合遺伝子があり、一部の融合遺伝子にはそれを標的とした治療が開発されている。例えば、NTRK融合遺伝子陽性の固形がんにはTRK阻害薬(エヌトレクチニブなど)が承認されており、臨床現場で使用可能である。
お問い合わせ先
研究に関するお問い合わせ
国立研究開発法人国立がん研究センター研究所
分子腫瘍学分野 斎藤 優樹
電話番号:03-3542-2511(代表)
Eメール: yukisai3●ncc.go.jp
広報窓口
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室
電話番号:03-3542-2511(代表)
Eメール:ncc-admin●ncc.go.jp
慶應義塾大学
信濃町キャンパス総務課
電話番号:03-5363-3611
Eメール:med-koho●adst.keio.ac.jp
