トップページ > 研究組織一覧 > 分野・独立ユニットグループ > 独立ユニットグループ > ゲノムストレス応答学ユニット > プロジェクト > DNA複製ストレス応答因子ATRキナーゼ阻害剤によるがん治療法の開発
SMARCA4遺伝子変異がんに新たな治療の可能性DNA複製ストレス応答因子ATRキナーゼ阻害剤によるがん治療法の開発
論文のポイント
- 肺がんなど多くのがんではクロマチンを制御するSMARCA4/BRG1遺伝子に欠損型変異を生じているが、有効な治療法がない。
- SMARCA4が欠損したがん細胞ではDNA複製のときのストレスが強く、ストレスに対処する役割を持つATRタンパク質を阻害すると細胞死が起きる。
- ATR阻害剤を用いることで、がん種横断的に、SMARCA4タンパク質の欠損したがんの治療が行える可能性がある。
概要
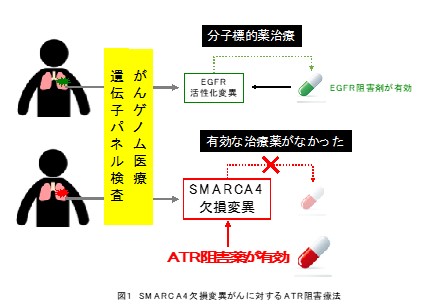
現在、遺伝子パネル検査(注1)により遺伝子変異を見出し、その変異に応じた分子標的治療薬(注2)による治療が行われています。しかし、遺伝子変異が見つかっても、対応する有効な治療薬のない患者さんも多くおられます。SMARCA4遺伝子はその代表的なもので、がん遺伝子変異のない肺がんなど、いくつかのがん種で変異が見られます。SMARCA4タンパク質は、SWI/SNFクロマチン再構成複合体(注3)の一員として、細胞中の染色体DNAのふるまいを調節しています。本研究では、ATRタンパク質(注4)に対する阻害薬を用いて、SMARCA4タンパク質の欠損したがん細胞を効率よく殺傷する治療法を発見しました(図1)。
論文内容
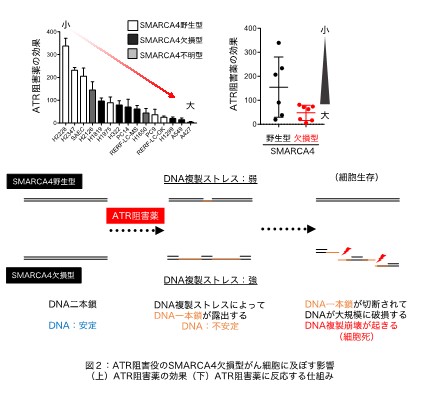
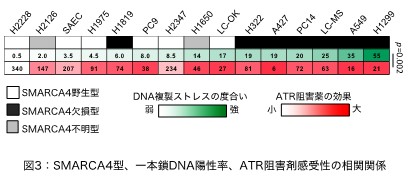
現在、保険診療として遺伝子パネル検査が行われ、その変異に応じた抗がん剤治療が行われています。SMARCA4遺伝子の変異は、いくつかのがん種で変異が見られますが、それに対応した有効な治療法がありません。特に肺がんでは、すでにある分子標的薬によって治療効果が得られるEGFR遺伝子などの変異がないがんで、SMARCA4遺伝子の変異やSMARCA4タンパク質の欠損が見られることから、有効な治療法の開発が望まれています。本研究では、SMARCA4タンパク質を欠損したがん細胞は、染色体や細胞周期に異常を示すことに着目し、DNA複製するときに発生する様々なストレス(DNA複製ストレス)(注5)に対処する役割を持つATR キナーゼタンパク質の阻害による治療法の有効性を検証しました。データベースDBKERO(https://kero.hgc.jp/(外部サイトにリンクします))から公開している日本人の肺がん細胞株のオミクス情報(ゲノム配列やmRNAの網羅的発現量)を活用し、肺がん細胞株におけるゲノム変異と遺伝子発現状態を調べました。そして、14種類の肺がん細胞に対してATRタンパク質に対する阻害剤(ATR阻害薬)の効果を調べました。その結果、SMARCA4を欠損したがん細胞ではATR阻害薬 によりがん細胞が効率よく死滅することが明らかとなりました(図2上)。ATR阻害薬はSMARCA4欠損がん細胞に対して、DNA複製ストレスを急激に引き起こしDNA複製崩壊(注6)と呼ばれる細胞死を誘導することがわかりました(図2下)。SAMRCA4タンパク質を欠損した肺がん細胞株では、他のがん細胞と比べてATR阻害薬によって誘導されるDNA複製ストレスの度合いが高く、ATR阻害薬によって死にやすいことがわかりました(図3)。これらのことからDNA複製のときに起こる様々なストレスに曝されているSAMRCA4を欠損したがん細胞では、これらのストレスに対応するATRの役割をATR阻害薬によって抑制すると細胞死を引き起こすことが明らかとなりました。
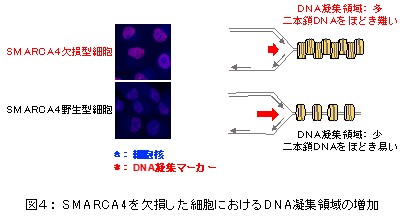
次に、SAMRCA4が欠損した細胞においてATR阻害薬がDNA複製ストレスを強く引き起こす理由に着目しました。DNAは二本の鎖が対をなす形で存在しており、DNAが複製されるときには一本鎖に解かれて、新しいDNAが合成されます。この時、DNAが硬く凝集した領域(電話線がよじれて絡まっているようなイメージ)では、DNAが解かれにくい状態となり、DNA複製の障害(DNA複製ストレスの原因)となることが知られています。またクロマチン再構成複合体因子であるSMARCA4タンパク質は、硬く凝集したDNAを緩める働きがあることが知られていました。そこでがん細胞のDNAの凝集の度合いを評価したところ、SAMRCA4が欠損した細胞において硬く凝集したDNAの領域が増加することがわかり、DNA複製ストレスが強くなる原因となることが明らかとなりました(図4)。
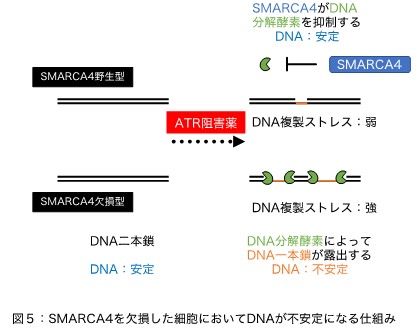
強いDNA複製ストレスによる細胞死の直接的な原因は、DNAがDNA分解酵素によって攻撃を受け不安定となり、大規模なDNAの破損が起こるためであることが知られています。非常に興味深いことに、研究グループはATR阻害薬を処理すると、SAMRCA4を欠損した細胞においてのみMre11というDNA分解酵素によってDNAが攻撃を受け、DNAが不安定になることを明らかにしました。(図5)。
以上のことから、(I)DNA凝集領域が増加することでDNA複製ストレスの原因が増加する、(II)DNA分解酵素による攻撃を受けやすいためにDNAが不安定になる、という2つの異なる理由が相乗的に働くことにより、SMARCA4タンパク質を欠損した肺がん細胞ではATR阻害薬が効率よく細胞を死滅させることが明らかとなりました。
SMARCA4 タンパク質の欠損は、肺がんのほか、小細胞卵巣がん、バーキットリンパ腫、小児髄芽腫など、他の腫瘍型にも見つかります。よって、SMARCA4タンパク質の欠損をバイオマーカーとすることによってATR阻害剤を用いた治療法は、がん種横断的に有効である可能性があります。
発表論文
雑誌名
NAR Cancer
タイトル
SMARCA4 deficiency-associated heterochromatin induces intrinsic DNA replication stress and susceptibility to ATR inhibition in lung adenocarcinoma
著者
Kiminori Kurashima, Hideto Kashiwagi, Iwao Shimomura, Ayako Suzuki, Fumitaka Takeshita, Marianne Mazevet, Masahiko Harata, Takayuki Yamashita, Yusuke Yamamoto, Takashi Kohno, Bunsyo Shiotani*
DOI
https://doi.org/10.1093/narcan/zcaa005
URL
https://academic.oup.com/narcancer/article/2/2/zcaa005/5827748 (外部サイトへリンクします)
用語解説
注1 遺伝子パネル検査
1度に多数のがんにかかわる遺伝子の変異を調べる検査。単一遺伝子の変異検査を重ねるよりも、検査時間や再生検などの患者さんの負担が軽減できる。現在、OncoGuideTM NCCオンコパネルシステム、FoundationOneR CDx がんゲノムプロファイル、FoundationOneR Liquid CDx がんゲノムプロファイルという三つの検査が保険診療で使われている。
注2 分子標的治療薬
がんの原因となる活性化したがん遺伝子産物(タンパク質)を特異的に阻害する薬。
注3 SWI/SNFクロマチン再構成複合体
DNAがヒストンと呼ばれるタンパク質に巻き付いているクロマチンの構造を変化させる活性を持つタンパク質複合体。
注4 ATR
Ataxia-telangiectacia mutated and Rad3-related kinaseの略。DNA複製ストレスの結果生じる一本鎖のDNAに応答して活性化し、下流のタンパク質をリン酸化することで、細胞周期進行やDNA修復、細胞死を制御する。
注5 DNA複製ストレス
細胞分裂の際に遺伝情報を倍加させるDNA複製において生じる様々な障害。通常は解消されることで遺伝情報が正確に保たれるが、解消されないとDNA破損の原因となる。
注6 DNA複製崩壊(replication catastrophe)
ゲノム複製の秩序が乱れ、複製フォークの失速と崩壊、大規模なDNAの破損、そして最終的には細胞死を含む壊滅的なゲノムの崩壊が生ずること。
問い合わせ先
国立がん研究センター研究所 ゲノムストレス応答学ユニット 独立ユニット長
塩谷 文章
〒104-0045 東京都中央区築地5-1-1
Tel: 03-3547-5201 内線 3681
Email:bshiotan●ncc.go.jp

