トップページ > 研究組織一覧 > 分野・独立ユニットグループ > がん創薬研究ユニット > 研究プロジェクト
研究プロジェクト
がんの分子生物学的理解や治療技術の進歩により、人類のがんに対する理解はかつてない水準に到達しています。しかしながら、がんの生物学は極めて奥深く、私たちが現在捉えているのは氷山の一角に過ぎません。進行がんの予後はいまだ厳しく、臨床の現場では治療抵抗性や再発といった課題に直面し続けています。私たちは、「がんを理解すること」と「がんを治療すること」を一体として捉え、臨床で生じた課題や疑問を出発点に、それを分子レベルで解明し、再び治療へと還元する研究を推進しています。本研究ユニットでは、主に以下の4つのアプローチに基づいて研究を展開しています。
1. 大規模検体解析によるがんの脆弱性の同定
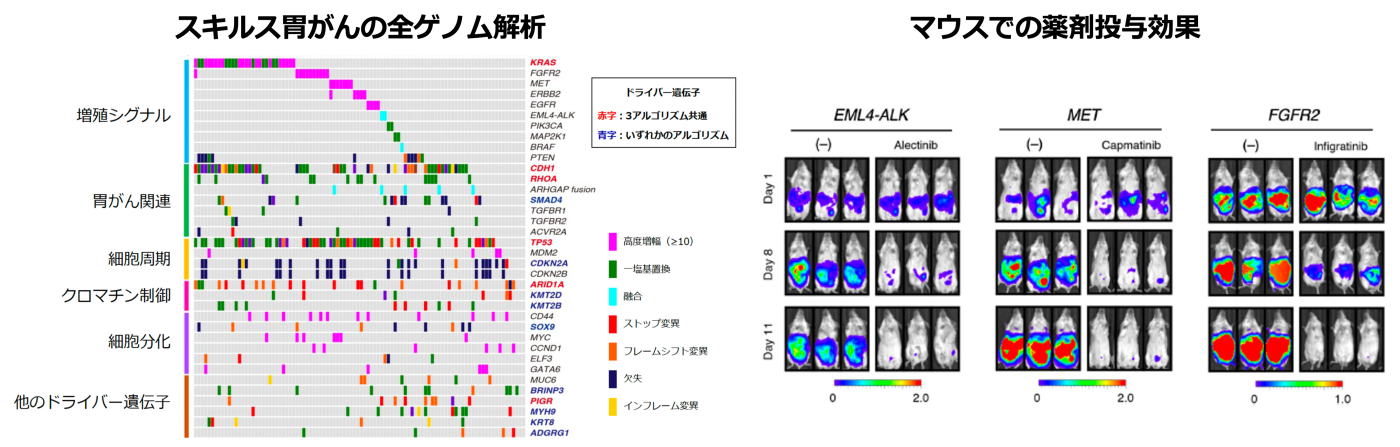
難治がんに対する新規治療標的を見いだすため、次世代シーケンサーを用いたマルチオミクス解析を基盤に、大規模な患者検体の解析を行っています。全ゲノム、トランスクリプトーム、エピゲノムなどの多層的データを統合することで、がん細胞が依存する分子機構を体系的に明らかにします。このような解析により、従来の単一遺伝子変異では捉えきれない「脆弱性」を同定することが可能となります。スキルス胃がんを対象とした研究では、包括的ゲノム解析により新規治療標的を同定し、その有効性を実験的に実証しました(Nature Cancer, 2021)。また、難治性白血病の解析からは新規融合遺伝子異常を見出し、分子機構に基づく治療可能性を提示しました(NPJ Precision Oncology, 2023)。現在も膵臓がんや肺小細胞がんなどの難治腫瘍を対象に、臨床検体に基づく網羅的解析から、実際の治療につながる標的の創出を目指しています。
2. 前がん病変の解析による発がん機構の解明
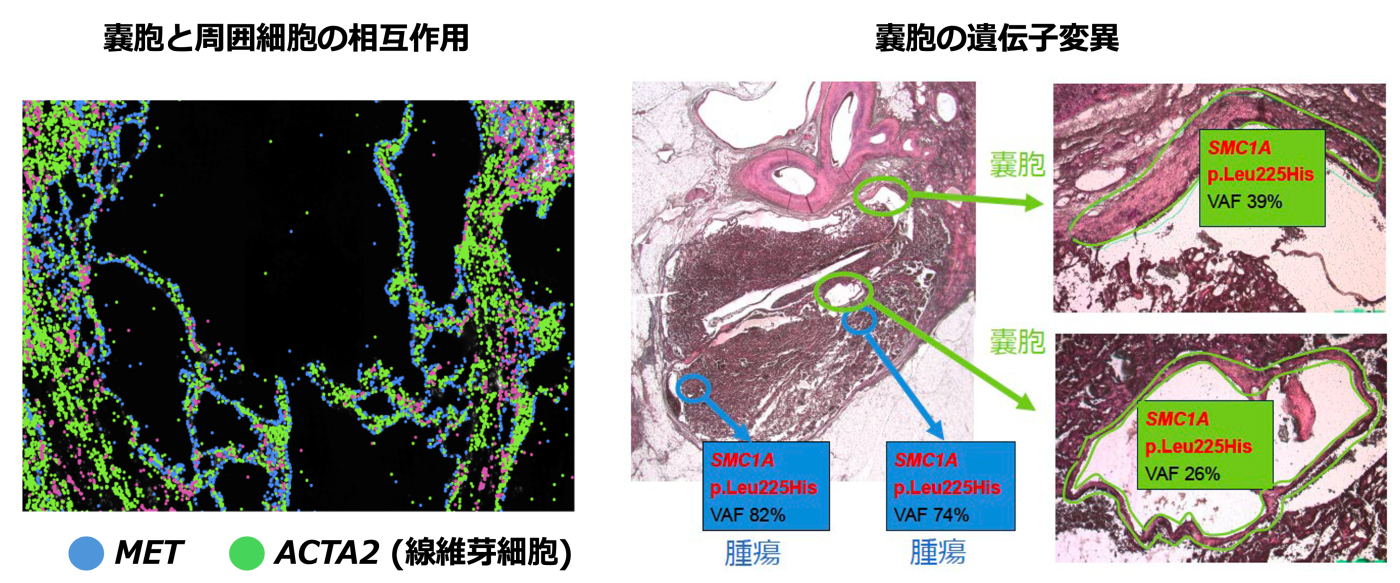
がんは突然生じるのではなく、正常組織が段階的な分子変化を経て発生します。その発生過程、すなわち前がん病変の理解は、がんの本質を捉える上で不可欠です。私たちは、シングルセル解析や空間トランスクリプトミクスを活用し、組織内の細胞状態と微小環境を高解像度で解析することで、発がんの起点となる分子変化を明らかにしています。特に、炎症や線維化といった組織環境が、クローン性増殖や遺伝子異常の蓄積をどのように促進するのかに着目しています。人工透析患者に特有の腎臓がんを対象とした研究では、透析腎に蓄積するゲノム異常と微小環境に依存した発がん機構を解明し、発がんに直結する介入点を提示しました(Cancer Discovery, 2025)。現在も多様な前がん病変を対象とした解析を進め、早期診断や予防的治療戦略の構築へとつなげています。
3. 機能検証と分子スクリーニングによる標的評価
網羅的解析から得られた候補分子が、実際に治療標的となり得るかを検証するため、機能解析を体系的に行っています。培養細胞や患者由来モデルを用いた実験に加え、CRISPR-Cas9を用いた網羅的遺伝子スクリーニングを実施し、がん細胞の生存や増殖に必須な遺伝子を同定します。これにより、「どの分子を標的とすればがんを制御できるのか」という問いに対する解を導きます。さらに、同定した脆弱性については製薬企業などと連携し、最適な薬剤の開発へと展開しています。
4.臨床との連携による治療戦略の最適化
創薬の最終的な目的は、患者さんにおける実際の治療効果の向上です。私たちは臨床医と密接に連携し、実際に薬剤が投与された患者さんの検体を解析することで、薬剤応答に関連する分子機構の解明を進めています。例えば、免疫チェックポイント阻害剤投与後の患者解析において、有効例や無効例に特徴的な分子変化を同定しました(Nature Cancer, 2025;J Immunother Cancer, 2024)。このような解析は、治療効果を規定するバイオマーカーの同定や、より適切な患者選択・治療戦略の構築につながります。

