トップページ > 研究組織一覧 > 分野・独立ユニットグループ > がん治療学研究分野
がん治療学研究分野
独自の発想が、独自の薬を生む。
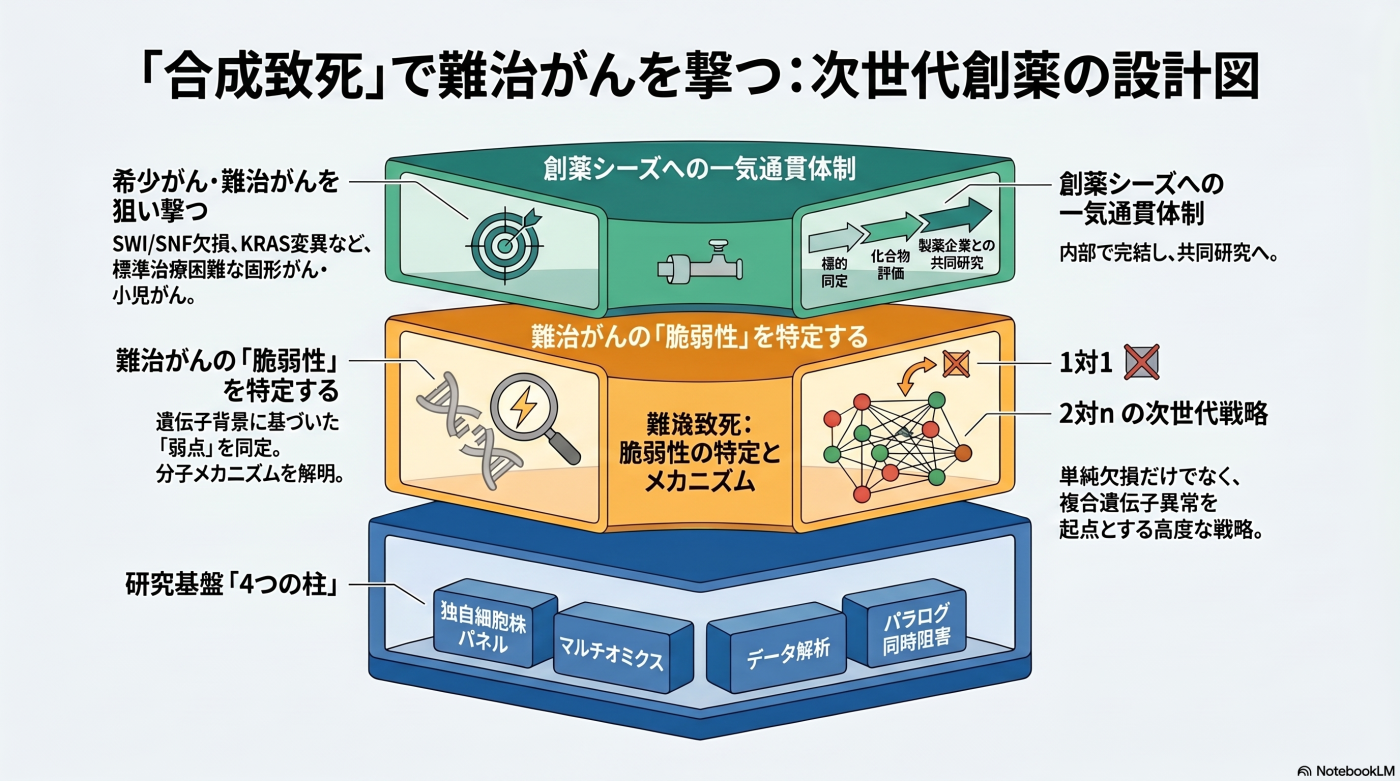
がん治療学研究分野では、合成致死(Synthetic Lethality)に基づく標的探索を軸に、SWI/SNF 欠損がん、KRAS 変異がん、SMAD4/KDM6A 欠損がんなどの難治がんを対象として、標的同定から作用機序解析、化合物評価、創薬シーズへの展開までを一気通貫で進めています。
独自のパラログ同時阻害法、希少がん・難治がん細胞株パネル、データ駆動型探索、マルチオミクス解析を組み合わせ、公共データだけでは到達しにくい治療標的の発見を目指しています。
私たちのビジョン
合成致死を、最も深く解き明かす。
「効く」という現象にとどまらず、「なぜ効くか」を分子メカニズムとして解き明かすことを重視しています。分子メカニズムの解明こそが、再現性のある創薬の出発点であり、新しい治療標的の発見につながると考えています。
私たちの研究基盤
研究室は、合成致死標的の探索から作用機序解析、化合物評価までを一気通貫で進めるための独自の研究基盤を、4 つの軸で整備しています。
- パラログ同時阻害法 ── 1 対 2 対応型の合成致死戦略
- 希少がん・難治がん細胞株パネル ── SWI/SNF 欠損、KRAS 変異、SMAD4/KDM6A 欠損などの疾患モデル
- データ駆動型探索 ── DepMap 再解析、CRISPR スクリーニング
- 作用機序・創薬評価 ── マルチオミクス(RNA-seq、ATAC-seq、CUT&RUN)、代謝解析、in vitro/in vivo 薬効評価
→ 研究基盤の詳細は 研究プロジェクト をご参照ください
希少がん・小児がん・難治性固形がんを対象とした研究
私たちが取り組むのは、有効な分子標的治療の選択肢が限られ、標準治療への抵抗性が課題となるがんです。
|
領域 |
主な対象がん |
主な遺伝子背景 |
|---|---|---|
|
希少がん・小児/AYA がん |
悪性ラブドイド腫瘍、類上皮肉腫、滑膜肉腫 |
SMARCB1 欠損、SS18-SSX 融合 |
|
婦人科・消化器の難治がん |
卵巣明細胞がん、びまん性胃がん(スキルス含む) |
ARID1A 欠損、SMAD4 欠損 |
|
難治性固形がん |
非小細胞肺がん、膵臓がん、食道がん、腎細胞がん |
SMARCA4、PBRM1、KDM6A、SMAD4 欠損、KRAS 変異 |
これらの難治性がんでは、遺伝子背景に基づく脆弱性が存在する一方で、それを十分に治療標的化できていない場合があります。私たちは、これらの脆弱性を同定し、新たな治療標的として検証しています。
→ 対象がん種ごとの研究プロジェクトは 研究プロジェクト を参照
研究ハイライト
研究室の研究は、6 つのテーマで展開しています。各テーマの詳細は、研究ハイライト の各詳細ページをご参照ください。
1. 従来型合成致死
SMARCA4 欠損がんにおける SMARCA2 依存性、CBP 欠損がんにおける EP300 依存性を示した、1 対 1 対応型の合成致死研究。
2. パラログ同時阻害法
SMARCB1 欠損がん・cBAF 欠損がんに対する CBP/p300 同時阻害を示した、1 対 2 対応型の合成致死戦略。
3. 次世代型合成致死
SMARCA4/SMARCA2 二重欠損がんに対する CHD3 依存性など、2 対 1/2 対 n 対応型の合成致死戦略。
4. データ駆動型探索
DepMap 再解析と独自細胞株パネルの統合により、ARID1A 欠損 OCCC の USP8/FGFR2 依存性を同定。
5. グルタチオン代謝脆弱性
ARID1A、SMARCB1 などの SWI/SNF 欠損がんにおける GSH 代謝依存性と GCLC 阻害戦略。
6. 既存薬の再定義
ARID1A 欠損 OCCC・びまん性胃がんにおけるゲムシタビン感受性とピリミジン代謝脆弱性。
図: 当分野の研究テーマと対象がん種の全体像。
私たちの実績
研究室の積み重ねを、3 つの軸で簡潔にお示しします。
研究発信
主要発表先: Cancer Cell(2019)/ Cancer Discov(2016)/ Nat Commun(2024)/ Cancer Res(2013、2026)/ Mol Cancer Res(2026)/ NPJ Precis Oncol(2025)/ Cancer Res Commun(2025)/ Sci Rep(2024)/ Gynecol Oncol(2019)など
創薬シーズ
論文公開済みの研究用化合物・共同研究成果として、CBP/p300 二重阻害剤 CP-C27 や、新規 GCLC 阻害剤 GCLCi1 / GCLCi0 などを用いた検証を報告しています。
共同研究・社会発信
- 製薬企業との共同研究成果を、論文公開済みの範囲で紹介(例: 小野薬品工業との GCLC 阻害剤研究 ── Cancer Res 2026)
- 2015 → 2019 → 2024 → 2026 と、節目ごとに NCC プレスリリースを通じて社会へ発信
- 連携大学院制度を通じて、大学院生を継続的に受け入れ
→ 業績の全体像は 論文業績 を参照(6 テーマ × 代表論文の Selected Publications Overview に整理しています)
プレスリリース・お知らせ
- (NEW)2026 年 3 月 17 日 ── SMARCB1 欠損希少がんの新たな治療標的を発見:グルタチオン代謝を標的とした GCLC 阻害剤のフェロトーシス誘導を介した新たな作用機序を解明 → プレスリリース
- 2024 年 6 月 26 日 ── SMARCB1 遺伝子欠損型の小児・AYA 世代のがんに有望な治療標的と阻害剤を発見 → プレスリリース
- 2019 年 1 月 25 日 ── 日本人に多い卵巣明細胞がんなどでみられる ARID1A 遺伝子変異がんを対象に、メタボロームを標的とした新たながん治療法を発見 → プレスリリース
- 2015 年 12 月 9 日 ── 肺小細胞がんや悪性リンパ腫などでみられる CBP 遺伝子変異について合成致死に基づく新しいがん治療標的を発見 → プレスリリース
サイト内ナビゲーション
共同研究、研究室見学、採用、取材に関するお問い合わせは、お問い合わせ・アクセス および メンバー紹介・採用情報 をご参照ください。
最終更新日: 2026-05-16



