低ブドウ糖環境下によるCAR-T細胞の機能不全を克服するオンデマンド型代謝強化CAR-T細胞を開発―抗腫瘍効果の向上と安全性をマウスモデルで検証―
国立研究開発法人国立がん研究センター
国立大学法人東海国立大学機構名古屋大学
国立大学法人京都大学
発表のポイント
- これまで膠芽腫のがん組織は極度の低ブドウ糖環境にあり、CAR-T細胞の機能が著しく低下する可能性が示唆されていましたが、本研究によりその実態が明らかになりました。
- 低ブドウ糖環境によるCAR-T細胞の機能不全を克服するため、ブドウ糖を高効率に取り込む細胞膜タンパク質 (ブドウ糖膜輸送体) GLUT3を必要に応じて発現させるオンデマンド型代謝強化CAR-T細胞 (On-d GLUT3 CAR-T細胞)の開発に成功しました。
- On-d GLUT3 CAR-T細胞について、ヒトの脳腫瘍を模した膠芽腫マウスモデルで検証した結果、腫瘍の根治を達成するなど、高い抗腫瘍効果が認められ、明らかな毒性は観察されませんでした。
概要
国立研究開発法人国立がん研究センター(東京都中央区、理事長:間野 博行)研究所 腫瘍免疫研究分野を中心とする研究チームは、ブドウ糖注1を高効率に取り込む細胞膜タンパク質 (ブドウ糖膜輸送体) GLUT3注2をT細胞のブドウ糖需要の高まりに応じてCAR-T細胞注3に発現させる、オンデマンド型代謝強化CAR-T細胞 (On-d GLUT3 CAR-T細胞)を開発し、極度の低ブドウ糖環境である膠芽腫注4に対する有効性をマウスモデルで検証しました(概要図)。
本研究成果により、ブドウ糖需要に応じたオンデマンド型のブドウ糖の取り込みを実現し、過剰なブドウ糖摂取によるCAR-T細胞の過度な活性化や、それに伴う有害事象を回避し、高い抗腫瘍効果と安全性を両立する可能性が示されました。また、これを検証する目的で、ヒト膠芽腫マウスモデルを用いた検討を実施した結果、腫瘍の消失を含む高い抗腫瘍効果と生存期間の延長が認められました。
On-d GLUT3 CAR-T細胞は、腫瘍の低ブドウ糖環境を克服するこれまでにない仕組みをもつ遺伝子改変T細胞であり、膠芽腫に対する、新たな治療開発につながることが期待されます。
本研究は、国立研究開発法人国立がん研究センター研究所 腫瘍免疫研究分野 渡邊 慶介主任研究員、西川 博嘉分野長 (名古屋大学大学院医学系研究科 微生物・免疫学講座 分子細胞免疫学教授、京都大学大学院医学研究科附属がん免疫総合研究センターがん免疫多細胞システム制御部門教授を兼務)らの研究チームで実施され、本成果は、米国科学雑誌「Science Translational Medicine」に米国東部時間2026年4月15日(日本時間4月16日)に掲載されました。
概要図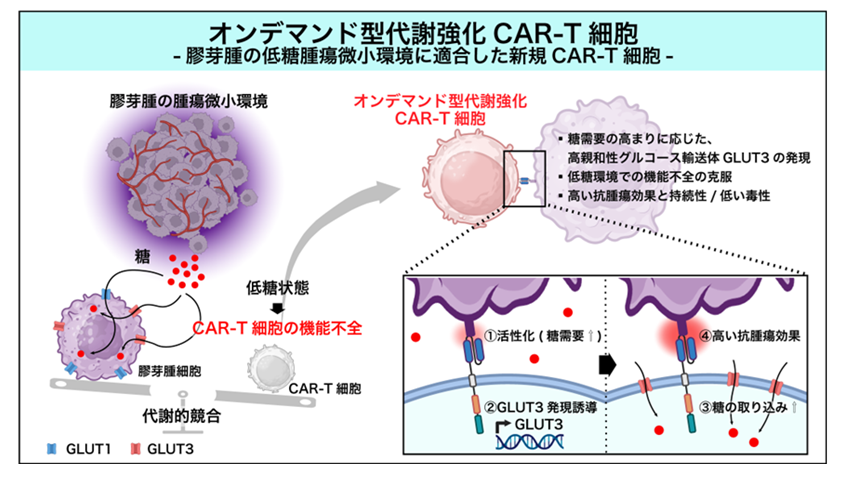
背景
膠芽腫は難治性がんのひとつで、標準治療に次ぐ新たな治療法の開発が望まれており、いくつかのCAR-T細胞療法の臨床試験が実施されていますが、残念ながら十分な効果が示されていません。その原因として、1.一般的にがん細胞は特有の代謝様式を有しており、ブドウ糖を大量に消費していること (Warburg 効果注5)、2.腫瘍のみでなく正常の脳もブドウ糖を大量に消費していること、3.膠芽腫細胞は、低ブドウ糖環境でも高効率にブドウ糖を取り込む細胞膜タンパク質 (ブドウ糖膜輸送体)を高く発現し、免疫細胞とのブドウ糖の奪い合いに優位にたっていることが挙げられます。これらの要因から、膠芽腫のがん組織は極度の低ブドウ糖環境であり、CAR-T細胞の機能が阻害されているため、このような低ブドウ糖環境でも十分な機能を発揮するCAR-T細胞の開発が必須であると考えられてきました。
研究成果
1. 膠芽腫のがん組織は極度の低ブドウ糖環境下にあり、CAR-T細胞が正常に機能しない
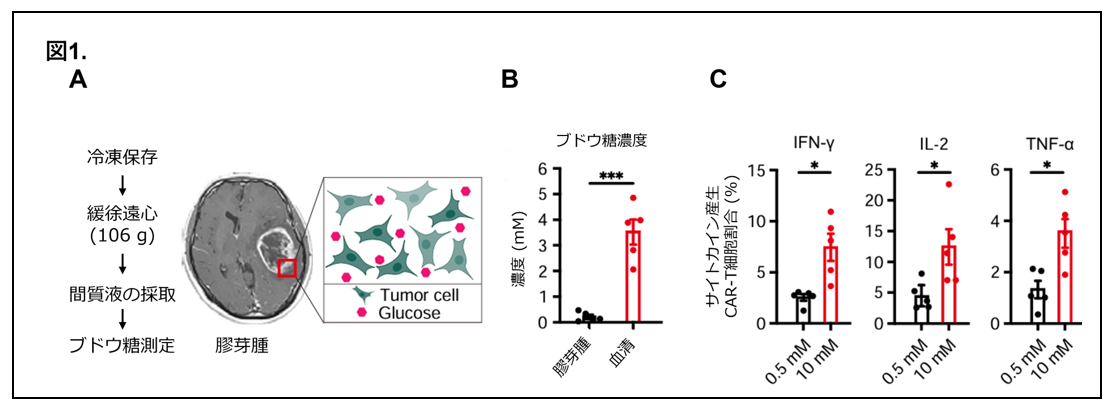
膠芽腫のブドウ糖環境がCAR-T細胞機能にどのような影響を与えるか解明するため、患者さんから摘出した腫瘍の一部を用いて、膠芽腫のブドウ糖濃度を測定しました (図1A)。その結果、膠芽腫内のブドウ糖濃度は血液中と比べ10分の1未満と極めて低濃度であり (図1B)、このような低ブドウ糖環境では、CAR-T細胞のサイトカイン産生能注6や細胞傷害活性注7など重要な機能が著しく低下することが明らかになりました (図1C)。このことから、膠芽腫においては、低ブドウ糖環境でもCAR-T細胞が有効に機能するための戦略をたてる必要があると考えられました。
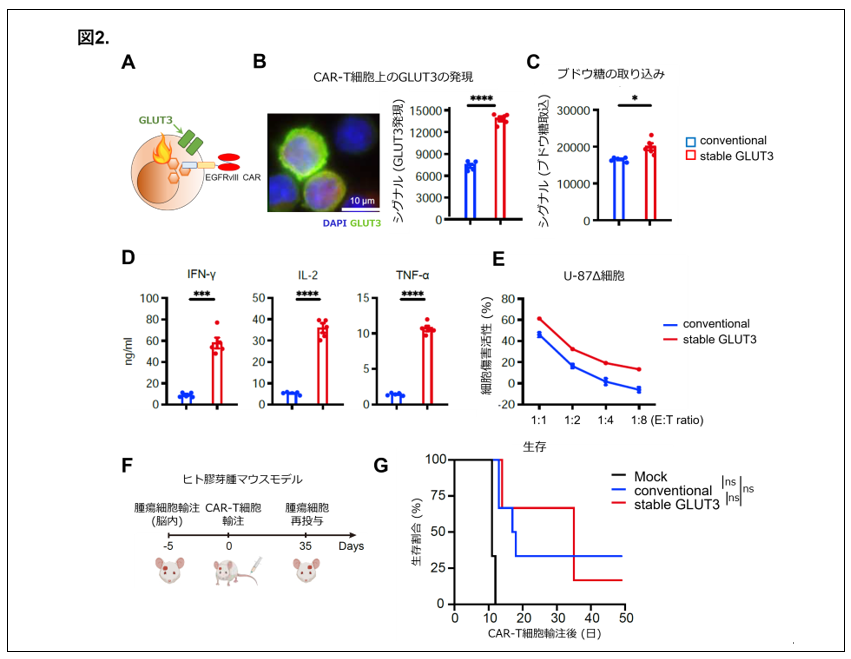
2. GLUT3を持続的にCAR-T細胞に発現させることで、CAR-T細胞の活性化が得られたが、ブドウ糖の過剰な取り込みによる毒性も認められた
CAR-T細胞のブドウ糖の取り込みを強化するため、効率的にブドウ糖の取り込みを担っているGLUT3を、CAR-T細胞に持続的に人工発現させたCAR-T細胞 (stable GLUT3 CAR-T細胞)を開発しました (図2A)。CAR-T細胞は持続的にGLUT3を発現し (図2B)、低ブドウ糖状態においても、従来のCAR-T細胞と比べ高いブドウ糖の取り込み能を示し (図2C)、その結果強いサイトカイン産生能 (図2D)、細胞傷害活性 (図2E)を発揮することが明らかになりました。しかし、ヒト膠芽腫マウスモデルでの検討 (図2F)では、予想に反し、stable GLUT3 CAR-T細胞による明らかな抗腫瘍効果や生存期間の延長は確認できませんでした (図2G)。詳細に検討すると、GLUT3による持続的なブドウ糖の取り込みがCAR-T細胞を過剰に活性化することでマウスモデルにおいて有害事象が発生すること、また、ブドウ糖取り込みによる過度な活性化によりCAR-T細胞は一時的に強い活性化を示すものの短期間に死んでしまうため長期の抗腫瘍効果が発揮されないためであることがわかりました。この結果により、GLUT3を持続的に発現させる手法では、CAR-T細胞がブドウ糖を大量に取り込んで過剰に活性化するため、過剰なT細胞の活性化を引き起こし、マウスモデルにおいて、安全性上の重大な問題となる毒性が認められました。
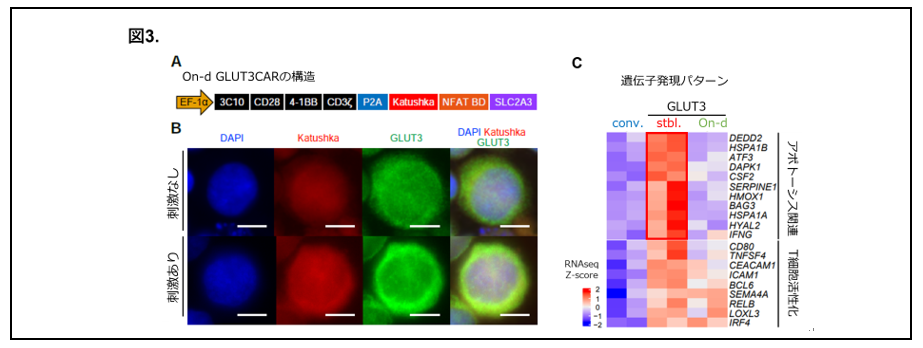
3. ブドウ糖需要にあわせてブドウ糖の取り込みを高めるオンデマンド型代謝強化CAR-T細胞 (On-d GLUT3 CAR-T細胞)を開発
CAR-T細胞がブドウ糖を過剰に取り込むことを防ぐため、腫瘍内でCAR-T細胞が活性化した時、つまりCAR-T細胞のブドウ糖の需要の高まりに伴ってGLUT3を発現するオンデマンド型代謝強化CAR-T細胞 (On-d GLUT3 CAR-T細胞)を開発しました (図3AB)。また、持続的にGLUT3を発現させた際に認められた、大量のブドウ糖取り込みに伴う過剰なCAR-T細胞の活性化によるT細胞死 (アポトーシス注8)などのCAR-T細胞への毒性は認められませんでした (図3C)。
4. On-d GLUT3 CAR-T細胞はヒト膠芽腫マウスモデルで腫瘍の根治を含む高い抗腫瘍効果を示した
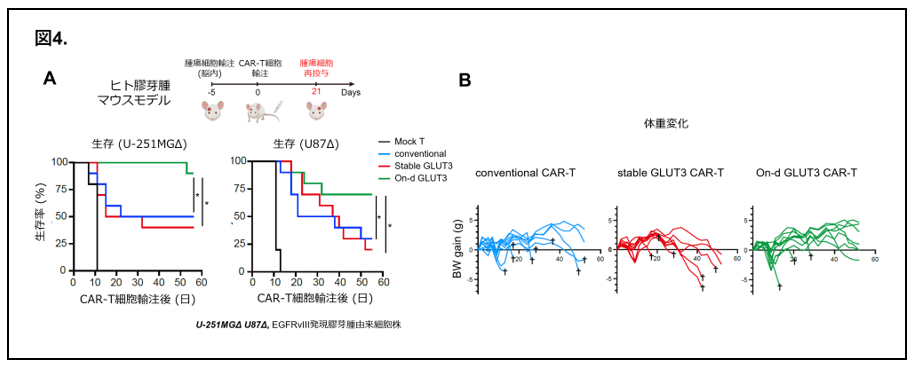
On-d GLUT3 CAR-T細胞は低ブドウ糖環境においても、従来のCAR-T細胞と比べ、有意にブドウ糖を取り込み、その結果強いサイトカイン産生能、細胞傷害活性を発揮することが明らかになりました。また、二種類のヒト膠芽腫マウスモデルにて抗腫瘍効果を検討したところ (図4A左)、従来型のCAR-T細胞やGLUT3を持続的に発現するCAR-T細胞 (stable GLUT3 CAR-T細胞)では効果が限定的であった一方、On-d GLUT3 CAR-T細胞では、腫瘍の消失を含む高い抗腫瘍効果と生存期間の延長が認められました (図4A中、右)。さらに、stable GLUT3 CAR-T細胞では体重減少や非腫瘍死等の毒性を疑わせる所見が認められましたが、On-d GLUT3 CAR-T細胞ではその様な毒性は認められませんでした (図4B)。
5. マウスモデルでの検討により、On-d GLUT3 CAR-T細胞の安全性の高さが示された
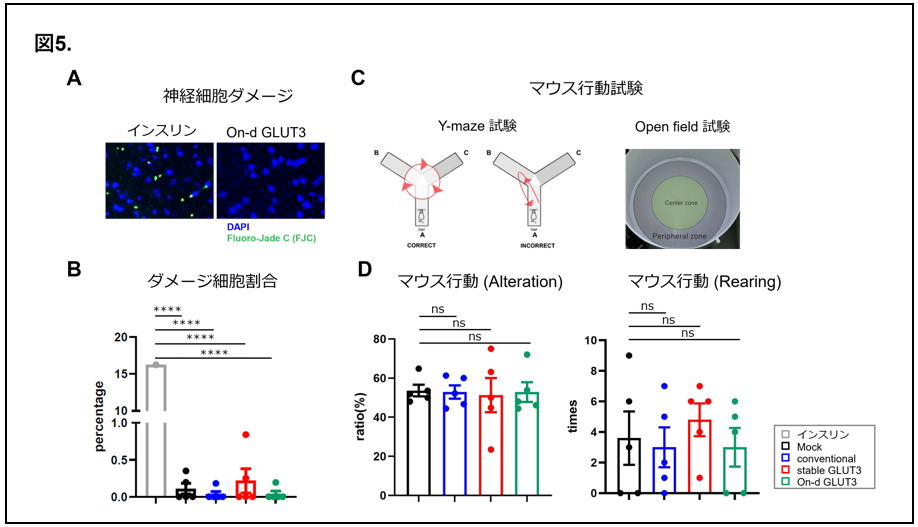
最後に、ブドウ糖の取り込みが強化され、抗腫瘍効果が高まったことを踏まえ、安全性への影響をより詳細に検討するため、ヒト膠芽腫マウスモデルでのCAR-T細胞投与後の脳に対する毒性を評価しました。CAR-T細胞投与後、マウスを解剖し、神経細胞の損傷を検知する色素 (Fluoro-Jade C;FJC)にて評価したところ (図5A)、On-d GLUT3 CAR-T細胞で治療したマウスには神経細胞の損傷の兆候は認められませんでした (図5B)。また、認知行動試験注9(図5C)においても、On-d GLUT3 CAR-T細胞の治療による行動変化や異常行動は認められず、正常脳に対する毒性が低いことを確認しました (図5D)。
展望
今回、高効率にブドウ糖を取り込む細胞膜タンパク質GLUT3をCAR-T細胞のブドウ糖需要の高まりにあわせて発現させるオンデマンド型代謝強化CAR-T細胞 (On-d GLUT3 CAR-T細胞)を開発しました。On-d GLUT3 CAR-T細胞は、低ブドウ糖環境下においてもCAR-T細胞の適切な活性化と同時に長期の抗腫瘍効果が得られることがヒト膠芽腫マウスモデルにおける検証で示されました。今後、がん組織が低ブドウ糖環境である膠芽腫に対する、新たな治療開発につながることが期待されます。
論文情報
雑誌名
Science Translational Medicine
タイトル
On-demand GLUT3 expression augments CAR-T cell metabolic fitness and antitumor efficacy in preclinical models of glioblastoma
著者
Junya Yamaguchi1,2,†, Keisuke Watanabe3,†, Akihiro Nakamura2,3,†, Nina Yi-Tzu Lin3, Sachi Maeda2, Daisuke Sugiyama1, Shinichiro Kato1,4, Akihito Nagata3, Hitomi Nishinakamura3, Kota Itahashi3, Shohei Koyama3,5, Hiroyuki Mizoguchi6, Yukihiro Shiraki7, Atsushi Enomoto7, Fumiharu Ohka2, Kazuya Motomura2,8, Yuichiro Tsukada9, Masaaki Ito9, Yuka Maeda3, Ryuzo Ueda1, Atsushi Natsume10, Ryuta Saito2, and Hiroyoshi Nishikawa1,3,4,11
所属
1Department of Immunology, Nagoya University Graduate School of Medicine, Nagoya 466-8550, Japan.
2Department of Neurosurgery, Nagoya University Graduate School of Medicine, Nagoya 466-8550, Japan.
3Division of Cancer Immunology, Research Institute/Exploratory Oncology Research & Clinical Trial Center (EPOC), National Cancer Center Japan, Tokyo 104-0045/Chiba 277-8577, Japan.
4Division of Cancer Immune Multicellular System Regulation, Center for Cancer Immunotherapy and Immunobiology (CCII), Graduate School of Medicine, Kyoto University, Kyoto 606-8501, Japan.5Department of Immunogenomic Medicine, National Cancer Center Research Institute, Tokyo 104-0045, Japan.
6Department of Neuropsychopharmacology and Hospital Pharmacy, Nagoya University Graduate School of Medicine, Nagoya 466-8560, Japan.
7Department of Pathology, Nagoya University Graduate School of Medicine, Nagoya 466-8550, Japan.
8Division of Neurosurgery, Shizuoka Cancer Center, Nagaizumi 411-8777, Japan.
9Department of Colorectal Surgery, National Cancer Center Hospital East, Kashiwa 277-8577, Japan.
10Institute of Innovation for Future Society of Nagoya University, Nagoya 466-8550, Japan.
11Kindai University Faculty of Medicine, Osaka-sayama 589-8511, Japan.†These authors contributed equally to this study.
*Correspondence to: Hiroyoshi Nishikawa, MD, PhD.
DOI
10.1126/scitranslmed.adu3532
掲載日
米国東部時間2026年4月15日(日本時間4月16日)付
URL
https://www.science.org/doi/10.1126/scitranslmed.adu3532(外部サイトにリンクします)
研究費
文部科学省
- 科学研究費助成事業 基盤研究(A)「がん組織の空間的マルチスケール解析による免疫監視と免疫寛容制御機構の解明」
国立研究開発法人日本医療研究開発機構(AMED)
- ムーンショット型研究開発事業 「慢性炎症の制御によるがん発症ゼロ社会の実現」
- 次世代がん医療加速化研究事業「腫瘍浸潤細胞の時間的空間的変化に基づく免疫抑制機構の解明と治療への展開 」
- 次世代がん医療加速化研究事業「固形腫瘍の代謝チェックポイントを打破するCART細胞療法の開発」
- 橋渡し・臨床加速化プロジェクト 橋渡し研究プログラム preF 「膠芽腫に対する新規賦活化機構実装CAR-T細胞療法の開発」
など
国立がん研究センター研究開発費
- 31-A-7 「がん免疫療法抵抗性を解除する新規治療法の臨床展開に向けた開発研究」
- 2024-A-03 「先進的免疫ゲノム解析確立に向けた検体バンキングと網羅解析基盤の樹立」
企業
- ARC Therapies株式会社 共同研究「新規免疫細胞療法の開発」
用語解説
注1 ブドウ糖
体内で主要なエネルギー源として利用される糖類。CD8+T細胞 (キラーT細胞)が活性化した際には、多くのブドウ糖を消費する。
注2 GLUT3(グルコース輸送体)
細胞膜に存在し、細胞内にブドウ糖を取り込む役割を担う輸送タンパク質 (トランスポーター)。複数の種類があり、GLUT1は多くの細胞に存在し、神経系細胞やそこから発生する脳腫瘍には、より高効率にブドウ糖を取り込む能力を有するGLUT3が発現することが知られている。
注3 CAR-T細胞(キメラ抗原受容体遺伝子改変T細胞)
がん細胞やウイルス感染細胞の排除に重要な役割を果たす免疫細胞の一種であるT細胞に、がんの目印 (抗原)を認識し、T細胞を活性化させる人工受容体タンパク質 (CAR)を導入した細胞のこと。血液がんに対し複数のCAR-T細胞製品が実用化されている。
注4 膠芽腫
脳に発生する悪性腫瘍のひとつで、成人、50~60代での発症が多い。手術、化学放射線療法が標準治療であるが、難治性がんのひとつであり標準治療に次ぐ治療法開発が望まれている。
注5 Warburg効果
がん細胞に特徴的な代謝様式で、酸素が十分に存在する環境下においても、エネルギー効率の悪い嫌気性解糖を行い、大量のグルコースを消費し乳酸を排出する現象。
注6 サイトカイン産生能
サイトカインは、免疫系細胞にて産生される細胞間情報物質である。サイトカイン産生能はT細胞の重要な役割のひとつで、T細胞の機能や性質を反映する。
注7 細胞傷害活性
免疫細胞ががん細胞やウイルス感染細胞などを殺傷する活性。サイトカイン産生と同じく、T細胞の重要な役割のひとつで、T細胞の機能や性質を反映する。
注8 アポトーシス
プログラム死ともよばれる制御された細胞死のひとつ。アポトーシスは様々な細胞に、様々な誘引で引き起こされるが、一例として、T細胞は過剰な活性化によりアポトーシスが誘導されることが知られている。
注9 認知行動試験
マウスを用いて行動や記憶、学習など公示機能を評価するための実験。本研究では、CAR-T細胞の毒性の評価として用いた。
お問い合わせ先
研究に関するお問い合わせ
国立研究開発法人国立がん研究センター研究所
腫瘍免疫研究分野 主任研究員 渡邊 慶介
電話番号:03-3542-2511(代表)
Eメール:keiswata●ncc.go.jp
広報窓口
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室
電話番号:03-3542-2511(代表)
Eメール:ncc-admin●ncc.go.jp
国立大学法人東海国立大学機構名古屋大学
医学部・医学系研究科 総務課
電話番号:052-744-2228
Eメール:iga-sous●t.mail.nagoya-u.ac.jp
国立大学法人京都大学 広報室 国際広報班
電話番号:075-753-5729
Eメール:comms●mail2.adm.kyoto-u.ac.jp
