日本初の吸収性食道用ステント「ELLA-BDステントPX」が 薬事承認を取得しました
2025年6月3日
株式会社パイオラックスメディカルデバイス
国立研究開発法人国立がん研究センター
発表のポイント
- 株式会社パイオラックスメディカルデバイスと国立がん研究センター東病院が共同研究で臨床試験を行った「ELLA-BDステントPX」が吸収性食道用ステントとして日本で初めて薬事承認されました。
- 「ELLA-BDステントPX」は、標準的治療で治療困難な難治性食道良性狭窄に対して使用される生分解性ステントです。「ELLA-BDステントPX」は生分解性素材を使用しており、食道がん手術などの後に起こることがある食道良性狭窄の患者さんに留置することで、食道の通りを良くします。本製品は約3ヶ月で加水分解される為、体外へ取り出す必要がありません。臨床試験(先進医療B、企業治験)で、嚥下障害評価が有意に改善されたという結果が示されました。
- 今後は、日本初の「吸収性食道用ステント」として、新たな特定保険医療材料区分での保険適用の手続きを行っていきます。
概要
株式会社パイオラックスメディカルデバイス(代表取締役:山本 由理、神奈川県横浜市)と国立研究開発法人国立がん研究センター(理事長:間野 博行、東京都中央区)東病院(病院長:土井 俊彦、千葉県柏市、以下「国立がん研究センター東病院」)が共同研究で臨床試験を行った「ELLA-BDステントPX」(BD Stent、社名:ELLA-CS, s.r.o.、本社:フラデツ・クローラヴェー、チェコ共和国)が、2025年3月7日付で、厚生労働大臣より製造販売承認(以下、薬事承認)されました。本製品は、日本国内で初めて薬事承認を取得した吸収性食道用ステントとなります。本製品を使用した臨床試験では、難治性食道良性狭窄注1の患者さんにおいて嚥下障害評価の改善が示されました。
本製品は、生分解性素材の一つであるポリジオキサノンを使用しています。ポリジオキサノンは、日本においても外科用縫合糸として広く使用されている素材です。この生分解性の特性により、体内に留置されたステントは約3ヶ月で分解・吸収されるため、体外への抜去が不要となり患者さんの負担を軽減するとともにQOL(Quality Of Life:生活の質)の向上が期待されます。
製造販売業者:株式会社パイオラックスメディカルデバイス
一般的名称:吸収性食道用ステント
承認番号:30700BZX00048000
販売名:ELLA-BDステントPX
承認取得日:2025年3月7日
外国製造業者:ELLA-CS, s.r.o.(チェコ共和国)
URL:https://ellacs.eu/(外部サイトにリンクします)
「ELLA-BDステントPX」 (イメージ画像)

「ELLA-BDステントPX」が分解される様子(イメージ画像)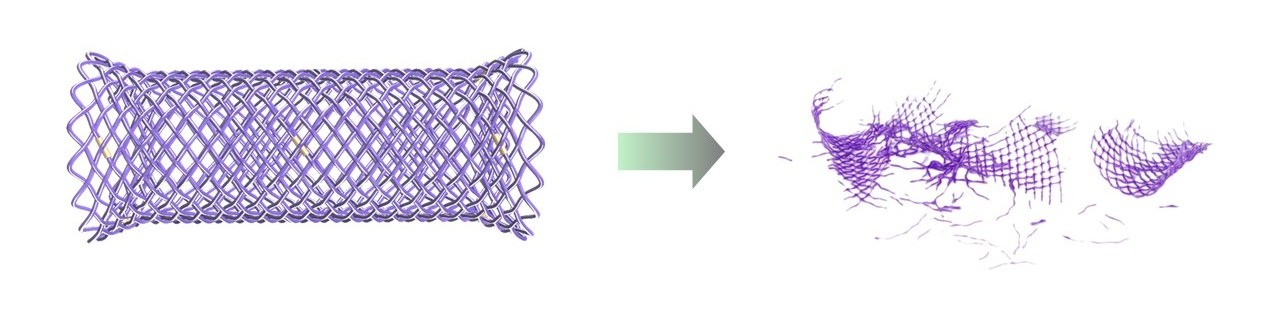
加水分解注2前の「ELLA-BDステントPX」 約3ヶ月後
背景
食道がんに対する標準的治療は外科手術が推奨されていますが、早期発見された患者さんに対しては、内視鏡を用いた切除が推奨されています。内視鏡切除には、内視鏡的粘膜切除術(Endoscopic Mucosal Resection:EMR)注3、内視鏡的粘膜下層剥離術(Endoscopic Submucosal Dissection:ESD)注4が行われており、広範な食道がんはESDで治療されることが一般的です。外科手術やESDでは、がんを切除したにも関わらず、一定の割合で術後の食道に良性狭窄を発症する場合があります。
現在、日本において食道良性狭窄(食道が細くなる)に対しては、内視鏡的バルーン拡張術(Endoscopic Balloon Dilatation:EBD)注5やブジー法注6による治療が一般的に行われています。これらの既存治療を施しても、繰り返し狭窄の発現する患者さんが難治性食道良性狭窄と診断され、EBD等の拡張処置を長期間、かつ定期的に実施することとなります。そして通院、施術の頻度が高くなり、再狭窄も短い周期で起こることから、狭窄による嚥下障害により、十分な栄養摂取ができず、低体重、栄養失調などの症状を来す場合があります。
こうした医療現場における課題や、患者さんの身体的・精神的苦痛を含むQOLの低下を解決するため、株式会社パイオラックスメディカルデバイスと国立がん研究センター東病院は、本製品の日本国内導入に向けた臨床試験に取り組むことになりました。結果を踏まえ、患者さんのQOL改善や身体的、経済的負担の軽減が期待できる医療機器であると判断し、NEXT医療機器開発センターの支援のもと、適正使用指針の作成などを経て薬事承認の申請を行いました。
臨床試験と企業治験の詳細
【先進医療B注7での臨床試験】
食道がん治療後の難治性良性狭窄の患者さんを対象として、生分解性ステント留置術の有効性と安全性を評価した試験で、2012年5月から2015年7月まで、国立がん研究センター東病院臨床研究支援部門の支援の下、国内4施設で実施しました。この試験は、先進医療Bの制度を活用し、国立研究開発法人日本医療研究開発機構(AMED)から資金提供を受け実施しました。研究に参加された18名の患者さんのうち、12名の患者さんが3ヶ月時点で食事の飲み込みづらさの症状の改善を認めました。
研究代表者:矢野 友規 (国立がん研究センター東病院 消化管内視鏡科長、医療機器開発推進部門 医療機器開発推進部長、内視鏡センター長、先端医療開発センター 内視鏡機器開発分野長)
臨床研究実施計画・研究概要公開システム:UMIN(試験ID:UMIN000008054)
先進医療で実施した試験の結果を株式会社パイオラックスメディカルデバイスに導出し、日本での薬事承認を目的とした治験が計画されました。
【企業治験】
難治性良性食道狭窄の患者さんを対象として、生分解性ステント(BD-stent)の有効性と安全性を評価した企業治験注8で、2017年4月から2020年3月まで、国立がん研究センター東病院をはじめとした9施設で実施しました。この治験に参加された30名の患者さんのうち、14名の患者さんが食事の飲み込みづらさの症状の改善を認めました。
治験依頼者:株式会社パイオラックスメディカルデバイス
治験調整医師:矢野 友規 (国立がん研究センター東病院 消化管内視鏡科長、医療機器開発推進部門 医療機器開発推進部長、内視鏡センター長、先端医療開発センター 内視鏡機器開発分野長)
医学専門家:前谷 容(東邦大学医学部内科学講座 消化器内科学分野(大橋)教授)【治験当時】
臨床研究実施計画・研究概要公開システム:治験実施計画書番号 BDS-001-001
臨床試験の結果
DS(dysphagia score:嚥下障害スコア)の値が高いほど、食事がとりにくい・飲み込みにくいといった障害の程度が強いことを意味します。
臨床試験では、DSが2以上の患者さんの割合の減少が確認できました。
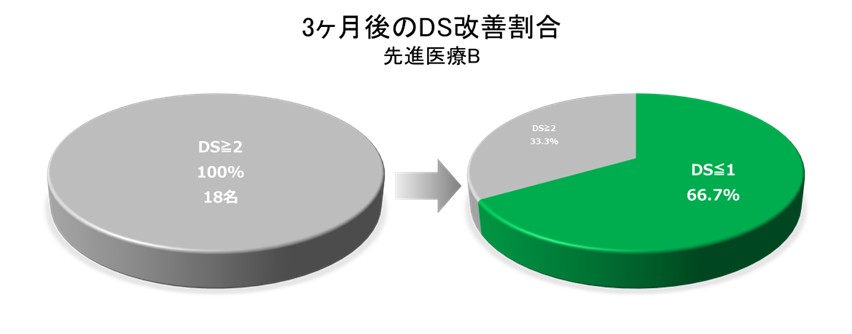
先進医療Bの成績…ELLA-BDステントPXを留置したDS2以上の患者さん(18名)のうち、3ヶ月後にDSが1以下に改善された患者さんの割合は66.7%(12名)でした。
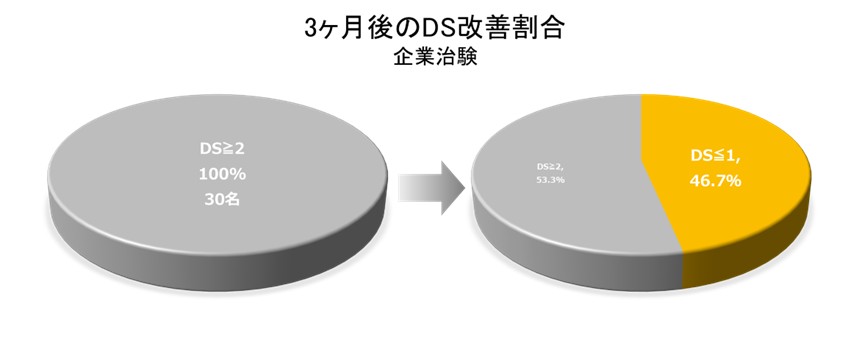
企業治験の成績…ELLA-BDステントPXを留置したDS2以上の患者さん(30名)のうち、3ヶ月後にDSが1以下に改善された患者さんの割合は46.7%(14名)でした。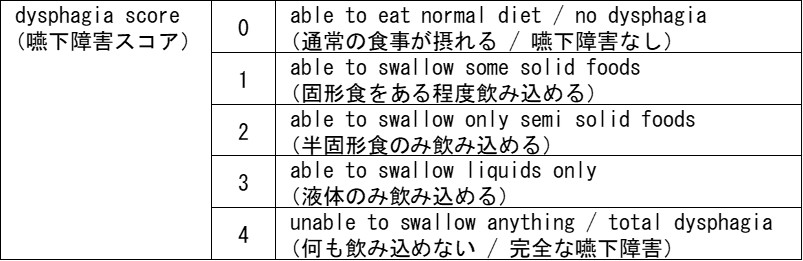
展望
株式会社パイオラックスメディカルデバイスは、患者さんの医療費自己負担の軽減を目的として、本製品の特定保険医療材料として保険適用の手続きを進めていきます。保険適用には、国立がん研究センター東病院において実施された、難治性良性食道狭窄の患者さんのQOL改善のエビデンスが主な根拠として提示されます。本製品は、日本初の吸収性食道用ステントであり、該当する特定保険医療材料の機能区分が存在しません。そのため、新たな機能区分での保険適用を目指し、厚生労働省に保険適用希望書を提出する予定です。保険適用に関する情報は、株式会社パイオラックスメディカルデバイスのウェブサイトで追ってお知らせします。
論文情報
雑誌名
Esophagus
タイトル
Pivotal trial of a biodegradable stent for patients with refractory benign esophageal stricture.
著者
Yano Tomonori, et al.
DOI
10.1007/s10388-022-00909-6
掲載日
2022年2月1日
URL
https://pubmed.ncbi.nlm.nih.gov/35106667/(外部サイトにリンクします)
雑誌名
Gastrointestinal Endoscopy
タイトル
Prospective trial of biodegradable stents for refractory benign esophageal strictures after curative treatment of esophageal cancer.
著者
Yano Tomonori, et al.
DOI
10.1016/j.gie.2017.01.011
掲載日
2017年1月27日
URL
https://pubmed.ncbi.nlm.nih.gov/28137598/(外部サイトにリンクします)
研究費
研究費名:国立研究開発法人日本医療研究開発機構(AMED)
研究事業名:医療機器開発推進研究事業(15hk0102022h001)
研究課題名:食道癌根治的治療後の難治性良性狭窄に対する生分解性ステント(BD-stent)留置術の有効性評価試験
研究代表者名:矢野 友規(国立がん研究センター東病院 消化管内視鏡科長、医療機器開発推進部門 医療機器開発推進部長、内視鏡センター長、先端医療開発センター 内視鏡機器開発分野長)
用語解説
注1 難治性食道良性狭窄
食道が狭くなり食べ物や飲み物が通りにくくなる状態で、内視鏡でのがんの所見がなく、食道を拡げる治療が繰り返し必要な狭窄です。
注2 加水分解
水を使って物質を分解する反応です。ポリジオキサノン(Polydioxanone)は体内で、最終的には水と二酸化炭素に分解されます。
注3 内視鏡的粘膜切除術(Endoscopic Mucosal Resection:EMR)
早期の消化管がんや前がん病変など、粘膜層にとどまる病変を対象に行う治療法です。開腹手術を行わずに、内視鏡を使って病変を切除できる低侵襲な治療法として普及しています。はっきりした茎やくびれのないがんに対する治療法で、周波電流を使ってがんを切除し、がんの下の粘膜下層に生理食塩水などを注入してがんを浮き上がらせます。内視鏡の先端からスネア(輪状のワイヤ)を出し、浮き上がった部分の根元に掛けて、ワイヤを少しずつ絞め、高周波電流を使って焼き切ります。その際、切断した面にがんが残らないように、病変の周囲の正常な粘膜も含めて一緒に切除します。
注4 内視鏡的粘膜下層剥離術(Endoscopic Submucosal Dissection:ESD)
早期の消化管がんや前がん病変に対して行われる内視鏡治療の一つで、病変の周りの粘膜下層を切開し、粘膜下層から病変を切除します。特に、広範囲にわたる病変や、EMRでは切除が難しい症例に適した治療法です。病変の周りの粘膜下層を切開し、粘膜下層から病変をはがしとり、がんの下の粘膜下層に生理食塩水やヒアルロン酸ナトリウムなどを注入してがんを浮き上がらせます。がんの周りの粘膜を高周波ナイフで切開し、粘膜下層から病変をはがしとります。
注5 内視鏡的バルーン拡張術(Endoscopic Balloon Dilatation:EBD)
食道や腸管などの消化管が狭くなった部分(狭窄部)に対し、内視鏡を用いてバルーン(風船状の器具)を挿入し、内部から拡張する治療法です。
注6 ブジー法
消化管の狭くなった部分(狭窄部)に対して、細長い棒状の器具(ブジー)を挿入して、徐々に拡張する治療法です。
注7 先進医療B
保険診療と先進的な医療技術(未承認の医療機器など)を併用することを可能にする制度で、患者さんにより多くの治療オプションを提供し、臨床試験の一部が健康保険でカバーされることで患者さんの負担を軽減する制度です。
注8 企業治験
医療機器メーカーなどの企業が主体となって行う臨床試験のことで、新薬や医療機器の有効性と安全性を確認し、薬事承認を得るために行われます。
国立がん研究センター東病院 NEXT医療機器開発センターについて
NEXT医療機器開発センターは、産学官・医工連携で臨床ニーズに基づいた次世代に望まれる革新的医療機器を開発するため、国立がん研究センター東病院に2017年5月に開設された組織です。医療機器企業、ものづくり企業、アカデミア、そして地域との連携で、医療機器開発を推進するとともに、臨床試験・治験のフィールドで医療機器開発を支援しています。また、臨床と隣り合わせのインキュベーション施設として人材育成、情報発信に取り組んでいます。
お問い合わせ先
製品に関する問い合わせ
株式会社パイオラックスメディカルデバイス
グローバルマーケティング部
電話番号:045-577-0021
ホームページ:https://www.piolax-md.co.jp/ (外部サイトにリンクします)
研究に関する問い合わせ
国立研究開発法人国立がん研究センター東病院
NEXT医療機器開発センター事務局
電話番号:04-7130-0199
Eメール:NEXT_AxL●east.ncc.go.jp
国立がん研究センターへの取材に関する問い合わせ
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室(柏キャンパス)
電話番号:04-7133-1111(代表)
Eメール:ncc-admin●ncc.go.jp
