アンドロゲン受容体陽性唾液腺がんに対するダロルタミドの効能追加承認-唾液腺がんに対する世界初のホルモン療法が誕生-
2026年3月23日
国立研究開発法人国立がん研究センター
国立大学法人神戸大学
発表のポイント
- アンドロゲン受容体(AR)陽性唾液腺がんに対して、AR阻害薬ダロルタミドが効能追加承認されました。
- 本承認は、唾液腺がんに対するホルモン療法として世界初の薬事承認です。
- 本承認は、医師主導治験である国内多施設共同第II相試験(DISCOVARY試験)の結果に基づくものです。
- これまで標準的な分子標的治療が確立していなかったAR陽性唾液腺がんに対し、新たな治療選択肢を提供します。
概要
国立研究開発法人国立がん研究センター(理事長:間野 博行、所在地:東京都中央区)東病院(病院長:土井 俊彦、所在地:千葉県柏市)頭頸部内科の田原 信科長、岡野 晋医長、神戸大学医学部附属病院腫瘍センターの清田 尚臣特命准教授らは、アンドロゲン受容体(AR)陽性唾液腺がんを対象に、ダロルタミドの有効性と安全性を検証する第II相試験を実施しました。その結果、ダロルタミドとゴセレリンを併用する複合アンドロゲン遮断(Combined Androgen Blockade:CAB)療法注1において、奏効割合(腫瘍が一定以上縮小した患者さんの割合)45.2%、無増悪生存期間中央値(病気が悪化せずに過ごせた期間の中央値)は13.1か月で、良好な抗腫瘍効果が示されました。
これらの結果に基づき、ダロルタミドは、ゴセレリンとの併用においてAR陽性唾液腺がんに対する効能追加承認を2026年3月23日付で取得しました。本承認は、唾液腺がんに対するホルモン療法として世界初の承認となります。
開発の経緯
希少がん領域では、患者数が限られることから市場規模が小さく、企業が採算性の観点から企業治験に進まない場合があります。そのため、有望な治療戦略であっても開発が停滞することが課題となっています。このような状況において、医師自らが主導して治験を企画・実施する医師主導治験は、未承認薬や適応外薬の有効性・安全性を科学的に検証し、患者さんに新たな治療選択肢を届けるための重要な仕組みです。
唾液腺がんは頭頸部がんの約2~3%を占める希少がんです。数多くの組織型がありますが、唾液腺導管がん(SDC)は進行が速く予後不良な組織型であり、切除不能局所進行または再発・転移した場合には、有効な治療法がまだ十分に確立されていません。
これまで本疾患に対する承認された標準的な全身治療は存在せず、細胞障害性抗がん薬による化学療法が実質的な標準治療とされてきました。しかし、化学療法の奏効率は限定的であり、毒性も強いことから、より有効で安全性の高い分子標的治療の開発が強く求められていました。
SDCの約70~90%でARの発現が認められることから、AR経路阻害は合理的な治療標的と考えられてきました。AR阻害薬とLH-RHアナログ注2を併用するCAB療法は、唾液腺がんにおいて有望な結果が報告されていましたが、承認には至っていませんでした。
ダロルタミドは第2世代の非ステロイド性AR阻害薬であり、ARへの高い結合親和性を有し、血液脳関門への移行が少ない特徴があり、良好な安全性プロファイルが既承認の適応で確認されている薬剤です。前立腺がんにおいては、第III相試験により、LH-RHアナログもしくはLH-RHアナログおよびドセタキセルとの併用で高い有効性と良好な忍容性が示されています。
このように、ダロルタミドを用いたCAB療法はAR経路をより包括的に抑制できる可能性がありますが、唾液腺がんにおいてダロルタミドを前向きに検証した臨床試験はこれまで実施されておらず、AR阻害単剤とCAB療法のいずれが最適な治療戦略であるかは明らかではありませんでした。
本試験は、このような背景のもと、医師が主体となって企画・実施した医師主導治験として行われました。希少がん領域においては、アカデミア主導で科学的根拠を創出し、承認取得へとつなげる取り組みが極めて重要です。
研究の成果
本試験により、ダロルタミド単剤群では有効性が事前に設定した有効性閾値に達しなかったものの、ダロルタミドとゴセレリンを併用するCAB療法は、臨床的意義のある奏効率を示し、無増悪生存期間を改善することが示唆されました。また、長期間にわたり腫瘍縮小が持続する症例も認められました。さらに、治療の忍容性は良好であり、治療期間中の生活の質(QOL)も概ね維持されていました。
これらの結果は、AR経路をより包括的に抑制するCAB療法の有効性を前向き臨床試験で初めて示したものであり、AR陽性唾液腺がんに対する新たな標準治療の確立につながる重要なエビデンスといえます。
展望
本治療の承認により、再発・転移を有する予後不良な患者さんにとって、生活の質(QOL)を維持しながら治療を継続できる期間が延長することが期待されます。さらに、本試験で示された有効性および安全性のデータを基に、AR陽性唾液腺がんに対する標準治療が確立されることが期待されます。
また、AR活性シグネチャーをはじめとする新規バイオマーカーの探索を通じて、より精緻な治療選択を可能とする個別化医療のさらなる発展が見込まれます。
DISCOVARY試験について
DISCOVARY試験(Phase II Study of Darolutamide (ODM-201) in Patients With Androgen Receptor-positive Salivary Gland Carcinoma)は、日本国内12施設で実施された多施設共同単群第II相試験であり、医師主導治験として実施されました。
本治験は、国立がん研究センター東病院頭頸部内科の田原 信科長を治験調整医師代表(Principal Investigator)として実施され、治験調整医師として岡野 晋医長と神戸大学医学部附属病院腫瘍センターの清田 尚臣特命准教授が参画しました。
医師主導治験とは、製薬企業ではなく医師自らが治験を企画・立案し、治験責任医師として試験の科学的妥当性および倫理性を担保しながら実施する臨床試験です。本試験は、日本のGCP(医薬品の臨床試験の実施の基準)およびヘルシンキ宣言に準拠して実施されました。
対象の主な組み入れ規準は、切除不能局所進行または再発・転移AR陽性唾液腺がん、ECOG PS 0–2注3、RECIST v1.1注4に基づく測定可能病変を有すること、十分な臓器機能を有することが条件でした。
本試験はまずダロルタミド単剤コホートを実施し、その後、ダロルタミド+ゴセレリン併用コホートを実施しました。
ダロルタミドは、600mg 1日2回服用し、併用群ではゴセレリン3.6mgの4週毎に皮下注射して、病勢の悪化、忍容できない毒性、同意の撤回、担当医判断などにて治験中止と判断されるまで継続されました。
主要評価項目は、ダロルタミド単剤療法コホートは、担当医評価の奏効割合(ORR)、ダロルタミド+ゴセレリン併用療法コホートは、中央判定によるORRとしました。
臨床試験実施計画・研究概要公開
ClinicalTrials.gov ID NCT05694819
jRCT番号:jRCT2031190241
URL:https://rctportal.mhlw.go.jp/detail/jr?trial_id=jRCT2031190241(外部サイトにリンクします)
URL:https://jrct.mhlw.go.jp/latest-detail/jRCT2031190241(外部サイトにリンクします)
合計57例が登録されました。ダロルタミド単剤コホートに24例(2020年4月–2021年2月)、ダロルタミド+ゴセレリン併用療法コホートに33例(2022年9月–2023年8月)が登録されました。併用療法コホートでは中央判定でAR陽性が確認され、31例が有効性解析集団とされました。
1)単剤療法コホート(n=24)
主要評価項目である奏効割合(ORR)は8.3%(90%信頼区間 1.5–24.0)であり、部分奏効(PR)2例、完全奏効(CR)は認められませんでした。病勢コントロール率(DCR)は54.2%、24週以上の臨床的有益率(CBR)は41.7%でした。無増悪生存期間(PFS)中央値は5.7か月(95%信頼区間 1.9–15.2)でした。全生存期間(OS)中央値は観察期間中央値19.1か月時点で未到達であり、12か月生存率は91.3%(95%信頼区間 69.5–97.8)でした。奏効持続期間(DOR)中央値は14.7か月、臨床的有益持続期間(CBD)中央値は16.4か月でした。データカットオフ時点では全例が治療を終了しており、その主な理由は病勢進行(19例)でした。
2)併用療法(CAB療法)コホート(n=31)
中央判定によるORRは45.2%(90%信頼区間 29.7–61.3)であり、完全奏効1例、部分奏効13例を認め、主要評価項目を達成しました(図1)。
図1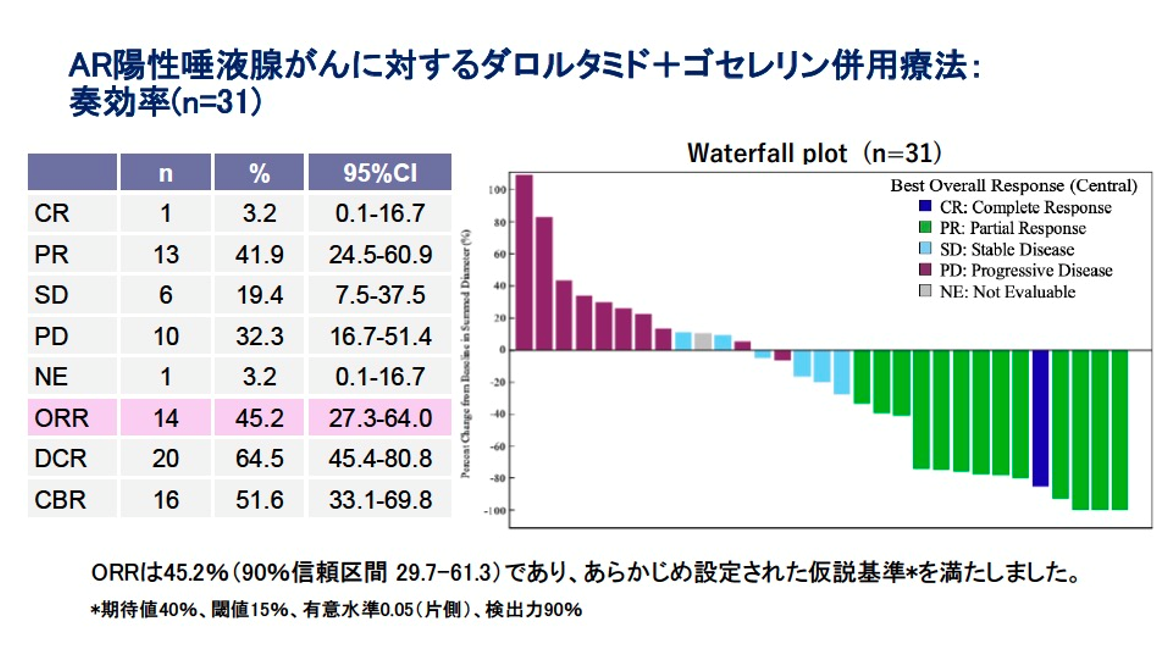
DCRは64.5%、CBRは51.6%と、単剤療法を大きく上回る結果でした。PFS中央値は13.1か月(95%信頼区間 2.0–未到達)で、単剤療法の約2倍の延長を示しました。12か月OS率は87.0%(95%信頼区間 68.9–94.9)でした(図2)。
図2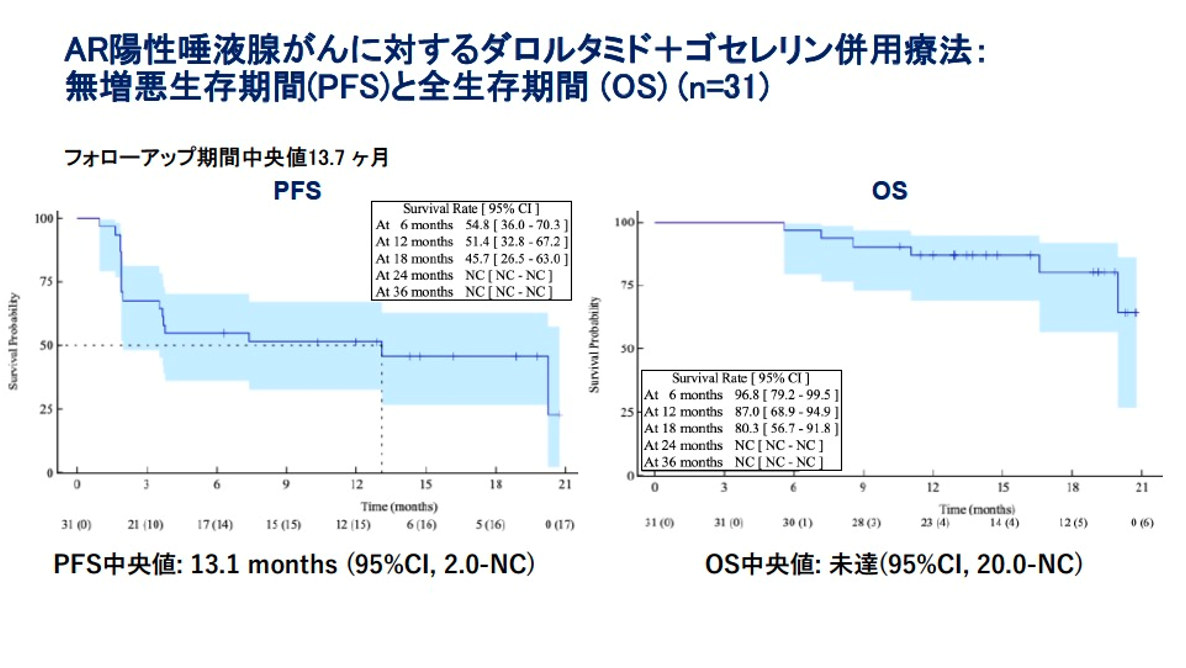
DOR中央値は18.2か月、CBD中央値は20.3か月と、持続的な腫瘍制御が確認されました。データカットオフ時点で13例(39.4%)が治療を継続しており、長期治療が可能であることが示唆されました(図3)。
図3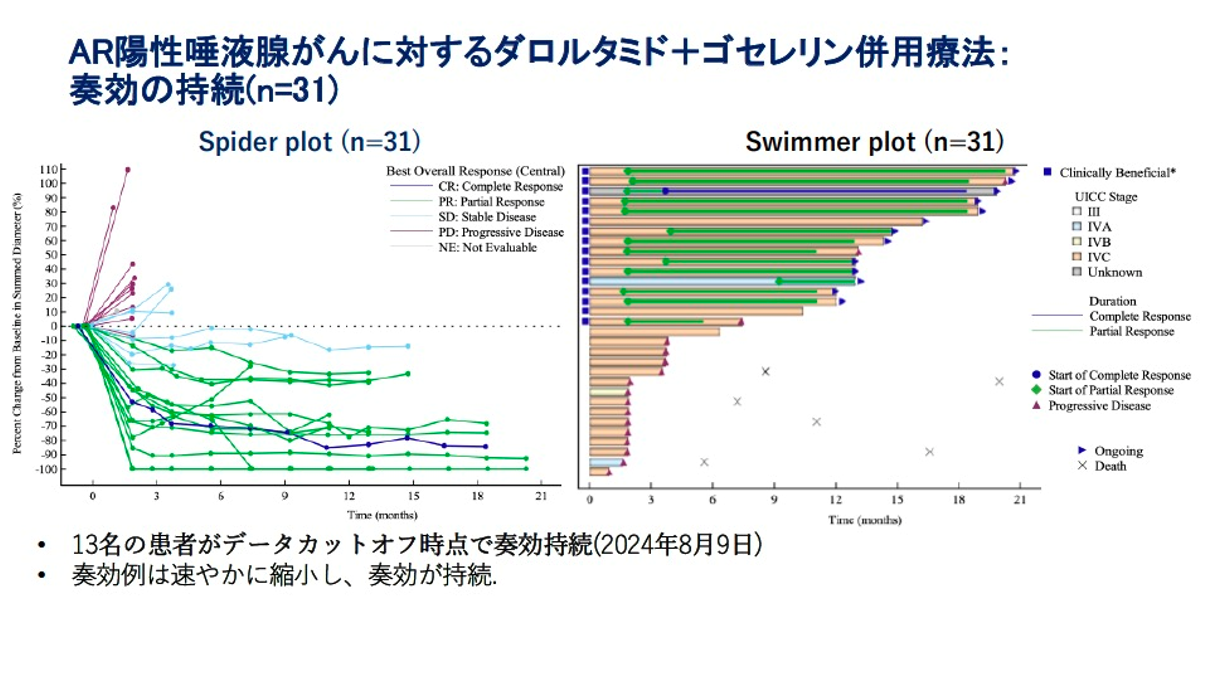
サブグループ解析として、併用療法コホートでは、前治療の有無にかかわらず抗腫瘍効果が認められました。特に、HER2標的治療歴を有する5例のうち3例で部分奏効が得られました。AR発現強度やKi-67指数注5と治療効果との明確な相関は認められませんでした。施設判定と中央判定によるAR陽性判定の一致率は93.9%と高い再現性を示しました。
併用療法の安全性として、Grade3以上の有害事象は18.2%でした。内分泌関連有害事象として倦怠感(9.1%)、ほてり(6.1%)がみられましたが、全体として忍容性は良好でした。重篤有害事象として過敏症、発熱、播種性血管内凝固症候群が報告されましたが、いずれも管理可能であり、Grade4またはGrade5事象は認められませんでした。さらに、生活の質(QOL)の評価として、EQ-5D-5LおよびEQ-VASによる評価を実施したところ、治療期間中に健康関連QOLは概ね維持されました。
学会発表
学会
2025 American Society of Clinical Oncology (ASCO) Annual meeting
タイトル
Darolutamide plus Goserelin for Androgen Receptor-Positive Salivary Gland Cancers:Results of Phase 2 Study (DISCOVARY)
発表者
Susumu Okano
発表日
2025年6月1日
研究費
支援
バイエル薬品株式会社(研究費および薬剤提供)
研究代表者名
田原 信(国立がん研究センター東病院 頭頸部内科 科長)
用語
注1 複合アンドロゲン遮断(Combined Androgen Blockade:CAB)療法
アンドロゲン受容体(AR)を直接阻害する薬剤と、男性ホルモン(アンドロゲン)の産生を抑える薬剤を併用する治療法。がん細胞の中には、男性ホルモンの刺激を受けて増殖するものがあります。CAB療法では、1)アンドロゲン受容体の働きを抑える薬剤(AR阻害薬)、2)男性ホルモンの分泌を抑制する薬剤(LH-RHアナログなど)を同時に用いることで、ホルモン刺激をより包括的に遮断します。
注2 LH-RHアナログ
性ホルモンの分泌を抑える薬です。本試験で用いたゴセレリンはこの種類の薬で、AR阻害剤と併用して男性ホルモンの働きを抑えます。
注3 ECOG PS(全身状態)
日常生活の動ける程度を0~4で示す指標です。PS0~2は「自立して生活でき、治療が検討できる目安」です(0=制限なし、1=軽作業可、2=身の回りの活動は可だが仕事は不可)。
注4 RECIST v1.1
CT/MRIで腫瘍径を同じ条件で測り、消失(CR)、縮小(PR)、不変(SD)、増大/新病変(PD)で治療効果を客観的に判定します。
注5 Ki-67指数
病理検査で「腫瘍(または細胞)がどれくらいの速さで増えようとしているか(増殖の活発さ)」をみる指標です。数値が高いほど、一般に“増え方が活発”と解釈されます。
お問い合わせ先
研究に関するお問い合わせ
国立研究開発法人国立がん研究センター東病院
頭頸部内科
科長 田原 信
電話番号:04-7133-1111(代表)
Eメール:matahara●east.ncc.go.jp
広報窓口
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室(柏キャンパス)
電話番号:04-7133-1111(代表)
Eメール:ncc-admin●ncc.go.jp
国立大学法人神戸大学
総務部広報課
電話番号:078-803-5106
Eメール:ppr-kouhoushitsu●office.kobe-u.ac.jp
