完全切除後のT1膀胱がんに対して無治療経過観察が標準治療の一つとなることを証明~JCOGによる研究成果~
国立研究開発法人国立がん研究センター
国立大学法人筑波大学
国立大学法人富山大学
日本臨床腫瘍研究グループ
発表のポイント
- 膀胱がん(T1膀胱がん)では、2度の内視鏡での診断、治療(TURBT:経尿道的膀胱腫瘍切除術)が行われ、がん細胞の残存が認められない場合は、再発予防の目的でBCG膀胱内注入療法を行うのが標準的治療とみなされてきました。
- T1膀胱がんの5年生存割合は高く9割を超えていますが、術後に行われるBCG膀胱内注入療法は、多くの患者さんで頻尿や排尿痛、血尿など、日常生活に支障のある副作用が生じ、また治療時の苦痛や負担も大きいことから、より低侵襲な治療が求められていました。
- JCOGでは、2度目の内視鏡手術でがん細胞の残存が認められない患者さんを対象に、BCG膀胱内注入療法に対する、無治療経過観察(追加治療を行わず慎重に経過観察を行う)の非劣性を確認するランダム化比較試験を行いました。
- 本試験の結果、無治療経過観察の患者さんの無再発生存期間は、BCG膀胱内注入療法を受けた患者さんに劣らず、副作用も少ない傾向が確認され、無治療経過観察が標準治療の一つとなることが示されました。
- 本試験の成果は、膀胱がん患者さんにおける標準治療に関する知見を示すものとして、医学雑誌「European Urology」に掲載されました。
概要
国立研究開発法人国立がん研究センター中央病院(所在地:東京都中央区、病院長:瀬戸 泰之)が中央支援機構(データセンター/運営事務局)を担い支援する日本臨床腫瘍研究グループ(Japan Clinical Oncology Group:JCOG)では、科学的証拠に基づいて患者さんに第一選択として推奨すべき最善の治療である標準治療や診断方法等を確立するため、専門別研究グループで全国規模の多施設共同臨床試験を実施しています。
この度、JCOG泌尿器科腫瘍グループでは、膀胱の粘膜下までがんが広がっているが筋層までは達していない膀胱がん(以下、T1膀胱がん注1)に対する術後治療の最適化を目的とした、国内多施設によるランダム化比較第III相試験注2を実施しました。
膀胱がんが疑われた場合には、診断と治療を兼ねて内視鏡でのTURBT(経尿道的膀胱腫瘍切除術)が行われ、T1膀胱がんと診断された場合は、がん細胞の残存を確認するため再度TURBT(2nd TUR)が行われます。その後、がん細胞の残存を認めた場合は追加治療を行い、認められない場合は再発予防の目的でBCGという薬剤を膀胱内に注入する治療(BCG膀胱内注入療法注3、以下BCG膀注療法)を行うのが標準治療とみなされ、広く一般診療で行われていました。しかし、この再発予防の目的で行うBCG膀注療法がT1膀胱がん患者さんの生存期間を延長する科学的な根拠は乏しく、また、多くの患者さんで治療による頻尿や排尿痛、血尿など、日常生活に支障のある副作用が生じ、また治療時の患者さんの苦痛や負担も大きいことから、より低侵襲な治療が求められていました。
そこで本試験では、2nd TURでがん細胞の残存を認められなかったT1膀胱がんの患者さんを対象に、術後のBCG膀注療法と、追加治療を行わず慎重に経過観察をする方法(無治療経過観察)を比較し、無再発生存期間注4(がんの再発までの期間)と副作用を評価しました。
本試験の結果、無治療経過観察を行った患者さんの無再発生存期間は、BCG膀注療法を受けた患者さんに比べて劣らないことが示され、生存期間も両群で差は認められませんでした。さらに、無治療経過観察群では副作用もより少ない傾向が示されました。これらの結果から、2nd TURでがんの残存が認められなかったT1膀胱がんの患者さんにおいては、無治療経過観察が標準治療の一つになることが示され、また副作用や治療負担の軽減により、患者さんのQOL(生活の質)の向上にも繋がると考えられます。
本試験の結果は、世界的に権威のある学術雑誌「European Urology」に2026年1月21日付でオンライン先行公開され、2026年5月号に掲載される予定です。
JCOGでは、がん患者さんにとっての最善の医療を確立するための臨床試験を今後も行ってまいります。
背景
膀胱がんは、膀胱粘膜から発生するがんで、最初は粘膜上皮層にとどまりますが(図1のTaの状態)、やがて粘膜より下の層へ進展し(T1の状態)、さらに膀胱壁の深部(T2、T3の状態)へと進展していきます。膀胱がんがどのくらい深くまで進展しているかは、Ta~T4bに分類され、Ta~T1までを筋層非浸潤性膀胱がんと呼びます。T1膀胱がんは、膀胱の粘膜下までは進展しているが筋層までは進展していない状態で、ステージ1ではありますが再発ハイリスクな群に分類され、術後には予防的にBCG膀注療法が標準的な治療法とみなされ広く一般診療で行われています。
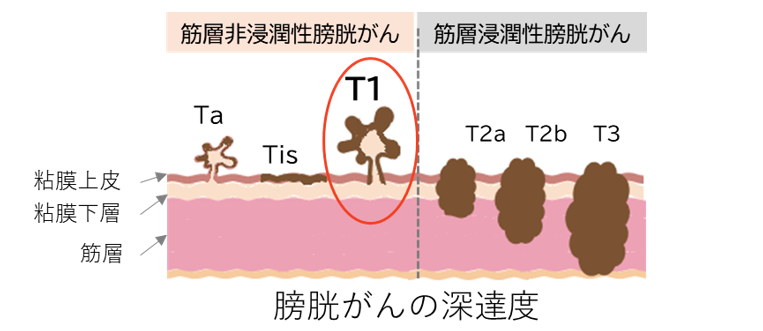 図1 膀胱がんの深達度
図1 膀胱がんの深達度
BCG膀注療法は、がん細胞を攻撃する免疫の力を強めるBCG(ウシ型弱毒結核菌)という薬剤を膀胱内に注入する治療法で、がんが筋層には達していないT1膀胱がんの患者さんに対しては、6~8回(週1回)行われます。一方で、頻尿や排尿時の痛み、発熱などの副作用が起こりやすく、副作用が強く出た場合には、治療を継続することが難しくなることもあります。また、多くは通院で行いますが、尿道から細い管(カテーテル)を通して薬剤を注入し、注入後、薬剤を行き渡らせるために排尿が制限されます。
T1膀胱がんの5年生存割合は9割を超えますが、術後、予防的に行われるBCG膀注療法の副作用により患者さんのQOLが低下することから、より低侵襲な治療が求められており、無治療経過観察がBCG膀注療法に劣らない治療方法であることを確認するための非劣性試験を行いました。
研究方法
TURBT後にT1膀胱がんと診断された患者さんを対象に、標準治療であるBCG膀注療法に対する、無治療経過観察の非劣性を本試験で検証しました。非劣性試験は、新たな治療法と既存治療法を比較し、効果が劣っていない(許容できる範囲内で同程度である)ことを評価する試験です。
本試験への参加(一次登録)後にまず2nd TURを受けていただき、切除された組織の病理学的検査により膀胱がんが完全に切除されていることが確認できた場合に、二次登録へと進みました。二次登録時に、A群(標準治療群:BCG膀注療法)、B群(試験治療群:無治療経過観察)のいずれかにランダム(無作為)に振り分けられました。2011年9月から2018年7月に一次登録された513人のうち、膀胱がんが完全に切除されたことが確認できた263人の患者さんが二次登録されました(A群:133人、B群:130人)。
A群ではBCGを週1回、計8回膀胱内注入を行い、B群では追加治療を行わず慎重に経過観察を行いました。主要評価項目は、無再発生存期間(二次登録日から膀胱内再発も遠隔転移もなく生存している期間)として評価しました。
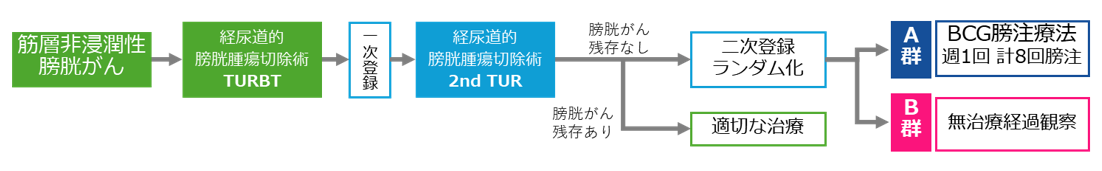 図2 試験の概要(シェーマ図)
図2 試験の概要(シェーマ図)
研究結果
無再発生存期間の評価
主要評価項目である無再発生存期間の評価では、5年時点の無再発生存割合はA群(BCG膀注療法):81.8%に対してB群(無治療経過観察):86.5%で、無治療経過観察の治療成績がBCG膀胱内注入療法に劣らないことが統計学的に示されました[ハザード比(HR)注5=0.69(90%信頼区間0.44-1.08)、p=0.001]。
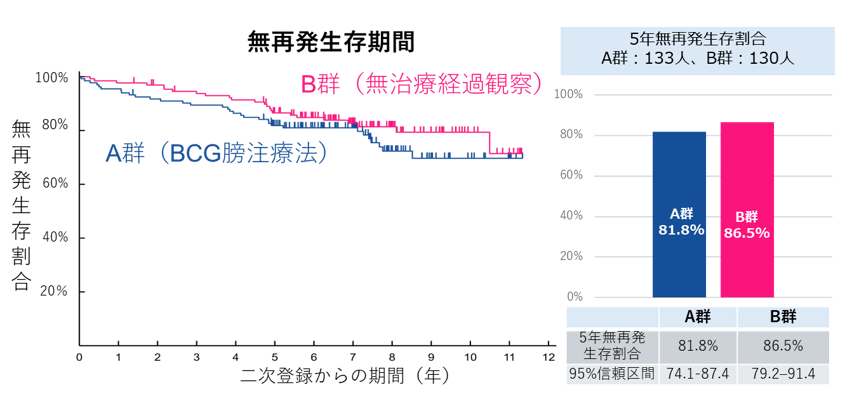 図3 無再発生存期間の結果
図3 無再発生存期間の結果
また、全生存期間(二次登録日から患者さんが生存している期間)の評価では、5年生存割合はA群91.7%、B群92.0%と、同等の治療成績でした。
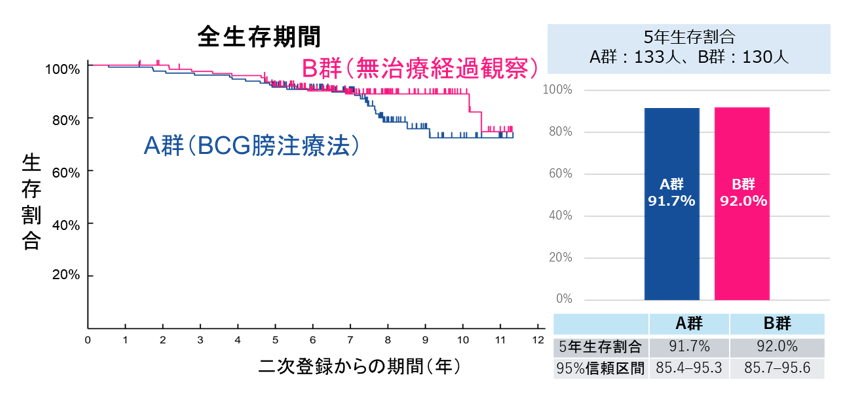 図4 全生存期間の結果
図4 全生存期間の結果
副作用の評価
BCG膀注療法で生じる主な副作用において、生活に支障のある重症度に当たるグレード2*以上の割合を評価しました。
その結果、血尿や頻尿、尿路痛といったBCG膀胱内注入療法に関連するグレード2以上の副作用は、無治療経過観察で少ない傾向であることが示されました。
*グレード2:中等症; 最小限/局所的/非侵襲的治療を要する; 年齢相応の身の回り以外の日常生活動作の制限。身の回り以外の日常生活動作とは、食事の準備、日用品や衣服の買い物、電話の使用、金銭の管理などをさす。
主な副作用(グレード2以上の副作用)
|
|
A群(BCG膀注療法) 133人 |
B群(無治療経過観察) 130人 |
|
血尿 |
8人(6.0%) |
3人(2.3%) |
|
頻尿 |
7人(5.3%) |
4人(3.1%) |
|
尿路痛 |
8人(6.0%) |
1人(0.8%) |
|
尿路障害 |
2人(1.5%) |
3人(2.3%) |
図5 主な副作用の結果
展望
本試験の結果、TURBT後の2nd TURでがんの残存が認められなかったT1膀胱がん患者さんにおいては、無治療経過観察でも無再発生存期間が劣らなかったことから、無治療経過観察が標準治療の一つになることが示されました。無治療経過観察にはBCG膀注療法の通院、副作用、費用などの負担がありません。今後は、これまで以上に膀胱がん患者さんのさまざまな希望や状況に応じた医療を提供できるようになり、QOL(生活の質)の向上にも繋がると考えられます。
本試験の詳細
試験名
High grade T1注6膀胱癌のsecond TUR後T0患者に対するBCG膀胱内注入療法と無治療経過観察のランダム化第III相試験(JCOG1019)
患者さんの登録時期
2011年9月22日~2018年7月13日
登録人数
513名
年齢中央値
69歳
研究の実施体制
JCOG泌尿器科腫瘍グループ代表:北村 寛(富山大学学術研究部医学系)
JCOG1019研究代表者:西山 博之(筑波大学医学医療系)
JCOG1019研究事務局:北村 寛(富山大学学術研究部医学系)
JCOG中央支援機関(データセンター/運営事務局):福田 治彦、片山 宏(国立がん研究センター)
目的
治療目的のTURBTで初めて病理組織学的にT1膀胱がんと診断され、2nd TURで病理組織学的に腫瘍を認めなかった膀胱がん患者さんを対象として、補助治療としてBCG膀胱内注入療法(BCG膀注療法)を実施する群 (A群)に対して、無治療経過観察群 (B群) が、「無再発生存期間(ただし、Tis、Ta膀胱内再発を除く)」において非劣性であることを検証する。
対象
一次登録適格規準
- TURBT において内視鏡肉眼所見で腫瘍が完全切除され、病理診断でHigh grade T1 膀胱癌と診断されている
- 年齢が20歳以上、85歳以下
- 骨盤部への放射線治療の既往がない
- 適切な臓器機能を有する
- 試験参加について本人から同意が得られている
二次登録適格規準
- 2nd TUR標本の病理組織診断にて腫瘍を認めない
- 尿細胞診で2回続けて陰性、疑陽性のいずれかと診断されている
- リンパ節転移および遠隔転移がない
- 適切な臓器機能を有する
評価項目
主要評価項目:無再発生存期間
副次的評価項目:全生存期間、無転移膀胱温存生存期間、年次膀胱内非再発生存割合、有害事象発生割合など
実施施設
国内43施設
UMIN臨床試験登録システム
https://center6.umin.ac.jp/cgi-open-bin/ctr/ctr_view.cgi?recptno=R000007297&language=J(外部サイトにリンクします)
論文情報
雑誌名
European Urology
タイトル
Active Surveillance Versus Intravesical Bacillus Calmette-Guérin for High-grade T1 Bladder Cancer with Negative Second Transurethral Resection: The Randomized Noninferiority Phase 3 JCOG1019 Trial
著者
Hiroshi Kitamura, Taiji Tsukamoto, Yoshiyuki Kakehi, Junki Mizusawa, Taro Shibata, Keita Sasaki, Toshiki Tanikawa, Katsuyoshi Hashine, Kiyohide Fujimoto, Naoya Masumori, Takashi Kobayashi, Tomonori Habuchi, Takahiro Kimura, Mikio Sugimoto, Atsushi Takahashi, Hisanobu Adachi, Yoshiyuki Matsui, Shingo Hatakeyama, Akihiro Ito, Masatoshi Eto, Hiroyuki Nishiyama, on behalf of the JCOG 1019 investigators
DOI
10.1016/j.eururo.2026.01.008
掲載日
2026年5月号(オンライン2026年1月21日)
URL
https://doi.org/10.1016/j.eururo.2026.01.008
研究費
- 厚生労働科学研究費補助金
がん臨床研究事業
高悪性度筋層非浸潤癌に対する経尿道的膀胱腫瘍切除術後の治療方針の確立に関する研究
塚本 泰司(札幌医科大学) - 国立がん研究センター研究開発費
革新的がん医療実用化研究事業成人固形がんに対する標準治療確立のための基盤研究
大江 裕一郎(国立がん研究センター中央病院(申請当時))
日本臨床腫瘍研究グループ(JCOG:Japan Clinical Oncology Group)の概要
国立がん研究センター研究開発費、日本医療研究開発機構研究費を主体とする公的研究費によって助成される研究班を中心とする多施設共同臨床研究グループで、がん診療連携拠点病院を中心とした医療機関の研究者で構成される専門分野別研究グループと国立がん研究センターが管轄する中央支援機構(国立がん研究センター中央病院臨床研究支援部門)、各種委員会から構成されており、法人格を有さない任意団体です。
JCOGウェブサイト: http://www.jcog.jp/index.html(外部サイトにリンクします)
用語解説
注1 T1膀胱がん
がんが筋層まで及んでいない状態の膀胱がん(Ta、Tis、T1)のことです。本試験では、T1と診断され、リンパ節や他の臓器への転移がない方(T1N0M0)を対象としています。なお、ステージは、TNMの3種のカテゴリー(TNM分類)の組み合わせで決まります。Tカテゴリーは、原発腫瘍(がんが初めに発生した部位)にあるがん)の深達度を指し、がんがどのくらい深くまで及んでいるかを示しています。
注2 ランダム化比較第III相試験
登録された患者さんをランダムに各治療群に割り付け治療成績を比較する、検証的な臨床試験のことです。
注3 BCG膀胱内注入
結核予防のためのワクチン(ウシ型弱毒結核菌)として使用されるBCGを膀胱内に注入する治療法です。膀胱がんの治療として、標準的には、TURBT後に6~8回注入するBCG導入療法と、その後1~3年間継続投与するBCG維持療法があり、リスクなどによって注入の回数や時期を判断します。細胞傷害性抗がん薬の注入療法よりも高い治療効果が期待できる反面、副作用が出やすい治療法で、副作用が強く出た場合には、治療を継続することが難しくなることもあります。
注4 無再発生存期間
この試験の二次登録日から、患者さんが再発なく生存している期間のことです。
注5 ハザード比(HR)
ある治療を行った場合に、一定期間に起こる出来事(本試験でいうと死亡)の「起こりやすさ」を別の治療と比べた数値のことです。数値が低い程、起こる確率が低いことになります。本試験では、「無治療経過観察がBCG膀注療法よりも劣っていない」と判断できる規準をハザード比で1.60と予め決めていました。実際の結果を統計的に解析したところ、信頼区間上限がその規準を超えなかったため、無治療経過観察がBCG膀注療法と比べて劣っていないと証明されました。
注6 High grade T1
筋肉までは達していないものの(T1)、がん細胞の悪性度が高い(High grade)タイプの膀胱がんのことです。
お問い合わせ先
研究に関するお問い合わせ
国立大学法人富山大学
学術研究部医学系 腎泌尿器科学 教授 北村 寛
電話番号:076-434-7372
Eメール:urology●med.u-toyama.ac.jp
国立研究開発法人国立がん研究センター中央病院
臨床研究支援部門 研究企画推進部 多施設研究支援室(JCOG運営事務局)
Eメール:webmaster●ml.jcog.jp
広報窓口
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室
電話番号:03-3542-2511(代表)
Eメール:ncc-admin●ncc.go.jp
筑波大学
広報局
電話番号:029-853-2040
Eメール:kohositu●un.tsukuba.ac.jp
国立大学法人富山大学
総務部総務課広報・基金室
電話番号:076-445-6028
Eメール:kouhou●u-toyama.ac.jp
関連ファイル
関連リンク
- 中央病院 泌尿器・後腹膜腫瘍科
- 中央病院 臨床研究支援部門
- JCOG (外部サイトにリンクします)
