クローディン18.2陽性HER2陰性進行胃がんに対するゾルベツキシマブ+化学療法+ニボルマブ併用療法が有効な可能性
2026年3月19日
国立研究開発法人国立がん研究センター
発表のポイント
- 本研究は、クローディン18.2 (以下CLDN18.2) 陽性かつHER2陰性の切除不能または転移性胃・食道接合部・食道腺がん (以下胃がん)に対し、CLDN18.2標的IgG1抗体であるゾルベツキシマブと抗PD-1抗体ニボルマブと化学療法併用の有効性・安全性を検討する第II相試験です。
- 無増悪生存期間の中央値は14.8か月であり、特にCLDN18.2高発現症例では18.0か月、さらにCLDN18.2高発現かつPD-L1 CPS ≥1症例では23.6か月と有望な結果が確認されました。
- 奏効割合は、全体で62.1%、CLDN18.2高発現では68.1%, CLDN18.2高発現かつCPS ≥1症例では74.2%でした。
- 安全性については、ゾルベツキシマブに伴う悪心・嘔吐、ニボルマブに関連する免疫関連有害事象、化学療法による骨髄抑制などを認めましたが、概ねこれまでの各薬剤に関する報告から想定される範囲内でした。
- これらの結果は、CLDN18.2とPD-L1という二重バイオマーカーに基づく併用療法の臨床的意義を示唆するものであり、進行中の第III相試験であるLUCERNA試験 (NCT06901531) を支持すると考えられます。
- 本研究は、国際共同第II相試験においてCLDN18.2陽性胃がんに対する新たな一次治療選択肢を検討した意義が評価され2026年3月16日に科学雑誌「Nature Medicine」に掲載されました。
概要
国立研究開発法人国立がん研究センター(理事長:間野 博行、東京都中央区)東病院(病院長:土井 俊彦、千葉県柏市)設楽 紘平消化管内科長らの研究グループは、CLDN18.2発現を認める(IHC3+もしくはIHC2+の腫瘍細胞が50%以上)注1切除不能または転移性胃・食道接合部・食道腺がん(以下胃がん)に対する一次治療として、抗CLDN18.2標的抗体であるゾルベツキシマブ注2 と抗PD-1抗体ニボルマブ注3、化学療法の併用の有効性と安全性を検証するための国際共同第II相・多コホート試験「ILUSTRO試験」を実施しました。本試験のコホート4では、CLDN18.2発現を認めるHER2陰性の切除不能または転移性胃がんに対する治療として、ゾルベツキシマブ、ニボルマブと化学療法として5-FU, oxaliplatinの併用(FOLFOX療法)が2週間毎に投与されました。その結果、無増悪生存期間の中央値は14.8か月であり、特にCLDN18.2高発現症例(IHC3+もしくはIHC2+の腫瘍細胞が75%以上) では18.0か月、さらにCLDN18.2高発現かつPD-L1 CPS ≥1注4症例では23.6か月と有望な結果が確認されました。安全性については、それぞれの薬剤に関連する副作用が認められたものの、新たな安全性上の懸念は確認されませんでした。
本研究は、CLDN18.2陽性胃がんに対する新たな一次治療選択肢を検討した意義が評価され2026年3月16日に科学雑誌「Nature Medicine」に掲載されました。
背景
切除不能または転移性胃がんは世界的に依然として予後不良な疾患ですが、近年はPD-L1、HER2、CLDN18.2などのバイオマーカーに基づく治療の選択により転帰が徐々に改善してきました。CLDN18.2は胃粘膜由来のタイトジャンクション蛋白で、腫瘍化に伴う構造変化により細胞表面へ露出し、治療抗体の標的となり得ます。胃がんのおよそ40%程度がCLDN18.2陽性と報告されています。
ゾルベツキシマブはCLDN18.2を標的とし、抗体依存性細胞傷害(ADCC)および補体依存性細胞傷害(CDC)を介して腫瘍細胞死を誘導します。先行する国際共同第III相試験であるSPOTLIGHT試験およびGLOW試験注5では、CLDN18.2陽性胃がんに対する一次治療としてゾルベツキシマブ+化学療法が化学療法単独に対して無増悪生存期間と生存期間を有意に改善しました (https://www.ncc.go.jp/jp/information/researchtopics/2024/0918/index.html)。一方で、胃がんにおいては化学療法と免疫チェックポイント阻害剤の併用療法の有効性も示されてきました。非臨床における検討では、ゾルベツキシマブ+化学療法+PD-1阻害の3剤併用療法は、いずれの2剤併用よりも強い抗腫瘍効果を示していました。また、ゾルベツキシマブ投与前後の臨床検体解析においてCD8陽性T細胞やマクロファージの増加といった腫瘍免疫微小環境の変化が示唆され、ゾルベツキシマブ+化学療法+PD-1阻害による併用療法を検討する意義が示唆されました。これらの結果を背景として、ゾルベツキシマブ・ニボルマブ・化学療法の併用療法を検討したのが本ILUSTRO試験(コホート4)です。
研究成果(方法・結果)
ILUSTRO試験のコホート4は、2つのコホート、すなわち4A(安全性導入期)および4B(拡大期)から構成され、標準投与量であるゾルベツキシマブ800mg/m²の導入投与と400mg/m²の維持投与を受けた患者は77例(コホート4A:6例、コホート4B:71例)でした。CLDN18.2の免疫染色の結果を有する76例中、65例(85.5%)がCLDN18.2高発現(腫瘍細胞の75%以上に中等度~強陽性膜染色)、11例(14.5%)が中等度発現(50%以上75%未満)でした。また、PD-L1評価可能な75例中、CPS <1が34.7%、CPS ≥1が65.3%でした。データ解析時点で、22例(28.6%)がゾルベツキシマブ継続中でした。
有効性解析の主要コホートであるコホート4Bの71例における無増悪生存期間の中央値は14.8か月(95%信頼区間:8.3–推定不能)でした(図1A)。6か月および12か月時点の、無増悪生存期間割合は、それぞれ72.6%および59.1%でした。CLDN18.2発現別の解析では、高発現群(n=59)の、無増悪生存期間中央値は18.0か月(95%信頼区間:11.1–推定不能)であり、95%信頼区間の下限は事前規定閾値として設定された8.5か月を上回っていたため、本治療の有効性が統計的観点から示唆されました(図1B)。また、CLDN18.2高発現かつPD-L1 CPS ≥1(n=36)では、PFS中央値は23.6か月でありCPS <1(n=21)では12.1か月でした(図1C)。
図1A. コホート4Bにおける無増悪生存期間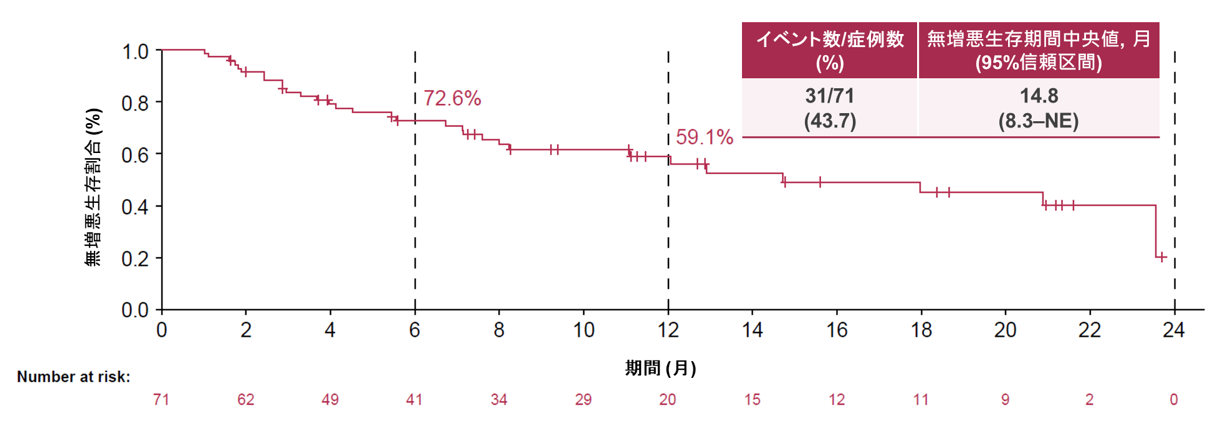
図1B. CLDN18.2発現別の無増悪生存期間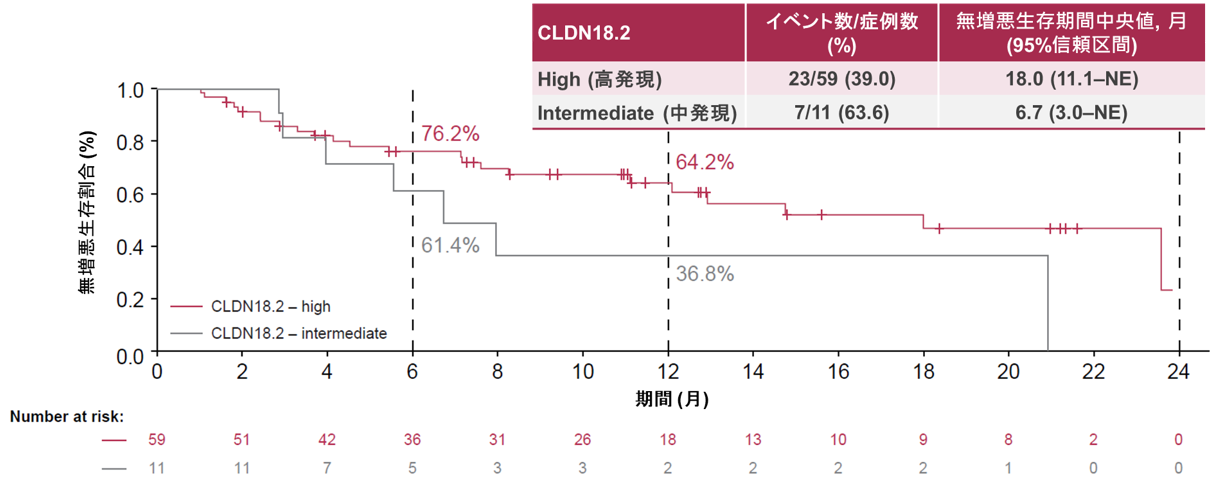
図1C. CLDN18.2高発現例におけるCPS別の無増悪生存期間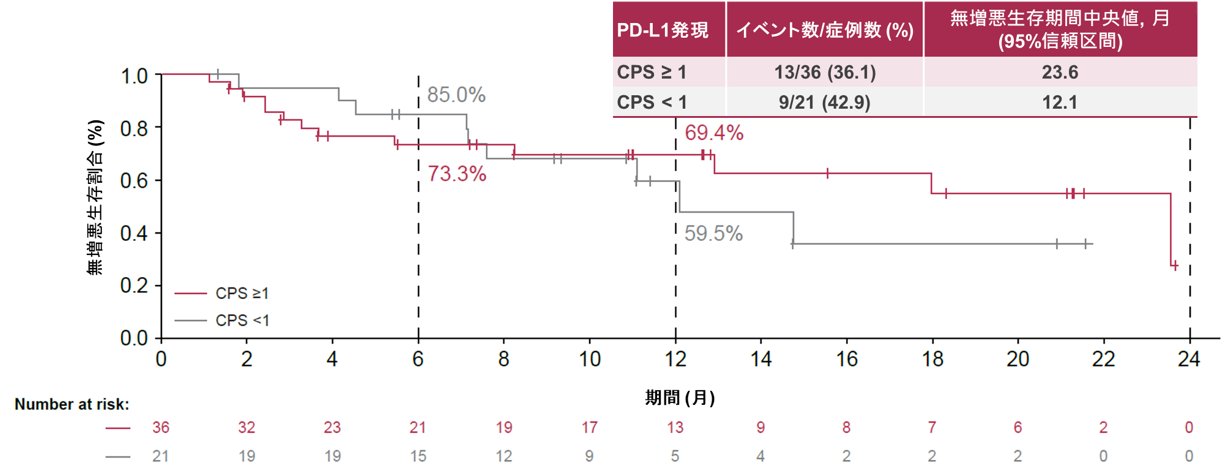
全生存期間は解析時点では未成熟であり、コホート4Bの71例中25例(35.2%)のみが死亡していました。追跡期間中央値15.4か月時点で、全生存期間の中央値は全体集団で18.0か月であり、CLDN18.2高発現群では未到達(95%信頼区間13.7–推定不能)でした。
測定可能病変を有する症例における腫瘍縮小割合については図2に示されており、コホート4B患者(n=58)における客観的奏効割合は62.1%でした。CLDN18.2高発現例(n=47)の奏効割合は68.1%、中等度発現例(n=10)では40.0%でした。さらに、CLDN18.2高発現かつPD-L1 CPS ≥1(n=31)ではORR 74.2%、CPS <1(n=15)では60.0%と、いずれも陽性の集団で高い奏効割合が示されました。
図2. 測定可能病変を有する症例における奏効割合・腫瘍縮小効果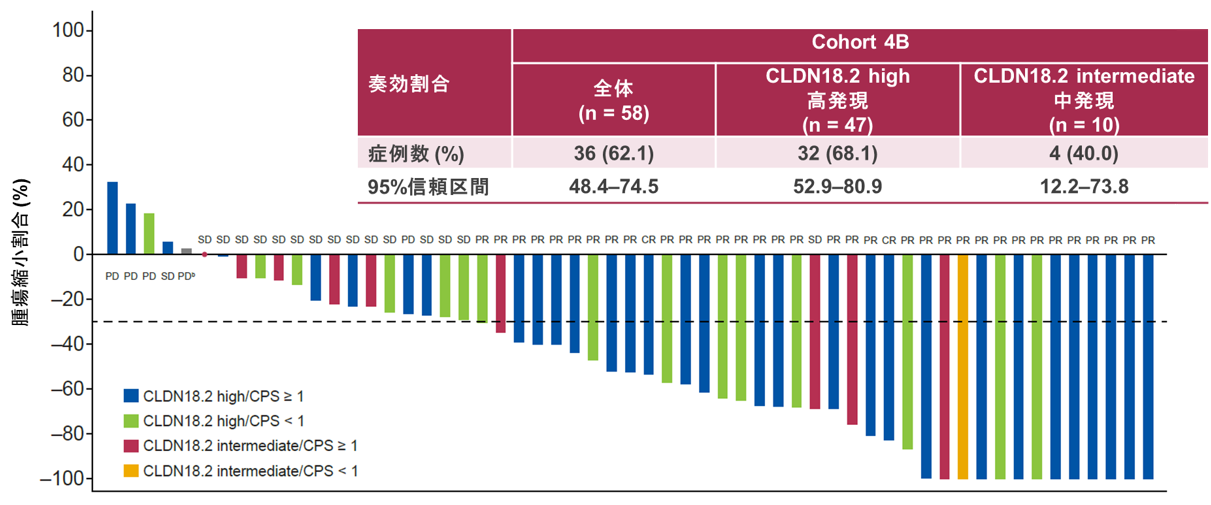
治療効果は概ね持続的であり、測定可能病変を有するコホート4B患者の奏効持続期間中央値は19.1か月(95%信頼区間10.8–推定不能)でした。
最も頻度の高い有害事象は、悪心(80.5%)、食欲低下(72.7%)、好中球減少(45.5%)、末梢感覚神経障害(45.5%)、嘔吐(37.7%)でした。高グレード 注6の消化器毒性は比較的少なく、グレード3以上の嘔吐は3.9%、グレード3以上の悪心は報告されませんでした。免疫関連事象は9.1%に認められました。有害事象によるゾルベツキシマブの中止は5.2%、ニボルマブ中止は7.8%に認められました。これらの頻度はこれまでの化学療法とゾルベツキシマブの併用や化学療法とニボルマブの併用における既知の安全性プロファイルと概ね一致していました。
展望
本研究は、CLDN18.2陽性かつHER2陰性の胃・食道接合部腺がんの一次治療において、化学療法とゾルベツキシマブ・ニボルマブの併用が良好な無増悪生存期間を示し、特にCLDN18.2高発現(75%以上)かつPD-L1陽性 (CPS ≥1)においてその有効性が高い可能性が示唆されました。現在国際共同第III相であるLUCERNA試験(NCT06901531)において、CLDN18.2高発現かつPD-L1陽性胃がんに対する化学療法・ゾルベツキシマブ・PD-1抗体(ペムブロリズマブ)と、化学療法・PD-1抗体の併用療法が比較されています (https://ascopubs.org/doi/10.1200/JCO.2026.44.2_suppl.TPS473(外部サイトにリンクします))。ILUSTRO試験の結果は、その科学的・臨床的根拠を提供するものであり、LUCERNA試験の結果によって、バイオマーカー注7に基づく胃がんの新たな標準治療となり得ることが期待されます。
論文情報
雑誌名
Nature Medicine
タイトル
First-line zolbetuximab plus mFOLFOX6 and nivolumab in unresectable CLDN18.2-positive gastric or gastroesophageal junction adenocarcinoma: a phase 2 trial
著者
Kohei Shitara, Hirokazu Shoji, Nicola Fazio, Sara Lonardi, Keun-Wook Lee, Li-Yuan Bai, Kensei Yamaguchi, Jean-Philippe Metges, Gianluca Masi, Denis Smith, Tae-Yong Kim, Maria Matsangou, Archita Shrivastava, Miaomai Zhou, Jason Hill, Abraham Guerrero, Xuewei Wang, Aziz Zaanan & Samuel J. Klempner
DOI
s41591-026-04306-9
掲載日
2026年3月16日
URL
https://www.nature.com/articles/s41591-026-04306-9(外部サイトにリンクします)研究費
研究費名(支援先)
Astellas Pharma Inc.
研究課題名
クローディン(CLDN)18.2陽性の転移性又は局所進行性切除不能の胃腺癌又は食道胃接合部(GEJ)腺癌、 及び局所胃腺癌又はGEJ腺癌患者を対象とした、ゾルベツキシマブ(IMAB362)の単剤療法、及び化学療法 及び/又は免疫療法との併用療法を評価する第2相試験
研究代表者名
Astellas Pharma Inc.
用語解説
注1 クローディン18.2 (Claudin 18 isoform 2, CLDN18.2)
細胞接着に関わる膜貫通型の蛋白であり、正常の胃粘膜に発現していますが、胃がんにおいても約40%で陽性例が認められます。胃がんでは腫瘍化に伴う極性破綻により細胞表面に露出し、治療標的となり得ます。ゾルベツキシマブ投与の適応判定基準では、免疫染色でクローディン18.2蛋白発現を判定し、中等度から強い染色を75%以上の腫瘍細胞の細胞膜に認める場合を示しますが、本ILUSTRO試験では50%以上の腫瘍細胞で陽性の患者さんが参加可能と設定されました。
注2 ゾルベツキシマブ
クローディン18.2 に対するキメラIgG1モノクローナル抗体のこと。二つの第III相試験の結果に基づき、クローディン18.2陽性の治癒切除不能な進行・再発の胃がんを効能・効果として日本における製造販売承認が得られています。
注3 ニボルマブ
プログラム細胞死1(PD-1)受容体を標的とする免疫チェックポイント阻害抗体。
注4 PD-L1(CPS)
PD-L1のCPS(Combined Positive Score)は、がん細胞だけでなく、周囲の免疫細胞(リンパ球、マクロファージ)におけるPD-L1タンパク質の発現を免疫染色検査で評価する指標です。
注5 SPOTLIGHT試験とGLOW試験
いずれもゾルベツキシマブと化学療法の有効性・安全性をプラセボと化学療法を比較した第III相試験です。SPOTLIGHT試験では化学療法としてmFOLFOX6療法(フルオロウラシルとレボホリナートにオキサリプラチンを併用する)が用いられ、GLOW試験ではCapeOX療法(カペシタビンにオキサリプラチンを併用する)が用いられました。いずれも全世界の国々で実施されましたが、国別の患者登録数の差異がありました。特にGLOW 試験では中国からの患者数が29%と多くを占めました。いずれの試験にも日本からの患者さんが参加されています。結果として、両試験において主要評価項目である無増悪生存期間の有意な延長と、中間解析時点における全生存期間の有意な改善を認めました。両試験において、併用による悪心・嘔吐の増加を認めましたが、これらの有害事象は初回投与時に多く発生し、その後の投与時には頻度が明らかに減少することが確認されています。(https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(23)00620-7/abstract)(外部サイトにリンクします) (https://www.nature.com/articles/s41591-023-02465-7)(外部サイトにリンクします)
注6 グレード
副作用はCTCAE(Common Terminology Criteria for Adverse Events)の規準に従って判断される。これは、がん治療や薬剤使用による有害事象の重症度を評価するための国際的に用いられる基準である。グレード1から5までの5段階で分類され、グレードが高いほど重症度が高いことを示す。
注7 バイオマーカー
ある疾患の有無や、病状の変化・進行・治療効果などで指標となる項目(血圧、心拍数、心電図、認知機能テストなど)及び生体内の物質(タンパク質、代謝物や遺伝子など)を指す。
お問い合わせ先
- 研究に関するお問い合わせ
国立研究開発法人国立がん研究センター東病院
消化管内科 設楽 紘平
電話番号:04-7133-1111(代表)
Eメール:kshitara●east.ncc.go.jp - 広報窓口
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室(柏キャンパス)
電話番号:04-7133-1111(代表)
Eメール:ncc-admin●ncc.go.jp
