“痛み”ががん病態に関与する可能性を報告–痛みを伝える“知覚神経”から放出される物質が乳がんの進行を促す仕組みを解明–
星薬科大学
国立研究開発法人国立がん研究センター
星薬科大学 薬学部 薬理学研究室の成田年教授、葛巻直子准教授らの研究グループは、国立がん研究センター研究所 がん患者病態生理研究ユニットの南雲康行ユニット長、同研究所 先端バイオイメージング研究分野の鈴木健一分野長および笠井倫志ユニット長、国立がん研究センター中央病院 緩和医療科の里見絵理子科長らとの共同研究により、「がんによる痛み」が、単なる随伴症状ではなく、腫瘍進行そのものを加速させる生物学的因子である可能性を、乳がん患者さんを対象とした観察研究、ヒトiPS細胞由来知覚神経モデルおよび動物モデルを組み合わせて明らかにしました。この成果は2月9日に国際学術誌 (Elsevier 刊行) 『Pharmacological Research』 にオンライン公開されました。
研究成果のポイント
- 乳がん患者さんにおいて、痛みの強さと病状の進行が相関している可能性があることを後ろ向きの観察研究で確認しました。
- 痛みを感じる神経から放出される物質である CGRPおよびサブスタンスP注1の血中濃度は疼痛スコアと正の相関を示し、全生存期間と負の相関を示しました。
- ヒト iPS 細胞由来知覚神経を光刺激で活性化すると、知覚神経と共存する乳がん細胞の増殖・転移能・薬剤耐性が顕著に増強されました。
- 動物モデルでは、CGRP受容体および NK1 受容体遮断により、知覚神経活性化に伴う腫瘍進行が抑制されました。
- 一方で、知覚神経由来で痛みを抑える物質ダイノルフィン注2はκオピオイド受容体を介して腫瘍進行を抑制しました。
- 今後は知覚神経ペプチド遮断あるいはκ オピオイド受容体作動薬に既存の抗がん剤や鎮痛薬を適切に組み合わせることで、腫瘍抑制と疼痛管理を同時に最適化する新たながん治療・がん支持療法につながることが期待されます。
概要
星薬科大学 薬理学研究室の成田年教授 (責任著者)、葛巻直子准教授 (共責任著者) らは、国立がん研究センター研究所 がん患者病態生理研究ユニットの南雲康行ユニット長、同研究所 先端バイオイメージング研究分野の鈴木健一分野長および笠井倫志ユニット長、国立がん研究センター中央病院 緩和医療科の里見絵理子科長らとの共同研究により、腫瘍周囲の知覚神経から放出される物質である神経ペプチドを介して、痛みのシグナルが腫瘍微小環境に作用し、腫瘍進行に関与し得る「神経–腫瘍相互作用」という病態がある可能性を明らかにしました。
がん関連疼痛(がんが引き起こす痛み)は患者さんの生活の質を著しく低下させる主要な症状として知られていますが、腫瘍進行を駆動する病態としては十分に理解されていませんでした。本研究では、疼痛自体が腫瘍の進行と関連するという新しい視点が提示されました。
乳がん患者さんを対象とした観察研究では、専門的緩和ケア介入後も疼痛が持続する患者さんでは、神経伝達物質であるカルシトニン遺伝子関連ペプチド (calcitonin gene-related peptide: CGRP) およびサブスタンス P の血中濃度が高く、血中濃度が高いと生存期間は短くなっていました。すなわち、疼痛の強度と神経ペプチド濃度は、患者さんの生存期間と関係する可能性が明らかになりました。
その仕組みを解明するために、ヒト iPS 細胞から分化誘導した知覚神経に光を当てることでその活動を制御できるようにしたモデルを構築しました。このモデルにより、光を当てて痛みを感じる神経を活動させると、CGRPおよびサブスタンスPが大量に放出されました。これらの神経から放出された物質を含む培養液を乳がん細胞にかけると、がん細胞を増殖させるPI3K–Akt シグナルが活性化し、細胞増殖、遊走能、抗がん剤抵抗性が著しく増強されました。
動物モデルにおいても、知覚神経が光で活動するようにしました。腫瘍周囲の知覚神経を光で刺激すると腫瘍増殖が加速し、この効果は CGRP受容体拮抗薬および NK1 受容体 (サブスタンス P 受容体) 拮抗薬の併用により完全に抑制されました。さらに患者さんの状態をよく反映する患者由来腫瘍移植 (PDX) モデル注3においても同様の傾向が確認されました。
興味深いことに、本研究では知覚神経が腫瘍促進因子だけでなく、腫瘍抑制因子も同時に放出していることが明らかになりました。知覚神経由来で痛みを抑えるダイノルフィンは κ オピオイド受容体 (KOR) を介して PI3K–Akt 活性化を抑制し、腫瘍進行を減弱させました。さらに、末梢選択的 KOR 作動薬によって腫瘍増殖が抑制されることも示され、神経系は腫瘍に対してアクセルとブレーキの両方を内在している可能性を示しました (研究概要図参照)。
本成果は、2026年2月9日に国際学術誌 (Elsevier 刊行) 『Pharmacological Research』 にオンライン公開されました。
<研究概要図>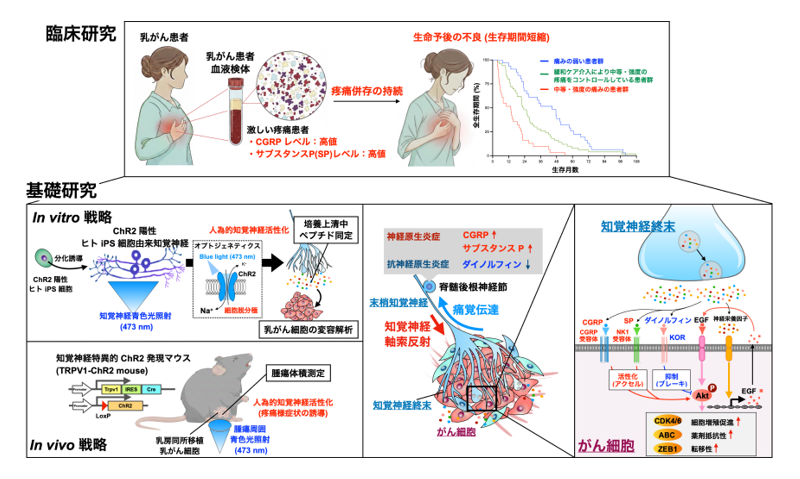
研究の背景
乳がんは女性で最も頻度の高い悪性腫瘍の一つであり、ホルモン受容体や HER2 の状態に基づく分子サブタイプにより、治療戦略、再発リスク、全生存期間(生存予後)が大きく異なります。とりわけ、再発・転移や薬剤抵抗性は依然として主要な臨床課題であり、腫瘍細胞そのものに加えて腫瘍微小環境を規定する要素の理解が重要になっています。近年、乳がん組織では正常乳腺に比べて知覚神経線維の密度が高いこと、さらに腫瘍内神経線維の存在や太さなどの神経関連所見が転移や生存予後と関連することが報告され、腫瘍微小環境における「神経」の位置づけが注目されています。
痛み刺激は末梢から中枢へ伝達される一方、末梢では知覚神経終末の軸索反射により CGRPやサブスタンスPが放出されます。これらの神経ペプチドは、神経―免疫のクロストークを介して神経原性炎症を引き起こし、局所環境を動的に変化させます。がん関連疼痛が生存予後と関連することは示されているものの、疼痛に伴う末梢神経シグナルが、どの分子経路を介して腫瘍進行や治療抵抗性へ結び付くのかは十分に整理されていません。特に、腫瘍微小環境に放出される CGRPおよびサブスタンスPがどの程度協調して腫瘍側の性質を変化させるのか、また、CGRPおよびサブスタンスPとは逆向きに腫瘍進行へ“ブレーキ”をかける内因性の拮抗的調節 (counter-regulation) が同じ神経系に備わっているのかは、検証課題として残っています。
本研究では、ヒト iPS 細胞由来知覚神経モデルを用いて疼痛様シグナルに伴う神経ペプチド放出と乳がん細胞への影響を評価するとともに、疼痛を有する乳がん患者さんの後ろ向き観察研究で血中 CGRPおよびサブスタンスPを測定し、その臨床的意義を解析しました。
本研究の成果
1.観察研究: 疼痛の改善度と血中 CGRPおよびサブスタンスPは、生存予後と相関する
国立がん研究センター中央病院に受診した乳がん患者さんを対象として、単施設後ろ向き観察研究により専門的緩和ケア介入前後の疼痛スコアの変化と生存率を解析しました。その結果、介入後にも続く強い疼痛と生存予後の間に相関があることを見出しました。さらに、循環血中の神経ペプチドである CGRPおよびサブスタンスP 濃度は、疼痛スコアの高さと正の相関を示す一方で、疼痛スコアおよび CGRPおよびサブスタンスP濃度はいずれも生存予後と負の相関を示しました。これらの結果は、疼痛強度の高さや持続性が長いほど血中 CGRPおよびサブスタンスP濃度の高値となり、その状態が病状の進行に影響する可能性を示唆しています。
2.ヒトiPS知覚神経モデル:CGRPおよびサブスタンスP放出が乳がん細胞の悪性形質と薬剤抵抗性を増強
ヒトレベルで知覚神経からの神経ペプチド放出とがん細胞への影響を解析するため、ヒト iPS 細胞由来知覚神経に光感受性陽イオンチャネル (ChR2)注4 を導入して、神経科学的手法による人為的知覚神経活性化を行いました。青色光刺激により知覚神経の脱分極を誘導して培養上清を回収したところ、培養上清中の CGRPおよびサブスタンス P 濃度が有意に上昇しました。さらに、この上清をトリプルネガティブ乳がん細胞 (TNBC) に処置すると、ドセタキセルの殺細胞効果 (抗腫瘍効果) が減弱しました。
この現象の分子基盤には、知覚神経活性化上清が、乳がん細胞におけるがん増殖シグナルの一つである PI3K–Akt 経路の活性化を促進し、そのシグナル増幅に CGRPおよびサブスタンスPが協調的に寄与することを1細胞1分子レベルの解析で明らかにしました。さらに、知覚神経活性化培養上清は、薬剤抵抗性に関連する分子 (CDK4/6、ABCB1、ABCC1 など)の発現を上昇させるとともに、SMAD2、ZEB1、vimentin の上昇/E-cadherin の低下といった、がん細胞の浸潤・転移に関連する表現型 (EMT 様変化) も誘導しました。
重要な点は、これらの表現型が CGRP受容体拮抗薬または NK1 受容体拮抗薬により抑制され、CGRPおよびサブスタンスPシグナルが機能的かつ協調的に寄与していることが支持されたことです。さらに同様の傾向は TNBC だけでなくHER2陽性乳がんでも認められ、がん細胞の分子サブタイプを横断して「知覚神経―腫瘍細胞クロストーク」が存在することを明らかにしました。こうした基礎的知見は、乳がん患者さんにおける疼痛の強度・持続と血中CGRPおよびサブスタンスP濃度レベル、ならびに生存予後との関連を理解する上での生物学的基盤を与えるものです。
3.個体レベル検証:知覚神経活性化は腫瘍進行のアクセルとブレーキの相反的制御を担う
侵害受容性神経活動と腫瘍進行を動物個体レベルで検証するため、末梢知覚神経特異的に ChR2 を発現させた遺伝子改変マウスを用い、乳房へ乳がん細胞株を同所移植したのち、腫瘍周囲の知覚神経を光刺激で活性化させることにより人為的に疼痛様症状を誘導しました。腫瘍周囲の知覚神経刺激により腫瘍の増殖は加速し、この加速効果は CGRP受容体拮抗薬 (BIBN4096) と NK1 受容体拮抗薬 (アプレピタント) の併用により完全に抑制されました。さらに、化学療法を想定した薬理試験では、ドセタキセル単独使用に比べ、CGRP受容体拮抗薬と NK1 受容体拮抗薬の併用によりドセタキセルの抗腫瘍効果が増強されました。
これら受容体遮断の臨床的有効性は、TNBC 患者由来腫瘍移植片を乳房同所移植によって作製した PDX モデルマウスでも支持され、CGRP受容体拮抗薬と NK1受容体拮抗薬の併用が腫瘍増殖を抑制し、生存を軽度に延長させました。
一方で本研究は、知覚神経由来因子が腫瘍進行を「促進」するだけでなく、「抑制」させることも明らかにしました。知覚神経活性化後の培養上清では、CGRPなどに加えて内因性KORリガンドであるダイノルフィンの増加が確認され、ダイノルフィンおよび KOR作動薬 (ナルフラフィン) は、ドセタキセルの細胞傷害性効果を増強するとともに、PI3K–Akt シグナルの活性化を抑制しました。さらに、乳がん同所移植モデルマウスでは、末梢性 KORに特異的に作用するナルフラフィン・メチオジドが腫瘍進行を抑制し、ドセタキセルとの併用でその効果が著明に増強されました。
今後の展望および波及効果
本研究は「神経-がん連関」という病態メカニズムを提示し、疼痛制御と腫瘍制御を統合した臨床応用の可能性を示しました。また、本研究では、末梢の知覚神経における軸索反射 (CGRPおよびサブスタンスP放出) を治療の“作用点”として捉え、痛みを「感じた後に抑える」だけでなく、神経ペプチド放出という“初期発生側”の過程にも介入する補完的な疼痛制御の考え方を提示します。
今後は神経ペプチド遮断と神経性ブレーキ賦活を組み合わせた新しい支持療法・抗がん治療の確立が期待されます。臨床応用に向けては、血中 CGRPおよびサブスタンス P を単純な「予後因子」としてではなく、痛み知覚と腫瘍生物学をつなぐ“病態統合マーカー”として位置づけ、単施設研究・後ろ向きであった本研究よりも大規模かつ前向きな検証によって臨床的有用性をしっかりと確立することが重要です。また、治療開発の観点では、モルヒネのような従来の医療用麻薬などの中枢性鎮痛薬による疼痛管理を基盤としつつ、CGRPおよびサブスタンス P 受容体拮抗薬による知覚神経由来の神経ペプチドを介したがん細胞上の応答遮断や KOR 作動薬による腫瘍進行抑制を組み合わせることで、疼痛完治と腫瘍制御を同時に見据えた新しいがん治療概念の確立が期待されます。さらには、これらの標的の発現変動に基づくがん患者さんの病態層別化の考え方等を導入し、どの患者さんにどの組み合わせが最適かを今後検証することが求められます。
以上のように、本研究は新しいがん病態の機序と治療標的の可能性を示しましたが、臨床での有効性・安全性や最適併用レジメンは未確立です。今後は、抗CGRPおよびサブスタンスP製剤のリポジショニングを含めた大規模かつ前向き試験が必要であると考えています。
論文情報
論文タイトル
Pain signaling via sensory neurons drives breast cancer progression through neuropeptide release and κ-opioid counter-regulation
著者
Hitoshi Makabe (筆頭著者), Michiko Narita, Yasuyuki Nagumo, Masanori Fujiwara, Yusuke Hamada, Jion Takise, Takumi Yoshizawa, Sakura Sano, Shin Iizuka, Eri Asaba, Yukari Suda, Tomohisa Mori, Tsuyoshi Saitoh, Hiroshi Nagase, Vivianne L. Tawfik, Shigehiro Yagishita, Akinobu Hamada, Kan Yonemori, Shin Takayama, Masayuki Yoshida, Ryo Yoshizawa, Kenichi GN Suzuki, Rinshi S Kasai, Naoko Kuzumaki (共責任著者), Eriko Satomi (共責任著者), Minoru Narita (星薬科大学:責任著者)
掲載誌
国際学術誌『Pharmacological Research』
DOI
https://doi.org/10.1016/j.phrs.2026.108113
研究資金
本研究は、国立研究開発法人日本医療研究開発機構 (AMED) (JP24ym0126134、JP25ym0126134)、国立がん研究センター研究開発費 (2020-A-1) および星薬科大学の支援を受けて行われました。また、今回の研究は、国立がん研究センターのバイオバンクの試料を用いた研究です。試料をご提供いただきました患者さんに深く感謝申し上げます。
用語解説
注1 カルシトニン遺伝子関連ペプチド (Calcitonin Gene-Related Peptide: CGRP)およびサブスタンス P
CGRPおよびサブスタンスPは、痛み刺激などで知覚神経が興奮した際に神経終末から放出される神経ペプチドです。放出されたCGRPやサブスタンス Pは血管や免疫細胞の働きに影響し、炎症反応(痛み・腫れ・赤みなど)を強めることがあります。近年、これらが腫瘍の周囲環境(腫瘍微小環境)にも影響し得ることが注目されています。
注2 ダイノルフィン
ダイノルフィンは、κオピオイド受容体の内因性リガンドとして作用する体内由来のオピオイドペプチドで、神経から放出されることで主に痛みを抑制し、かゆみを含む感覚応答の調節にも関与しています。また、ストレス応答や神経興奮の制御にも重要な役割を果たしています。
注3 患者由来腫瘍移植モデル
がん患者由来腫瘍移植 (Patient-Derived Xenograft: PDX) モデルとは、がん患者さんの腫瘍組織を免疫の働きが弱いマウス (重度免疫不全マウス: NOGマウスなど) に移植し、ヒト腫瘍を体内で増殖させる実験モデルです。培養で作るがん細胞株に比べ、腫瘍の細胞不均一性や組織構造、遺伝子変異、薬剤反応が保たれやすく、“患者の腫瘍に近い状態”で治療効果を評価できる点が特長です。
注4 光感受性陽イオンチャネル
チャネルロドプシン (Channelrhodopsin: ChR) は、光で開く陽イオンチャネルを形成するタンパク質です。神経細胞に導入すると、光刺激により陽イオンが流入して脱分極が起こり、神経活動を人為的に活性化させることが可能となります (光遺伝学: オプトジェネティクス)。代表的な ChR2 は青色光 (約 470 nm) で活性化されます。
お問い合わせ先
研究に関するお問い合わせ
国立がん研究センター研究所
がん患者病態生理研究ユニット ユニット長 南雲 康行
Eメール: yanagum●ncc.go.jp
広報窓口
星薬科大学
星薬科大学 総務部
Eメール: somu●hoshi.ac.jp
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室
電話番号:03-3542-2511(代表)
Eメール: ncc-admin●ncc.go.jp
