SMARCB1欠損希少がんの新たな治療標的を発見グルタチオン代謝を標的としたGCLC阻害剤のフェロトーシス誘導を介した新たな作用機序を解明
2026年3月17日
国立研究開発法人国立がん研究センター
発表のポイント
- 悪性ラブドイド腫瘍や類上皮肉腫は、有効な治療薬が限られており、新たな治療法の開発が強く望まれる希少がんであり、「SMARCB1」という遺伝子の欠損が特徴的であることから、SMARCB1欠損がんの代表的疾患とされています。
- 研究グループは、SMARCB1欠損がんの弱点として、「グルタチオン合成能力の低下」を特定し 、GCLC阻害剤の単独および、グルタチオン代謝経路を標的とする阻害剤との併用によって、強力な抗腫瘍効果を発揮することを明らかにしました。
- また、この阻害剤には、「フェロトーシス」と呼ばれる鉄依存性の細胞死をがん細胞に誘導するという特徴的な作用機序があることを解明しました。
- 本研究成果は、有効な治療法が限られている希少がんに対する新たな治療標的を提示するものであり、米国癌学会(AACR)の学術誌「Cancer Research」にて発表されました。
概要
国立研究開発法人国立がん研究センター(所在地:東京都中央区、理事長:間野 博行)研究所 がん治療学研究分野 竹内 麻里子 ユニット長、荻原 秀明 分野長らの研究グループは、小児に多い難治性がんである悪性ラブドイド腫瘍 注1や、思春期・若年成人(AYA世代注2)に多い類上皮肉腫注3に対して、「GCLC注4阻害剤」が有望な治療戦略となりうることを明らかにしました。 本研究では、これらのがんで欠損している遺伝子「SMARCB1注5」に着目し、その欠損が細胞内の抗酸化物質「グルタチオン注6」の量を低下させることを発見しました。さらに、グルタチオン合成の鍵となる酵素「GCLC」を阻害することで、がん細胞特異的に「フェロトーシス注7」と呼ばれる細胞死を誘導し、腫瘍の増殖を抑制することに成功しました。 また、本阻害剤をグルタミナーゼ阻害剤などのグルタチオン代謝経路を標的とする阻害剤と併用することで、抗腫瘍効果が相乗的に増強されることも見出しました。特に、今回使用したGCLC阻害剤は、既存のEZH2阻害剤と比較して、SMARCB1欠損型細胞への選択性が高いことが非臨床試験において明らかとなりました。
本研究成果は、有効な治療法が限られている希少がんに対する新たな治療標的を提示するものであり、米国東部時間2026年3月16日(日本時間3月17日)付で、米国癌学会(AACR)の学術誌「Cancer Research」にて発表されました。
背景
悪性ラブドイド腫瘍は、主に乳幼児の腎臓や脳に発生する希少がんで、既存の治療では十分な効果が得られにくい特徴があります(成人での発症は稀)。また、類上皮肉腫はAYA世代に好発する軟部肉腫であり、進行が早く再発しやすい特徴があります。これらのがんは、細胞のがん化を抑制する遺伝子である「SMARCB1」の機能が失われている(欠損している)という共通点がありますが、現在有効な治療薬は限られており、新たな治療法の開発が強く望まれています。
研究グループは、これらのがん細胞に特有の代謝の「弱点(アキレス腱)」を攻める「合成致死注8治療法」の開発に長年取り組んできました。 これまでに、SMARCB1と同じ「クロマチンリモデリング複合体」の異常を持つがん(ARID1A欠損がん)において、抗酸化物質「グルタチオン」の代謝が弱点になることを世界に先駆けて発見しました(参考1)。また、SMARCB1欠損がんに対する新たな合成致死標的(CBP/p300)を同定するなど、本疾患の病態解明に向けた研究をリードしてきました(参考2)。
本研究は、GCLC阻害剤を用いることで、SMARCB1欠損がんにおけるグルタチオン代謝の脆弱性を標的とする、新たな治療標的の発見を目指したものです。
研究成果
1. SMARCB1欠損がんの「弱点」を特定
研究グループは、SMARCB1が欠損した細胞では、アミノ酸の一種であるシスチン(Cys-Cys:システインが2つ結合したアミノ酸)を取り込むタンパク質「SLC7A11」の量が減少していることを突き止めました(図1)。シスチンは、細胞を酸化ストレスから守る物質「グルタチオン」の材料となるため、SMARCB1欠損細胞ではシスチンの低下に伴い(図2)、グルタチオンの量が正常細胞に比べて著しく低下していました(図3)。この「グルタチオン不足」こそが、これらのがん細胞の弱点であることを発見しました。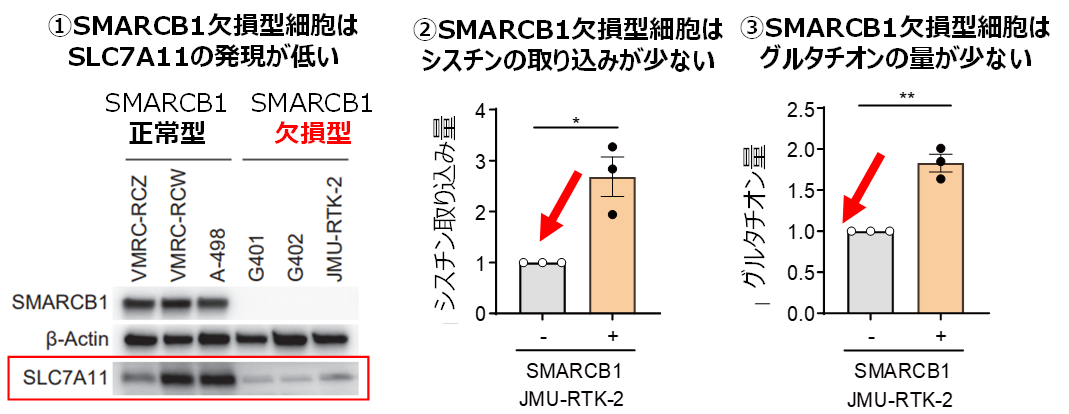
2. GCLC阻害剤の効果とメカニズム
この弱点をさらに攻めるため、グルタチオン合成の律速酵素注9である「GCLC」を標的としました。GCLC阻害剤(GCLCi0/GCLCi1)を用いた実験の結果、GCLC阻害剤によりグルタチオンが減少すると(図4)、活性酸素による脂質の酸化が進行することから(図5)、鉄依存性の細胞死である「フェロトーシス」が引き起こされることが分かりました。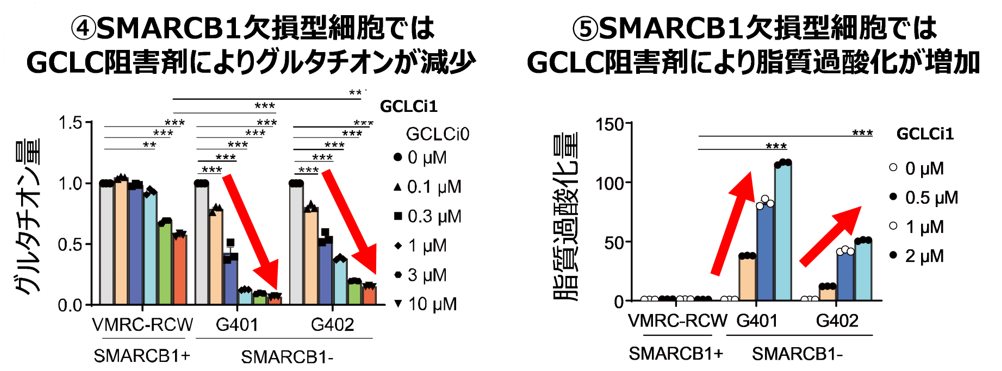
3. GCLC阻害剤の優位性
今回使用GCLC阻害剤は、SMARCB1を持つ正常な細胞には影響が少なく、SMARCB1が欠損したがん細胞だけを選択的に抑えることができました(図6)。また、非臨床試験(細胞実験)において、米国で類上皮肉腫の治療薬として承認されているEZH2阻害剤と比較して、SMARCB1欠損型細胞への選択性が約4倍高いことが明らかとなりました(図7)。この結果は、既存の治療薬よりも抗腫瘍効果が高い可能性があることが期待されます。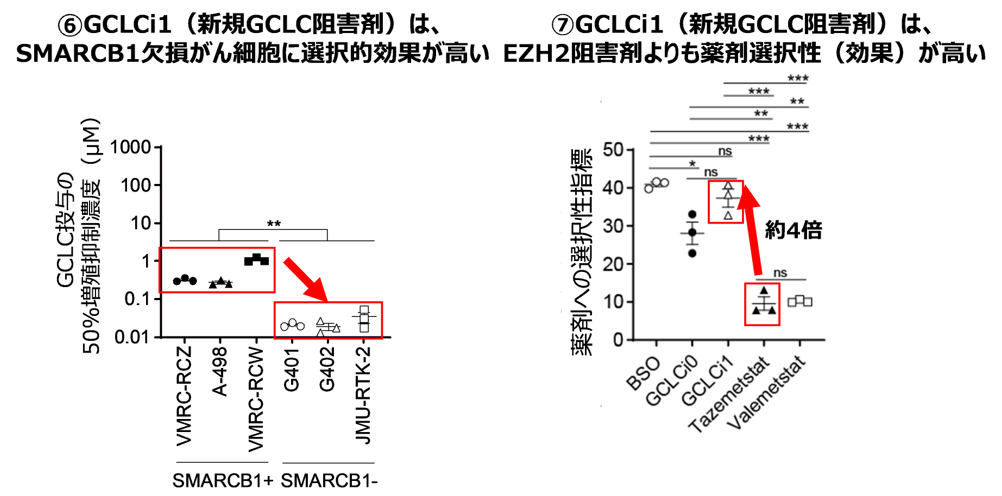
4. マウスモデルでの効果
ヒトの悪性ラブドイド腫瘍を移植したマウスに本阻害剤(GCLCi1)を投与したところ、体重減少などの副作用を伴わずに、顕著な腫瘍縮小効果が認められました(図8)。本実験では、阻害剤を連続して投与するのではなく、休薬期間を設ける「間欠投与(5日間投与・2日間休薬)」という投与条件を工夫することで、効果を維持しつつ安全性が担保できる可能性を示唆しました。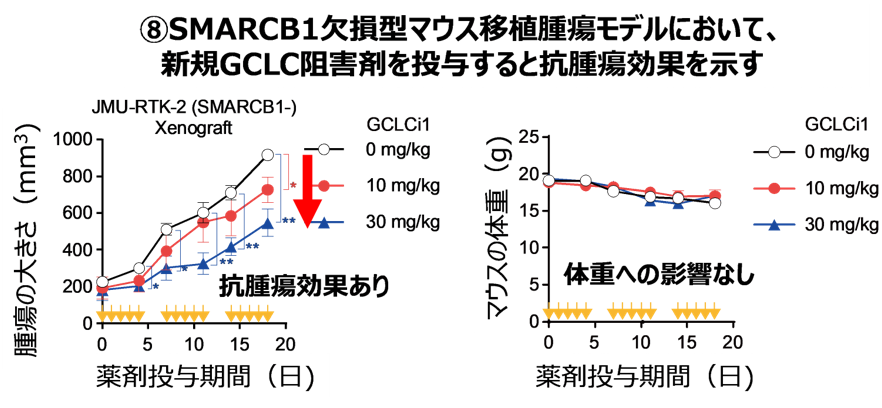
5. 併用療法による効果増強
さらに、本GCLC阻害剤をグルタミナーゼ(GSL)阻害剤「テラグレナスタット」など、他のグルタチオン代謝阻害剤と組み合わせることで、抗腫瘍効果がさらに増強されることも見出しました(図9)。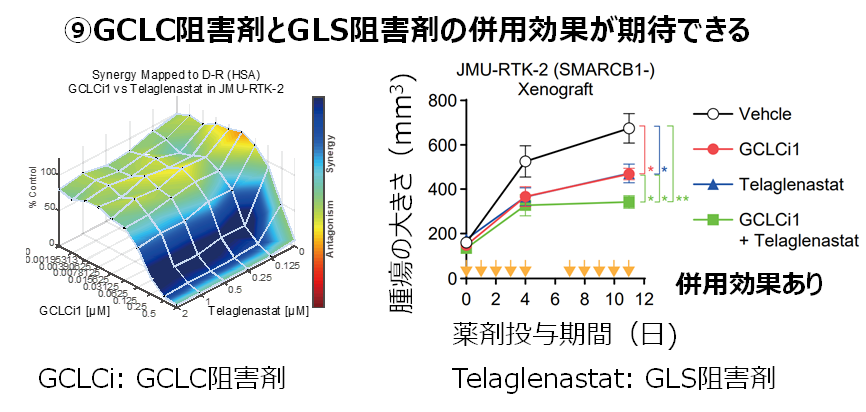
展望
本研究により、SMARCB1欠損がんに対するGCLC阻害剤の有効性が非臨床試験(細胞・動物実験)レベルで示されました。あわせて、GCLC阻害剤をグルタミナーゼ阻害剤などのグルタチオン代謝経路の阻害剤と併用することで、その抗腫瘍効果が相乗的に増強されることも明らかとなりました。今回用いたGCLC阻害剤は、既存の実験用試薬(L-buthionine sulfoximine (BSO))に比べて低用量で高い効果を示し、投与条件を工夫することで生体内での安全性を制御できることが示唆されています。
本研究は、SMARCB1欠損がんにおいてGCLC阻害及びグルタチオン代謝経路を標的とする治療戦略が有望である可能性を示しました。今後、この知見が他の薬剤や治療法との併用も含めたさらなる研究につながり、これまで有効な治療法が限られていたSMARCB1欠損がんに対する個別化医療(プレシジョン・メディシン)に基づく新たな治療法開発の一助となることが期待されます。
論文情報
雑誌名
Cancer Research
タイトル
GCLC Inhibitor Enhances the Antitumor Efficacy of Glutathione Metabolic Pathway Inhibition in SMARCB1-Deficient Rhabdoid Tumors (SMARCB1欠損ラブドイド腫瘍におけるGCLC阻害剤とグルタチオン代謝経路阻害の併用による抗腫瘍効果の増強)
著者
竹内 麻里子, 石川 善則、岡田 拓也、小崎 龍平、荻原 秀明* (*責任著者)
DOI
10.1158/0008-5472.CAN-25-2848
掲載日
米国東部時間2026年3月16日(日本時間3月17日)付
URL
https://aacrjournals.org/cancerres/article/doi/10.1158/0008-5472.CAN-25-2848(外部サイトにリンクします)研究費
本研究は、小野薬品工業株式会社との共同研究として実施されました。研究費名: 共同研究費(小野薬品工業株式会社)
研究事業名: 共同研究
研究課題名: クロマチンリモデリング複合体欠損がんに有望な治療標的薬の開発
研究代表者名: 荻原 秀明
参考(本研究と関連するプレスリリース情報)
- 2019年1月25日プレスリリース:
日本人に多い卵巣明細胞がんなどでみられるARID1A遺伝子変異がんを対象に代謝(メタボローム)を標的とした新たながん治療法を発見 - 2024年6月26日プレスリリース:
SMARCB1遺伝子欠損型の小児・AYA世代のがんに有望な治療標的と阻害剤を発見新たに開発した網羅的な創薬標的探索方法により難治性がんの治療開発の加速が期待
用語解説
注1 悪性ラブドイド腫瘍
主に乳幼児の腎臓や中枢神経系、軟部組織に発生する、極めて悪性度の高い希少がん。
注2 AYA世代
Adolescent and Young Adult(思春期・若年成人)の頭文字をとったもので、主に、思春期(15歳~)から30歳代までの世代を指しています。
注3 類上皮肉腫
AYA世代の四肢(腕や脚)に発生しやすい軟部肉腫の一種。悪性ラブドイド腫瘍と同様にSMARCB1遺伝子の欠損を特徴とし、再発・転移しやすく十分な治療効果が得られにくい希少がん。
注4 GCLC (グルタミン酸システインリガーゼ触媒サブユニット)
グルタチオンを合成する最初のステップを担う重要な酵素。
注5 SMARCB1
遺伝子のスイッチを入れたり切ったりする「クロマチンリモデリング複合体」の構成因子。多くのがんでこの機能が失われていることが知られています。
注6 グルタチオン
細胞内に存在する主要な抗酸化物質。活性酸素種を除去し、細胞を酸化ストレスから守る役割があります。
注7 フェロトーシス (Ferroptosis)
近年発見された新しい細胞死の形態。細胞内の鉄と過酸化脂質の蓄積によって引き起こされます。
注8 合成致死 (Synthetic Lethality)
私たちは通常、同じ働きをする遺伝子を1対(2個)持っています。そのため、一方の機能が失われても、もう一方が「バックアップ」として働くことで、細胞は生存し続けることができます。しかし、特定のがん細胞では、すでに両方の遺伝子が失われ、バックアップが効かない状態になっています(本研究ではSMARCB1遺伝子の欠損)。この「がん細胞だけの弱点」を突き、バックアップとして機能している別の遺伝子を薬で抑えると、がん細胞だけを力尽きさせ、死滅させることができます。正常な細胞にはバックアップが残っているため影響を受けにくく、がん細胞だけを効率よく狙い撃ちできる画期的な治療戦略です。
注9 律速酵素
一連の化学反応において、最も反応速度が遅く、全体の速度を決定する重要な酵素のことです。この酵素の働きを調節することで、代謝経路全体の流れをコントロールできるため、創薬の標的となりやすいと考えられています。
お問い合わせ先
- 研究に関するお問い合わせ
国立研究開発法人国立がん研究センター研究所
がん治療学研究分野 荻原 秀明
電話番号:03-3542-2511(代表)
Eメール:hogiwara●ncc.go.jp - 広報窓口
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室
電話番号:03-3542-2511(代表)
Eメール:ncc-admin●ncc.go.jp
