トップページ > 診療科・共通部門 > 内科系 > 消化管内視鏡科 > 研究について
研究について
人工知能を用いた内視鏡診断補助機器
内視鏡画像を機械に学習させ、病変の有無や質的診断を補助する人工知能システムを開発しています。画像診断における機械学習の領域は近年大きな進歩が得られている領域であり、機械学習に関する専門家との連携を通じて内視鏡診断への応用を進めています。
咽喉頭表在がんの自動検出
咽喉頭領域のがんは早期発見が難しいとされてきましたが、NBI(Narrow band image)システムという特殊な波長を用いて内視鏡観察する方法が考案されて以降、早期発見率が向上してきました。しかしながら咽喉頭領域は解剖学的にも複雑な構造をしており、また内視鏡挿入時に咽頭反射が起きやすく観察が難しい場合や、内視鏡での細胞の採取が難しい場合もあり、がんの発見、観察、診断は必ずしも容易ではありません。近年、消化管領域(食道、胃、大腸)において、人工知能によるがんを含む腫瘍性病変の早期発見の有用性が報告されるようになり、内視鏡の診断補助機能の一つとして注目されています。咽喉頭領域のがんを含む腫瘍性病変の早期発見にも、人工知能の利用が有効なのではないかと考えられます。
我々は咽喉頭表在がんと正常な咽喉頭領域粘膜の内視鏡画像を学習させて咽喉頭領域の表在がんの検出のための人工知能モデルを作成し、その性能を検証しました(Inaba A, et al. Head and Neck 2020, DOI: 10.1002/hed.26313)。静止画像のみを用いた検証でしたが、感度(がんがある部位に対して「がんがある」と判断できる確率)は95.5%と非常に高い数値を示しました。
図1. 咽喉頭表在がんの検出例(青色の枠:内視鏡専門医が表在がんがある部位を囲った範囲、赤色の枠:人工知能が表在がんがあると予測して囲った範囲、10mm以下の表在がんも内視鏡専門医と同じように検出できています)

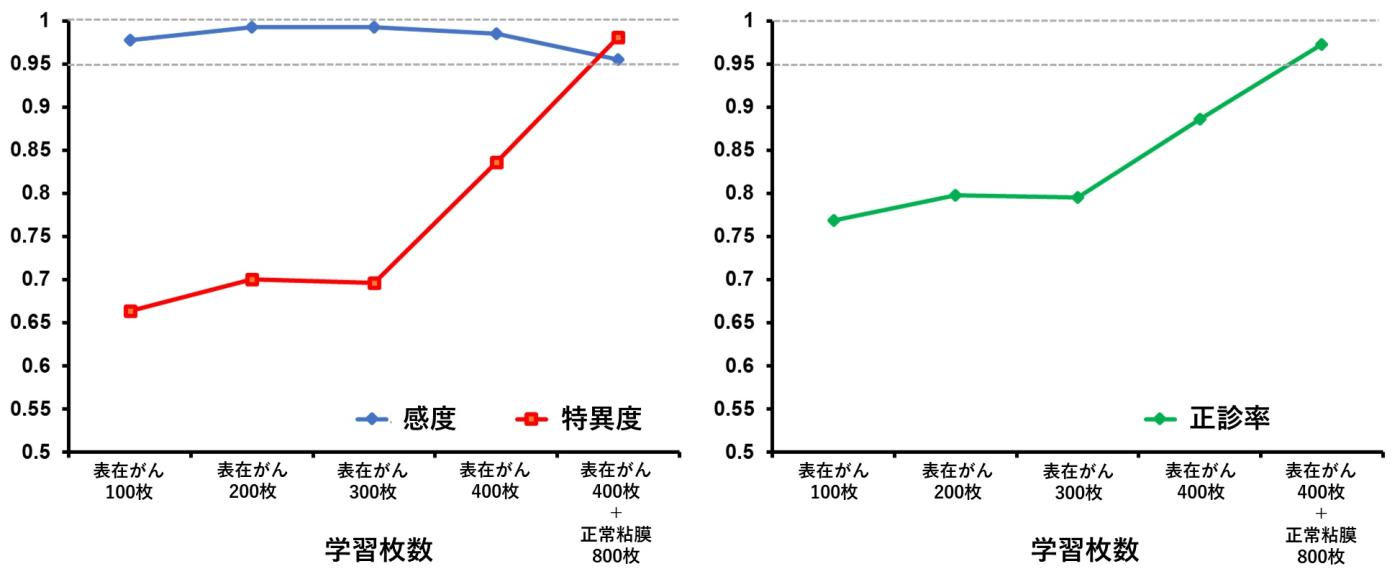
また、がんのない正常な咽喉頭領域の粘膜を追加学習させることで、特異度(がんがない部位に対して「がんがない」と判断できる確率)が改善する(学習前:83.6%→学習後:98.4%)ことも明らかになりました。
図2. 人工知能に対する内視鏡画像の学習枚数と性能の推移について
これらの研究をもとに現在、我々は企業との共同研究を行い内視鏡動画を利用してリアルタイムに咽喉頭表在がんを検出するための人工知能モデルの開発を進めています。