トップページ > 取り組み > 荘内病院×国立がん研究センター東病院 医療連載「つながる医療 がん治療最前線」 > 第11回 あなたの日常を守る大腸がんに対する外科治療の進展・リキッドバイオプシーによるがんゲノム医療
荘内病院×国立がん研究センター東病院 医療連載「つながる医療 がん治最前線」第11回 あなたの日常を守る大腸がんに対する外科治療の進展・リキッドバイオプシーによるがんゲノム医療
2022年3月26日
あなたの日常を守る 大腸がんに対する外科治療の進展
国立がん研究センター東病院 大腸外科、手術機器開発分野長 伊藤 雅昭
手術と他の治療方法を組み合わせたあきらめない大腸がん治療
「がん」という診断をされた場合、多くの方は非常に悲しい思いをされると思います。この先どのような治療が待っているのか、本当に治るのだろうか、手術によって日常生活は今まで通り送ることができるだろうか、と。
もちろん病気の進み具合により治療方法が限られることもありますが、近年の治療開発の進展により多くの大腸がんはたとえ進行した場合においてもあきらめる必要のない病気になってきました。今なお手術は大腸がんを治すうえで中心的な治療方法ですが、同様に抗がん剤治療や放射線治療の治療開発も年々進化してきました。
その結果これらの治療方法を手術と適切に組み合わせることによって以前に比べ、がんが治る確率は飛躍的に向上してきました。ですので大腸がんになったとしても、すぐにあきらめる必要はないのです。
機能を残しやさしく治す外科治療の実践
またもう一つ重要な側面はいかに体へのダメージが少なく、かつ手術後の生活を維持できる手術を提供できるのかという点です。
とりわけ肛門に近い直腸にがんができた場合、永久人工肛門をなるべく作らない方法で手術ができるか、術後に排便機能や排尿機能を保ったままの生活できるのか、といった心配は多くの方々が持たれることだと思います。
国立がん研究センター東病院大腸外科では、過去20年以上にわたり直腸がんに対して腹腔鏡手術による肛門温存手術を数多く行ってまいりました。
その結果従来では永久人工肛門しか選択肢なかった中で多くの患者さんは自分の肛門を残す手術を受ける選択が可能になりましたし、70%以上の方は比較的良好な排便を保つことができることもわかってまいりました。つまり機能を残しながらやさしく治す治療の実践です。
また近年の治療開発では、通常のおなか側から行う腹腔鏡手術に加え、肛門側から同様に内視鏡を使って精度の高い手術を併用するやり方(TaTMEという新しい手術方法)も登場してまいりました。
その結果さらに肛門温存率は向上し、神経の良好な温存により排尿機能が損なわれることがとても少なくなってきました。
またおなか側からと肛門側から同時に内視鏡手術を行う「2チーム手術」も実践されており、その結果手術時間が従来の方法の半分程度で行えるようになりました。
最近では国立がん研究センター発ベンチャー企業と連携し、二人の外科医の役割を代用する新たな手術ロボットを開発中です。近い将来このロボットを使った新しい内視鏡手術では、従来5人の外科医が必要であった2チーム手術の人員を2人にまで減らすことができる可能性もあります。
超高齢化社会を避けることのできない日本において、今後増え行く多くの大腸がん患者さんを治すためには、このような手術ロボットを利用しながら質の高い手術を提供する必要があります。

執筆者

- 伊藤雅昭(いとう・まさあき)
- 1993年千葉大医学部卒。1994年社会保険船橋中央病院外科医員、1995年国立がんセンター東病院大腸外科レジデント、1998年久留米大免疫学教室助手、2000年国立がんセンター東病院大腸骨盤外科医員、2009年同病院消化器科医長、2012年同病院大腸外科外来医長等を経て、同病院大腸外科科長、先端医療機器開発センター手術機器開発分野長(併任)、医療機器開発センター手術機器開発室長(併任)、現在に至る。
リキッドバイオプシーによるがんゲノム医療
国立がん研究センター東病院 消化管内科長 吉野 孝之
がん組織から血液中に放出されたがん細胞あるいはその断片である腫瘍由来DNA(血液循環腫瘍DNA:ctDNA)を捉える革新的技術が現実のものとなりました。
このリキッドバイオプシー技術は、がん患者さんから通常量の20ミリリットル程度の血液採取を行い、その中に含まれる1000個のDNA断片(ほとんどは正常細胞由来)の中にctDNAが1個以上の割合で存在すれば検出可能です。
2021年8月1日から、このctDNAを用いて数百の遺伝子異常を一度に検査できる「遺伝子パネル検査」が保険診療として受けられるようになりました。つまりPrecision Oncology(がんゲノム医療)として進行固形がん(主にステージ4期)の患者さんに対して臨床応用が開始されました。
現在のリキッドバイオプシー最先端技術を用いれば、20ミリリットルから40ミリリットルまで/回の血液採取を行い、その中に含まれる1万個のDNA断片の中にctDNAが1個以上の割合で存在すれば検出可能となっています。この最先端技術はがんの早期発見に活用できるのではないかと期待されています。
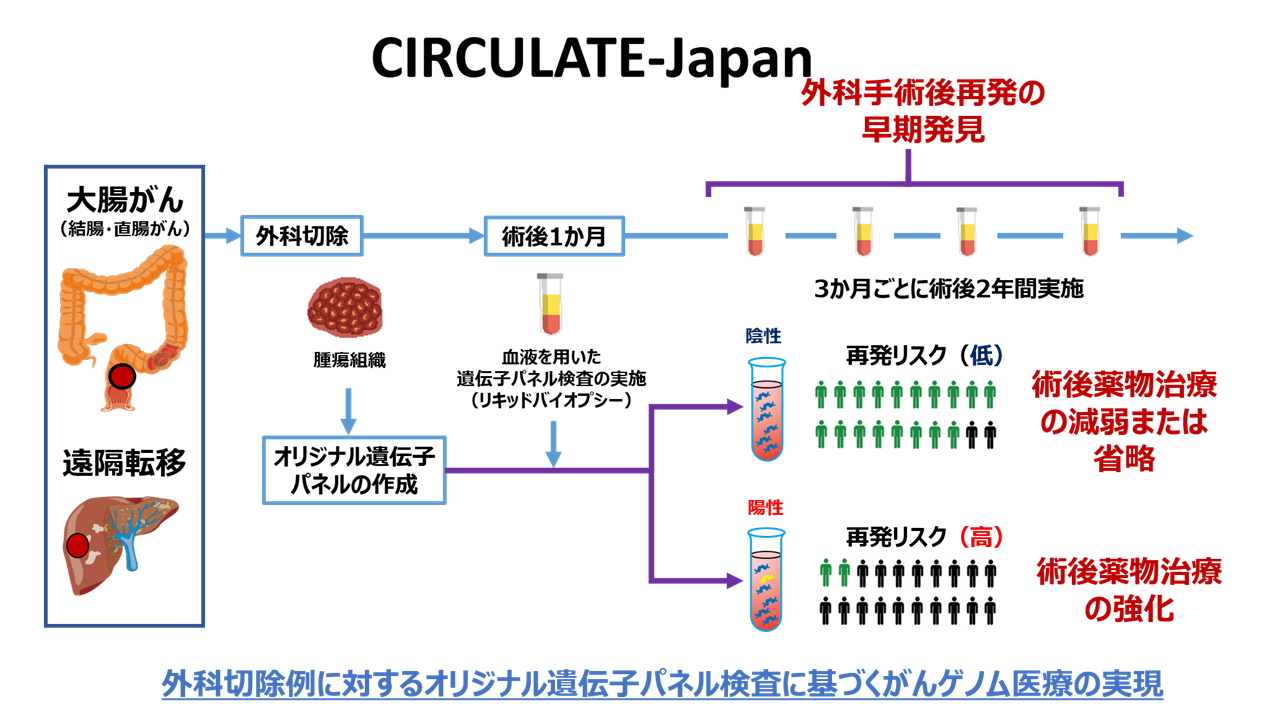
まずは外科切除後の患者さん(結腸・直腸がん、肺がん、乳がん、尿路上皮がん、等)の再発予測能の評価として始まり、特に結腸がん根治切除後1か月の時点でctDNAが陽性なら90%以上再発、陰性なら10%以下の再発と報告されています。
つまりctDNA陽性なら術後補助薬物療法を強める、陰性なら術後補助薬物療法を弱めるまたは省略するといった治療戦略が成り立つ可能性があります。
現在国立がん研究センター主導で、その検証研究(CIRCULATE-Japan)が国内外約150病院との協力下で進行中です(下図)。
本研究では、根治的外科治療を予定しているステージ2期から4期を含む大腸がんの患者さん5000名を対象に、術後2年間、リキッドバイオプシーを用いた再発のモニタリング検査を行います。手術で取り出した腫瘍組織を用いた全エクソーム解析の結果をもとに、患者さんオリジナルの遺伝子パネルを作製します。
その後、術後1か月時点から定期的に血液を採取し、患者さん毎のオリジナル遺伝子パネルを用いて、血液中のがん遺伝子異常の有無を調べます。
まさにPrecision Onco-surgery(手術可能ながんのがんゲノム医療)の幕明けです。
現時点では画像診断によるがんの早期発見が行われていますが、さらに超早期発見に向けた臨床開発として、いくつかのがん腫で早期がんばかりでなく前がん病変(例えば大腸進行腺腫)を含めて検出可能か臨床研究が進んでいます。検出感度を向上するためctDNAの検出に加え、メチル化、蛋白発現、マイクロRNAなどの腫瘍由来の変化をも加味した診断系の確立も進んでいます。
近い将来、まずは採血、その結果を用いてここを集中的に精査するという診断手順、ひいては超早期発見と検診の個別化が可能となると思います。
執筆者

- 吉野孝之(よしの・たかゆき)
- 千葉県出身。1995年防衛医科大学校卒。97年国立がんセンター中央病院臨床検査部・病理部研修医、99年同東病院内視鏡部消化器内科研修医、2002年静岡県立静岡がんセンター消化器内科副医長、2007年国立がんセンター東病院内視鏡部消化器内科医員、2010年国立がん研究センター東病院 消化管内科外来・病棟医長を経て2014年より現職。BEST DOCTORS IN JAPAN 2020受賞。