トップページ > 研究組織一覧 > 分野・独立ユニットグループ > がん治療学研究分野 > 研究プロジェクト
研究プロジェクト
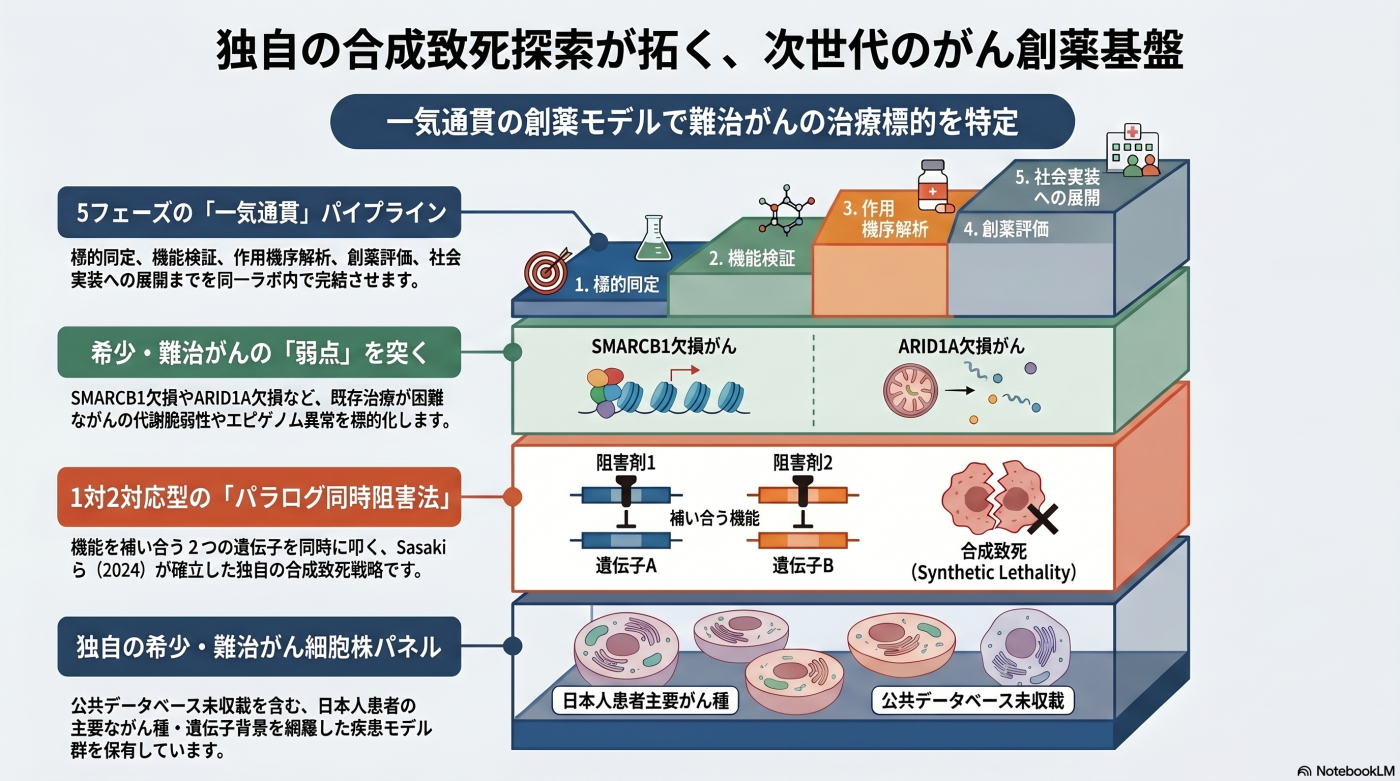
独自の標的探索が、独自の創薬シーズを生む。
がん治療学研究分野では、合成致死(Synthetic Lethality)に基づく標的探索を軸に、独自のパラログ同時阻害スクリーニング、希少がん・難治がん細胞株パネル、マルチオミクス解析を組み合わせ、標的同定から作用機序解析、化合物評価、創薬シーズ化までを一気通貫で進めています。
本ページでは、その研究を支える 独自の研究基盤 と、対象がん種別の研究プロジェクト を紹介します。研究内容の詳細な解説は 研究ハイライト を、論文業績は 論文業績ページ をご参照ください。
1. 独自の研究基盤
合成致死標的の探索から、作用機序解析、化合物評価までを一気通貫で進めるための独自の研究基盤を、4 つの軸で整備しています。
1-1. パラログ同時阻害法・パラログペア同時 KO ライブラリー
1 対 2 対応型の合成致死戦略
がん細胞で生じた 1 つの遺伝子異常に対して、機能を補い合う 2 つのパラログ標的を同時に阻害する、1 対 2 対応型の合成致死戦略 です。単一標的阻害では補完されてしまうパラログ関係を設計段階から考慮することで、特定の遺伝子背景を持つがん細胞の脆弱性を治療標的化することを目指します(Sasaki et al., Nat Commun, 2024)。
- パラログペア同時ノックアウトベクターライブラリー: ゲノム網羅的にパラログペアを同時阻害して合成致死性を評価可能な独自資産
- CRISPR/Cas9 スクリーニング系: Chronos、MAGeCK 等を用いた解析パイプラインを整備し、がん細胞株パネルへの適用に最適化
これまでの主な成果(論文公開済み範囲)
- SMARCB1 欠損がん(悪性ラブドイド腫瘍、類上皮肉腫など)に対する CBP/p300 同時阻害 の合成致死性を確立 ── Nat Commun 2024(Sasaki et al.)
- cBAF 欠損がん(肺がんなど)への展開 ── Cancer Res Commun 2025(Sasaki et al.)
- 研究用化合物 CP-C27(CBP/p300 阻害)を用いた検証 ── Nat Commun 2024 で公開済み
→ 詳しくは 研究ハイライト「パラログ同時阻害法」 を参照
1-2. 希少がん・難治がん細胞株パネル
国立がん研究センター研究所の研究室として、私たちは臨床現場で課題となる希少がん・難治がんを研究対象に、独自の細胞株パネルと疾患特異的モデルを整備してきました。公共データベースに未収載の細胞株や、日本人患者で臨床的に重要な病型を含むモデルを活用することで、公共データ解析だけでは見えにくい治療標的の探索を進めています。
- 独自細胞株パネル: SMARCB1 欠損型(悪性ラブドイド腫瘍、類上皮肉腫)、ARID1A 欠損型(卵巣明細胞がん、びまん性胃がん)、SMARCA4 欠損型(非小細胞肺がん)、KRAS 変異型(肺がん・膵臓がん)、SMAD4 欠損型(びまん性胃がん、膵臓がん、食道がん)、KDM6A 欠損型(食道がん)など、当分野が標的とする主要ながん種・遺伝子背景をカバー
- 患者由来モデル: PDX、オルガノイド等を含む患者由来モデルを、NCC 内外の連携基盤を活用しながら薬効評価に接続
1-3. データ駆動型探索基盤
公的データベースの再解析と、研究室独自の細胞株パネルによる検証を組み合わせて、合成致死標的を効率的に同定する基盤です。
- DepMap データ再解析: Chronos 等の遺伝子依存性スコアを用いた標的候補抽出
- CRISPR スクリーニング解析: MAGeCK 等を用いた自前スクリーニングデータの解析
- 公共データベース横断解析: CCLE / TCGA / GTEx などとの統合解析
代表的成果
- ARID1A 欠損卵巣明細胞がんに対する USP8/FGFR2 経路の同定 ── NPJ Precis Oncol 2025(Saito et al.)
→ 詳しくは 研究ハイライト「データ駆動型探索」 を参照
1-4. メカニズム・創薬評価基盤
標的同定後の作用機序解析と、化合物評価までを一貫して実施するための基盤です。
- マルチオミクス解析: RNA-seq、ATAC-seq、CUT&RUN、ChIP-seq
- 代謝解析: メタボロミクス、グルタチオン代謝・ピリミジン代謝経路の解析
- 薬効評価: in vitro 細胞死アッセイ、in vivo CDX モデル評価
- 化合物評価: 製薬企業との共同研究を通じた創薬シーズの実証
一気通貫の研究パイプライン
これらの研究基盤は、以下の 5 フェーズで一気通貫に接続されています。
|
フェーズ |
内容 |
主な技術・資産 |
|---|---|---|
|
標的同定 |
合成致死標的候補の抽出 |
パラログペア同時 KO ライブラリー、DepMap 再解析、CRISPR スクリーニング |
|
機能検証 |
遺伝子依存性・薬剤感受性の確認 |
KO/レスキュー実験、独自細胞株パネル、薬効評価 |
|
作用機序解析 |
なぜ効くかの解明 |
RNA-seq、ATAC-seq、CUT&RUN、代謝解析、ウェスタンブロット |
|
創薬評価 |
化合物・併用療法の検証 |
in vitro 評価、CDX モデル、薬効・毒性評価 |
|
展開 |
共同研究・導出・臨床接続 |
NCC 臨床部門との連携、製薬企業との共同研究 |
標的候補の同定から、作用機序解析、化合物評価、共同研究・創薬展開への接続までを、一つの流れとして進められることが、当研究室の強みです。
2. 対象がん種別の研究プロジェクト
希少がん・小児がん・難治がんを対象とした研究プロジェクト
私たちが取り組むのは、有効な分子標的治療の選択肢が限られる、または標準治療への抵抗性が課題となるがんです。これらに共通するのは、「弱点はあるが、それを正面から突く治療がまだ存在しない」という現実です。私たちの基盤を適用して、この急所を探し当てる ── それが対象がん種別研究プロジェクトの目的です。
研究プロジェクトは、患者さんを起点に 2 つのカテゴリで展開しています。
注: 各プロジェクトの遺伝子変異頻度の出典・詳細解説は、論文業績ページ および 研究ハイライト の該当ページをご参照ください。
Category A ── 希少がん・小児がんへの挑戦
Project A-1: 悪性ラブドイド腫瘍・類上皮肉腫
|
項目 |
内容 |
|---|---|
|
対象がん |
悪性ラブドイド腫瘍、類上皮肉腫 |
|
患者層 |
小児・AYA 世代(若年成人) |
|
主な遺伝子背景 |
SMARCB1 欠損(悪性ラブドイド腫瘍では高頻度に認められ、類上皮肉腫でも主要な分子異常) |
|
臨床的課題 |
予後不良で、有効な分子標的治療の選択肢が限られる |
|
研究アプローチ |
パラログ同時阻害法の適用(CBP/p300 同時阻害)と、グルタチオン代謝脆弱性に基づく GCLC 阻害戦略 |
|
関連論文 |
Sasaki et al., Nat Commun 2024(パラログ同時阻害、CP-C27 を用いた検証)/ Takeuchi et al., Cancer Res 2026(GCLC 阻害剤、小野薬品工業との共同研究) |
|
関連研究ハイライト |
Project A-2: 卵巣明細胞がん
|
項目 |
内容 |
|---|---|
|
対象がん |
卵巣明細胞がん(OCCC) |
|
患者層 |
日本人女性に比較的多いサブタイプ |
|
主な遺伝子背景 |
ARID1A 欠損(約 50% の症例で欠損) |
|
臨床的課題 |
従来のプラチナ製剤など標準化学療法が効きにくく、再発例での治療選択肢が限られる |
|
研究アプローチ |
エピゲノム異常が引き起こす代謝脆弱性(グルタチオン代謝への依存性)、既存薬の再定義、データ駆動型 USP8 標的の同定 |
|
関連論文 |
Ogiwara et al., Cancer Cell 2019(グルタチオン代謝への依存性を示した成果)/ Kuroda et al., Gynecol Oncol 2019(既存薬ゲムシタビンの選択的有効性)/ Saito et al., NPJ Precis Oncol 2025(USP8 を介した合成致死) |
|
関連研究ハイライト |
Category B ── 難治性固形がんの攻略
Project B-1: 非小細胞肺がん(NSCLC)
|
項目 |
内容 |
|---|---|
|
対象がん |
非小細胞肺がん(NSCLC) |
|
主な遺伝子背景 |
SMARCA4 欠損(約 10%)/ CREBBP 変異(約 8%)/ KRAS 変異(NSCLC で認められる主要なドライバー異常の一つ) |
|
臨床的課題 |
EGFR 変異や ALK 融合など、既存の分子標的薬の対象となる代表的ドライバー異常を持たない症例を含み、治療選択肢が限られる |
|
研究アプローチ |
パラログ依存性に着目。SMARCA4 欠損がんでは SMARCA2 を、CREBBP 欠損がんでは EP300 を、それぞれ標的とする。KRAS 変異 NSCLC については、SWI/SNF 異常との複合背景や薬剤耐性を含めた合成致死標的探索を進めています |
|
関連論文 |
Oike et al., Cancer Res 2013(SMARCA4 欠損がんでの SMARCA2 依存性)/ Ogiwara et al., Cancer Discov 2016(CREBBP 欠損がんでの EP300 依存性)/ Kanada et al., J Med Chem 2023(EP300/CBP HAT 阻害剤 DS-9300) |
|
関連研究ハイライト |
Project B-2: びまん性胃がん(スキルス胃がんを含む)
|
項目 |
内容 |
|---|---|
|
対象がん |
びまん性胃がん(スキルス胃がんを含む) |
|
主な遺伝子背景 |
ARID1A 欠損(約 25%)/ SMAD4 欠損 |
|
臨床的課題 |
腹膜播種を伴いやすく、既存化学療法では制御が難しい症例が多い難治性がん |
|
研究アプローチ |
独自の細胞株パネルを用いたスクリーニングで同定したピリミジン代謝の脆弱性。ARID1A 欠損が SLC28A3 サイレンシングを介して dCTP プールを枯渇させる Dual-hit メカニズムを解明 |
|
関連論文 |
Hirano et al., Mol Cancer Res 2026(ARID1A 欠損びまん性胃がんでのピリミジン代謝脆弱性、ゲムシタビン感受性のメカニズム解明) |
|
関連研究ハイライト |
Project B-3: 膵臓がん・食道がん
|
項目 |
内容 |
|---|---|
|
対象がん |
膵臓がん、食道がん |
|
主な遺伝子背景 |
SMAD4 欠損(膵臓がんの約 33%、食道がんの一部)/ KRAS 変異(膵臓がんの約 95%)/ KDM6A 欠損(食道がんの約 14%) |
|
臨床的課題 |
KRAS 阻害剤などが開発されつつあるものの、膵臓がん・食道がんでは依然として治療成績に課題が残り、多角的な治療戦略が必要 |
|
研究アプローチ |
エピゲノム制御因子(KDM6A 等)と代謝経路に着目し、標準治療抵抗性を克服する新規標的の探索を進める |
|
成果と展開 |
SMAD4 / KDM6A / KRAS 軸の合成致死標的探索を進行中。今後の論文公開によって順次本ページを更新予定 |
|
関連研究ハイライト |
Project B-4: 腎細胞がん(PBRM1 欠損型)
|
項目 |
内容 |
|---|---|
|
対象がん |
腎細胞がん(PBRM1 欠損型) |
|
主な遺伝子背景 |
PBRM1 欠損 |
|
臨床的課題 |
既存治療への応答性や耐性機構に多様性があり、分子背景に基づく新たな層別化・治療標的探索が求められる |
|
研究アプローチ |
SWI/SNF 複合体構成因子の欠損がもたらす合成致死標的を探索 |
|
成果と展開 |
探索的フェーズ。SWI/SNF 欠損がん全般の知見(Sasaki et al., Sci Rep 2024 ほか)を基盤に展開 |
|
関連研究ハイライト |
関連ページへのリンク
研究プロジェクトの個別研究の詳細・データ・引用文献については、以下のページをご参照ください。
- 研究ハイライト(親ページ) ── 6 つの研究テーマの俯瞰
- 従来型合成致死 ── 1 対 1 対応型の合成致死戦略
- パラログ同時阻害法 ── 1 対 2 対応型の合成致死戦略
- 次世代型合成致死 ── 2 対 1/2 対 n 対応型の合成致死戦略
- データ駆動型探索 ── DepMap 再解析と USP8 発見
- グルタチオン代謝脆弱性 ── ARID1A / SMARCB1 系の代謝標的
- 既存薬の再定義 ── ゲムシタビンの新たな可能性
- 論文業績 ── 全論文・総説・代表論文
- メンバー紹介・採用情報 ── ラボ文化、連携大学院、応募・見学のご相談
- お問い合わせ・アクセス ── 共同研究・採用・取材
最終更新日: 2026-05-16

