トップページ > 共通部門のご案内 > 医療安全管理部門 > 感染制御室 > 新型コロナウイルス感染症について > 新型コロナワクチンについて
新型コロナワクチンについて
がん患者さんへの新型コロナワクチンについて
がん患者さんへの新型コロナワクチンの接種は国内外で推奨されています。(がん患者さんへの新型コロナワクチン接種Q&Aの1をご参照ください。)本内容は2025年9月29日時点の内容となります。
- がん患者さんもワクチン接種により重症化や後遺症のリスクを減らせる。
- 定期的な追加接種(ブースター)が推奨される。
- 感染時は早期の受診と抗ウイルス薬治療が重要。
ワクチンの感染・重症化予防効果オミクロン株の流行以降、ワクチンの感染予防効果は低下していますが、重症化予防効果は高く、引き続きがん患者さんへの接種が推奨されます。
がん患者さんにおけるワクチン効果がん患者さん(特に血液がん患者さん)は健常人と比較するとワクチンの効果が弱いことが知られていますが、重症化予防や後遺症のリスク低減などの効果が示されています。追加接種(ブースター接種)の重症化予防効果も示されており、定期的な接種が推奨されます。
副反応の状況がん患者さんへのワクチン接種において、健康な方と比較しても副反応の増加は見られていません。
感染時の対応ワクチン接種後でも、新型コロナウイルス感染症に感染した場合は、速やかに医療機関を受診し、さらなる重症化予防目的に抗ウイルス薬の治療を受けることが推奨されます。
がん患者さんは健常者よりワクチンの効果が劣るものの、ある程度の重症化予防効果を期待できる
抗体量の差がん患者さんにワクチンを2回接種した場合に産生される抗体量は健康な人の4分の1から20分の1程度と報告されています(参考文献[1])。
ワクチン効果の特徴産生される抗体量が少ないため、感染を予防するワクチン効果も速やかに低下しますが、重症化の予防効果は持続することが示されています(参考文献[2])。
血液がん患者さんへの効果より重症化しやすいことが知られる血液がん患者さんにおいても重症化のリスクを下げてくれることが米国の大規模データからも示されており(参考文献[3])、ワクチン接種が推奨されます。
(非がん患者さんと血液がん患者さんを比較した場合のワクチン接種後の感染リスクは血液がん患者さんの方がオッズ比(注1)4.64と高いものの、重症感染のオッズ比は1.45と差が縮まっていることが示されています。)
<参考文献>
[1]Barriere J らの報告(Eur J Cancer. 2021)(外部サイトにリンクします)
[2]Lee LYWらの報告(Lancet Oncol. 2022)(外部サイトにリンクします)
[3]Song Qらの報告(J Clin Oncol. 2022)(外部サイトにリンクします)
特に血液がん患者さんへの一部の抗がん剤治療では、ワクチンの効果が著しく落ちる場合がある
固形がん患者さん抗がん剤治療中でもワクチン接種によって産生される抗体量は大きく減少はしないという報告があります(参考文献[4])。
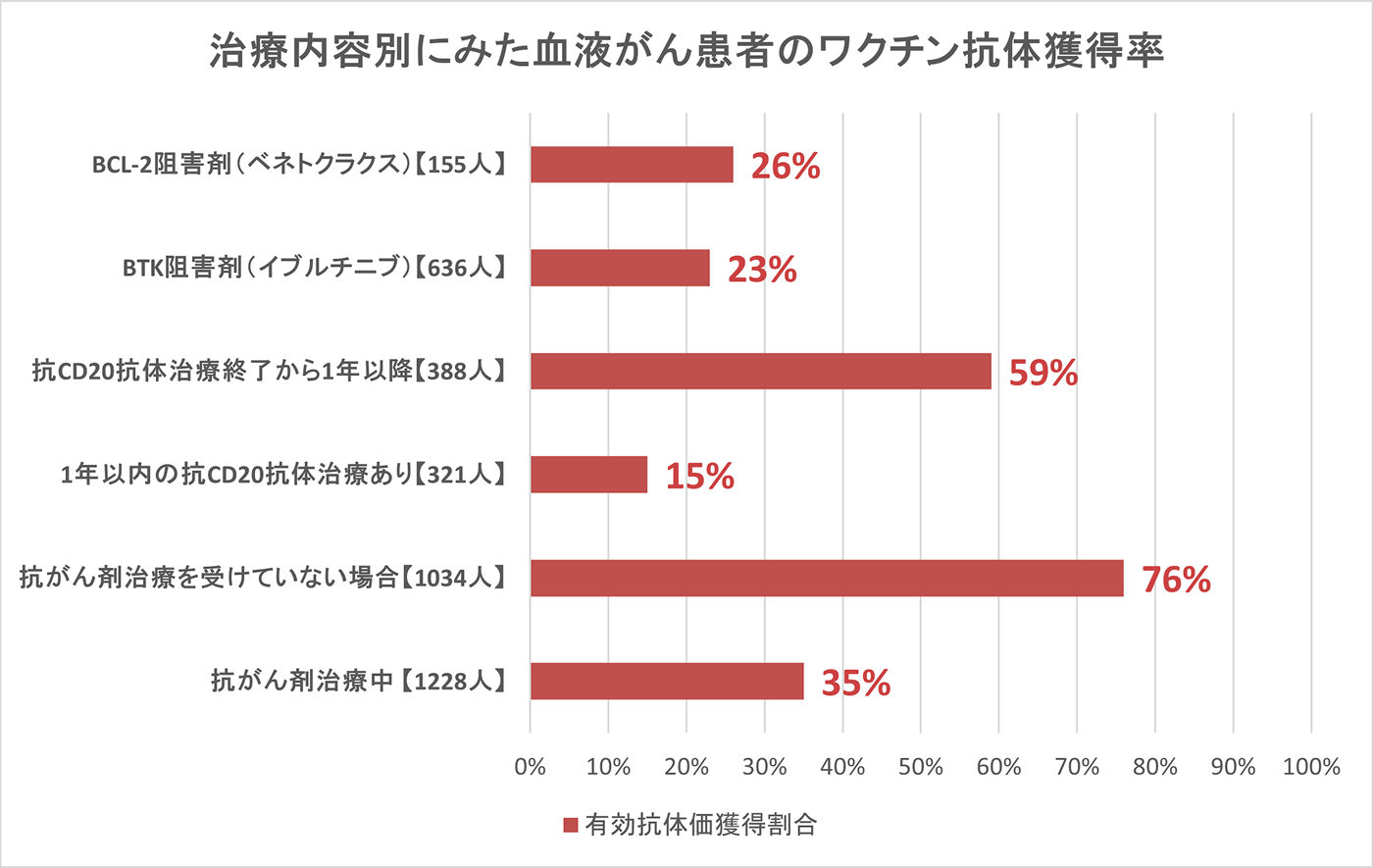
血液がんの患者さんリツキシマブやオビヌツズマブなどの抗CD20抗体薬をはじめとした一部の治療後のワクチン接種では抗体産生量が大きく減少する可能性が指摘されています(表 参考文献[5])。
同種造血幹細胞移植後1年以内は抗体産生能力が低下する可能性が指摘されています(参考文献[6])。
<参考文献>
[4]Oosting F らの報告(Lancet Oncol. 2021)(外部サイトにリンクします)
[5]Gagelmann Nらの報告(Haematologica. 2022)(外部サイトにリンクします)
[6]Maillard Aらの報告(Blood. 2022)(外部サイトにリンクします)
がん患者さんに特有の副反応が多いという報告はない
がん患者さんに特有なワクチンの副反応の存在や、副反応の割合が増えるということは報告されてい
ません(参考文献[4][7])。
免疫チェックポイント阻害剤による治療中も大きな副反応の問題はないだろうと考えられています。(参考文献[8])
<参考文献>
[4]Oosting F らの報告(Lancet Oncol. 2021)(外部サイトにリンクします)
[7]Figueiredo JCらの報告(Ann Oncol. 2022)(外部サイトにリンクします)
[8]Ma Yらの報告(J Immunother Cancer. 2021)(外部サイトにリンクします)
がん患者さんはブースター接種が推奨される
- ブースター接種を繰り返すことで、より高い抗体価が得られる。
- 感染を完全には防げないが、重症化は大幅に抑えられる。
- 血液がん患者でもブースター接種の高い効果が報告されている。
1.がん患者さんの抗体量とブースター接種
- 上記の通り、がん患者さんではより早くワクチンの効果が減衰することが示されています(参考文献[2])。このためワクチンの追加接種(ブースター接種)が勧められます。
- がん患者さんはワクチン接種をしても産生できる抗体量が健常者より少ないですが、ブースター接種によって抗体産生量が健常者に近づく可能性が指摘されています。(参考文献[9])
- がん患者さんの中でもワクチンによる抗体産生量が特に少ないとされる慢性リンパ性白血病の患者さんでも5,6回のワクチン接種で、健常者と同等の抗体産生を促せたという報告もあります。(参考文献[10])
<参考文献>
[2]Lee LYWらの報告(Lancet Oncol. 2022)(外部サイトにリンクします)
[9]Body Aらの報告(Vaccine. 2025)(外部サイトにリンクします)
[10]Roberts Tらの報告(Blood Cancer J. 2024)(外部サイトにリンクします)
2.ブースター接種による感染・重症化予防効果
がん患者さんにおけるブースター接種のワクチン効果を示す報告は数多くあります。
- オミクロン株流行期(2022年、シンガポールでのがん患者約7万人の報告)の研究では、2回目のブースター接種(合計4回目の接種)を行った人とブースター接種をしていない人と比較すると、新型コロナウイルス感染症に感染する人数は2割程度しか減少しませんでしたが、重症感染症は約9割減少することが示されています(参考文献[11])。(この研究でブースター接種をしていない人=最初の2回の接種のみの人)
- 血液がん患者さんでも、ブースター接種が感染や重症化のリスクを下げてくれることが示されています。(2回接種の患者さんと比較して、3回以上接種した患者さんの新型コロナウイルス感染症のハザード比注2は0.55、重症感染のハザード比は0.27と低いことが示されています。)(参考文献[12])
<参考文献>
[11] Tan WCらの報告(JAMA Oncol. 2023)(外部サイトにリンクします)
[12] Kevličius Lらの報告(Br J Haematol. 2024)(外部サイトにリンクします)
3.接種間隔と重症化リスク
近年では、最終接種からの期間が重症化予防効果に影響を与えるという報告もあります。
- 米国のがん患者を対象とした研究では、COVID-19に感染した場合、その直前のワクチン接種が半年以上前の接種の場合、直近半年以内の接種の場合より死亡のリスクが高い(ハザード比1.32)という報告もあります。(参考文献[13])
<参考文献>
[13] Kirkwood MKらの報告(JCO Oncology advances. 2024)(外部サイトにリンクします)

注2:ハザード比:ワクチン2回接種の患者さんと3回以上接種の患者さんが一定の期間内に新型コロナウイルス感染症にかかる確率が同じ場合はハザード比が1となります。3回以上接種の患者さんの感染する確率の方が高い場合にハザード比は1を上回ります。(つまり、ハザード比が1を超えて大きな値となるほど3回以上接種した場合の感染リスクが高く、逆に1より小さくなればなるほど感染リスクが低いということになります。)
ブースター接種をしていても、新型コロナウイルス感染症に感染した場合はできるだけ早期に医療機関を受診する
- ワクチンは重症化予防効果は高いが100%の効果ではない。
- 感染時はすぐに医療機関へ相談・受診。
- ここまでの説明の通り、ワクチンのブースター接種によって重症化を防ぐ効果が示されています。
しかし、ワクチンの効果は100%ではないため、接種しても重症化してしまう患者さんはいます。
(例:ワクチンの重症化予防効果が80%の意味:1万人のがん患者さんのうち、ワクチン未接種の場合一定期間に1000人が感染し、100人が重症化すると仮定すると、ワクチン接種は重症患者さんを100人から20人に減少させる効果があるものの、重症患者さんを0人にすることはできません。)
| 状況 | 感染症数(1万人中) | 重症化する人数 |
| ワクチン未接種 | 1,000人 | 100人 |
| ワクチン接種済み(効果80%の場合) | 1,000人 | 20人 |
- 新型コロナウイルス感染症にかかってしまったかな、と感じた際には重症化のリスクを少しでも減らすために、速やかに担当医へ相談、もしくは近医を受診し、抗ウイルス薬治療の相談をしましょう。
- 抗ウイルス薬で重症化リスクを大幅に低減。
- 薬は発症から5日以内の内服が効果的。
- 例えば、ワクチンを接種済みの高齢血液がん患者さんの重症化率(オミクロン株流行期:23.9%)をニルマトレルビル/リトナビル(パキロビッドパック®)治療によって3.1%、モルヌピラビル(ラゲブリオ®)によって5.1%に減少させることができたという報告があります。(経口抗ウイルス薬治療による重症化リスクのオッズ比0.12)(参考文献[14])
抗ウイルス薬の効果(報告例:高齢血液がん患者さん、オミクロン流行期)
| 治療 | 重症化率 |
| ワクチン接種のみ | 23.9% |
| +ニルマトレルビル/リトナビル(パキロビッドパック®) | 3.1% |
| +モルヌピラビル(ラゲブリオ®) | 5.1% |
- 抗ウイルス薬は発症から5日以内に内服を開始したほうが効果が高いことも報告されていますので、早期の受診をお勧めします。(新型コロナウイルスの抗ウイルス薬について参照)
<参考文献>
[14] Anand STらの報告(JAMA Netw Open. 2024)(外部サイトにリンクします)
ワクチン接種は罹患後症状(後遺症)のリスクも下げる
- がん患者さんの後遺症はオミクロン株流行期に減少。
- 後遺症はがん患者さんの死亡リスクを高める。
- ワクチン接種で後遺症リスクを低減。
- ブースター接種でさらに後遺症予防の可能性あり。
2021年12月から2022年1月までのがん患者さんのグローバルデータベース研究(世界中の患者さんの情報が登録されたデータベースを用いた研究)によると、がん患者さんにおける感染1-3ヵ月後も続く罹患後症状(後遺症)は減少していました(デルタ株以前の頻度16%以上→オミクロン株6.2%)。
一方で、このような後遺症はがん患者さんが亡くなるリスクとなることが示されました(ハザード比1.39)。
この研究の中で、がん患者さんが亡くなる理由の一つとして、後遺症によって治療の継続が困難となることが挙げられます。
この研究の中で、がん患者さんへのワクチン接種による後遺症のオッズ比が0.41とワクチン接種が後遺症のリスクを減少させることが示されました(参考文献[15])。
この研究では、ブースター接種によって後遺症の割合をさらに減少させる可能性も示唆されています。
<参考文献>
[15] Cortellini Aらの報告(Lancet Oncol. 2023)(外部サイトにリンクします)


