トップページ > 共通部門のご案内 > 支持療法開発部門 > 支持療法・緩和治療領域研究ポリシー
支持療法・緩和治療領域研究ポリシー
支持療法・緩和治療領域研究ポリシーについて
支持療法開発センターでは、日本医療研究開発機構(AMED)の支援を受けて、支持・緩和領域の臨床研究および新規治療開発の推進に欠かせない「支持療法・緩和治療領域研究ポリシー」を作成しております。
本ページで公開しているポリシーを支持療法・緩和治療領域の臨床研究立案にお役立てください。
支持療法・緩和治療領域研究ポリシー(総論)
「支持療法・緩和治療領域研究ポリシー(総論)」の作成をオールジャパン体制ですすめ、2018年12月完成に至りプレスリリースを行いました。プレスリリースの詳細は国立がん研究センターの広報活動のページをご覧ください。今後は、このポリシーに則った質の高い臨床研究を支持療法・緩和治療領域で推進していきます。
なお、臨床試験立案の際に「支持療法・緩和治療領域研究ポリシー(総論)」を参照した場合には参考文献として下記を明示ください。
Sadamoto Zenda, Yosuke Uchitomi, Tatsuya Morita, Takuhiro Yamaguchi, Akira Inoue. Establishment of a research policy for supportive and palliative care in Japan. Japanese Journal of Clinical Oncology:1-7、2021
例)
・This clinical trial was conducted with reference (according) to a research policy for supportive and palliative care in Japan11).
・This prospective study was conducted according to a research policy for supportive and palliative care in Japan11).
支持療法・緩和治療領域研究ポリシー(各論)の公開
支持療法開発センターでは日本医療研究開発機構(AMED)の支援を受け「支持療法・緩和治療領域研究ポリシー(各論)」の作成を進めております。
「支持療法・緩和治療領域研究ポリシー(各論)」は「支持療法・緩和治療研究ポリシー(総論)」で述べられている研究方法論をもとに、「各領域・テーマにした研究を行う場合どのように進めていけばよいか」という具体的な研究者の悩みに応える形で作成しています。
作成にあたりワーキンググループによる議論を重ねたのち、J-SUPPORTでの校閲、関連学会による査読、パブリックコメント募集を行います。
図:ポリシー(各論)作成の流れ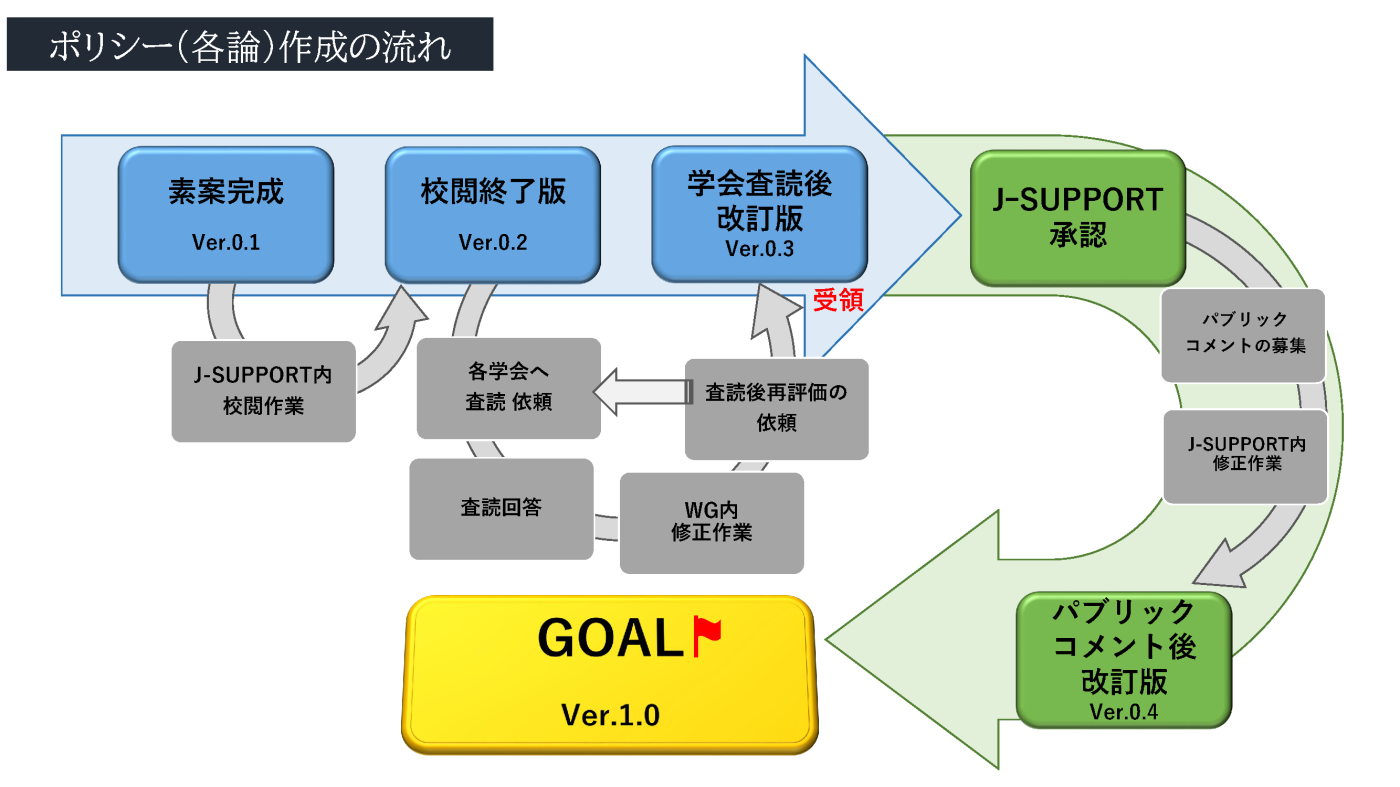
「化学療法誘発性悪心・嘔吐(CINV)」
このたび「支持療法・緩和治療領域研究ポリシー(各論):化学療法誘発性悪心・嘔吐(CINV:Chemotherapy Induced Nausea and Vomiting)」が完成しましたので公開します。(2021年10月1日公開)
公開にあたり2021年7月16日から7月30日までパブリックコメント募集を行い、寄せられたご意見を参照のうえ大きな修正は行わず2021年10月1日にVer1.0が完成しました。
「粘膜炎(口腔粘膜炎)」
2021年8月16日にVer1.0が完成・公開しました。
公開にあたり2021年6月14日から6月28日までパブリックコメント募集を行いました。
誤記訂正のため8月25日に改訂を行いました。
「呼吸困難 Dyspnea/Breathlessness」
2021年4月1日にVer1.0が完成・公開しました。公開にあたり2021年1月25日から2月7日までパブリックコメント募集を行いました。
「支持/緩和治療領域研究における研究者主導二重盲検比較試験を実施する際のプラセボ薬剤の設定に関する考え方」
2021年3月に公開しました。ISPORタスクフォース報告書(日本語訳)の公開
支持・緩和治療領域研究ポリシーの開発の一環として臨床アウトカム評価(Clinical Outcome Assessments: COA)ワーキンググループが翻訳を行った、「ISPORタスクフォース報告書 臨床アウトカム評価:概念的基盤―ISPOR臨床アウトカム評価報告書アウトカム研究のための新たな実施基準タスクフォース」が、『薬理と治療(JPT)』出版社の、患者報告アウトカム(Patient-Reported Outcome:PRO)評価関連 特設ページにて一般公開されました。
- ライフサイエンス出版株式会社
患者報告アウトカム(Patient-Reported Outcome:PRO)評価関連 特設ページ(外部サイトにリンクします)
この特設ページは厚生労働省科学研究班開発 患者報告アウトカム(Patient-Reported Outcome:PRO)使用についてのガイダンス集として発行されたものであり、本報告書はPRO評価の関連資料「臨床試験のためのPRO使用ガイダンス」関連文献日本語訳に掲載されています。
本報告書は、COA測定の原則を理解するために重要で基本的な定義を提供し、測定特性に影響を与えうる患者評価および臨床試験の要因の本質的な属性について解説した報告書の翻訳です。評価を開発するとき、または改良するときにこれらの要因を考慮すべきであり、これらの考慮事項は研究者が試験をデザインする際に既存の評価を用いるか、それとも新しいアウトカム評価を開発するかを選択するのに役立つ報告書です。
特設ページでは本報告書のほかにも、臨床試験の立案や解釈、また評価結果の臨床現場や社会への積極的な応用を考えている研究者に役立つ、患者報告アウトカム(Patient-Reported Outcome:PRO)使用に関する様々な資料を参照することができます。